11.下列除杂选用试剂正确的是( )
| A. | 用过量的O2除去CO2中的CO | B. | 用过量的HC1溶液除去Cu中CuO | ||
| C. | 用过量的NaOH除去CaCl2溶液中HCl | D. | 用过量的FeSO4,除去Zn中Fe |
10.规范的实验操作是实验成功的关键.下列实验操作正确的是( )
| A. | 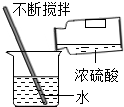 | B. | 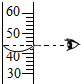 | C. | 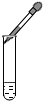 | D. | 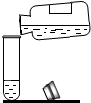 |
9.目前H7N9病毒局部流行,造成人员伤亡,治疗费用巨大.达菲(C16H31N2PO8)是目前用来治疗该型流感患者的重要药物之一.下列有关达菲的说法正确的是( )
| A. | 一个达菲分子中含有一个N2分子 | |
| B. | 达菲分子中C、N、0、P的原子个数比是8:1:4:1 | |
| C. | 达菲由五种元素组成 | |
| D. | 达菲相对分子质量为410g |
8.环境、能源和资源是人类生存和发展的基本条件.下列说法不正确的是( )
| A. | 二氧化硫的产生主要原因是煤的大量燃烧 | |
| B. | 海底埋藏着大量的可燃冰,它不可能成为未来的新能源 | |
| C. | 氢气极易燃烧,燃烧的产物是水,被认为是最淸洁的燃料 | |
| D. | 化石燃料面临被耗尽的危险,人类正在利用和开发新的能源.如太阳能、风能、地热能等 |
6.同学们运用对比的学习方法探究碱的性质.
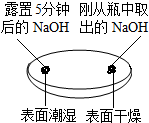
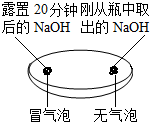
(1)由实验一、二可知,氢氧化钠会吸收空气的H2O、CO2,因此要密封保存.
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,对比A瓶与C(选填“B”或“C”)瓶的实验现象可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别氢氧化钠溶液与氢氧化钙两种饱和溶液.
(4)某同学发现工业上使用的氢氧化钠固体标签如图所示,于是对其成分进行了探究:

【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】
①在化工生产中,原料往往不能完全转化为产品.
②工业上制取NaOH的反应原理是:2NaCl+2H2O$\stackrel{通电}{→}$2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体.
③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
【提出猜想】氢氧化钠中含有的杂质为碳酸钠和氯化钠.提出上述猜想的理由是原料中的NaCl未完全反应,氢氧化钠与空气中的二氧化碳反应生成碳酸钠.
【进行实验】取固体于试管中,加水溶解并向溶液中加入过量稀盐酸
【实验结论】溶液中有明显现象,证明杂质中一定含有碳酸钠.
【反思评价】该同学想进一步证明固体中的氢氧化钠,实验方案是取少量固体于试管中加水溶解,加入过量的氯化钙溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液,溶液变红,则固体中含有氢氧化钠.
(5)某碳酸钠样品中含有少量氯化钠.现称量11g该样品放入烧杯中,然后加入一定量溶质的质量分数为14.6%的稀盐酸,至恰好完全反应,去除溶液中的水分,最终得到12.1g氯化钠固体.计算:
①碳酸钠样品中碳酸钠的质量;
②反应后所得溶液中溶质的质量分数.(结果精确到0.1%)
| 实验一 观察固体表面 | 实验二 向两块固体表面滴加稀盐酸 | 实验三 振荡3个塑料瓶 |
 |  | 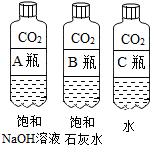 |
(2)实验三中可观察到三个软塑料瓶变瘪的程度大小为A>B>C,对比A瓶与C(选填“B”或“C”)瓶的实验现象可证明CO2能与NaOH发生反应.
(3)同学们设计如下两种方案鉴别氢氧化钠溶液与氢氧化钙两种饱和溶液.
| 实验一 | 实验二 | 分析 |
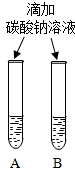 | 微热(不考虑水分蒸发)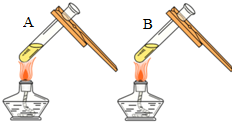 | 两种方案中均观察到A试管内出现白色浑浊,则A中溶液为饱和氢氧化钙溶液;;方案二的设计原理是氢氧化钙的溶解度随温度升高而减小,氢氧化钠的溶解度随温度升高而增大. |

【提出问题】氢氧化钠中含有什么杂质?
【查阅资料】
①在化工生产中,原料往往不能完全转化为产品.
②工业上制取NaOH的反应原理是:2NaCl+2H2O$\stackrel{通电}{→}$2NaOH+H2↑+Cl2↑,然后蒸发溶剂获得NaOH固体.
③碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
【提出猜想】氢氧化钠中含有的杂质为碳酸钠和氯化钠.提出上述猜想的理由是原料中的NaCl未完全反应,氢氧化钠与空气中的二氧化碳反应生成碳酸钠.
【进行实验】取固体于试管中,加水溶解并向溶液中加入过量稀盐酸
【实验结论】溶液中有明显现象,证明杂质中一定含有碳酸钠.
【反思评价】该同学想进一步证明固体中的氢氧化钠,实验方案是取少量固体于试管中加水溶解,加入过量的氯化钙溶液使沉淀完全,静置后向上层清液中滴加酚酞溶液,溶液变红,则固体中含有氢氧化钠.
(5)某碳酸钠样品中含有少量氯化钠.现称量11g该样品放入烧杯中,然后加入一定量溶质的质量分数为14.6%的稀盐酸,至恰好完全反应,去除溶液中的水分,最终得到12.1g氯化钠固体.计算:
①碳酸钠样品中碳酸钠的质量;
②反应后所得溶液中溶质的质量分数.(结果精确到0.1%)
4.葡萄糖是生命体所需能量的主要来源.
【提出问题】葡萄糖的燃烧产物是CO2和H2O,由此能否证明葡萄糖是只由碳元素和氢元素组成的有机物?
【实验设计】为了确定葡萄糖的元素组成,某小组设计了如图实验(其中浓硫酸、无水CaCl2均为常用干燥剂,部分固定装置省略).
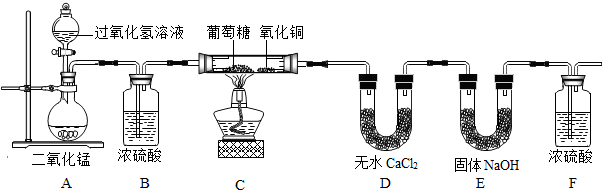
(1)装置B中浓硫酸的作用是吸收从A中溢出的水蒸气.
(2)装置C处氧化铜的作用是将葡萄糖不完全燃烧产生的少量CO氧化成CO2,保证葡萄糖中的碳都转化为CO2.
【方案评价】
(1)用充有空气的储气球代替装置A,是否更有利于实验的进行?原因是否;空气中的CO2会干扰实验结果的测定.
【数据处理】下表是同学们填写的实验报告,请你帮助完成.
【讨论交流】
从定量实验的角度看,为了尽量减少误差:,该实验是否可进一步改进?请简要写出一个改进意见:
将F换成装有NaOH的干燥管,同时吸收空气中的CO2和H2O,减少实验误差.
【提出问题】葡萄糖的燃烧产物是CO2和H2O,由此能否证明葡萄糖是只由碳元素和氢元素组成的有机物?
【实验设计】为了确定葡萄糖的元素组成,某小组设计了如图实验(其中浓硫酸、无水CaCl2均为常用干燥剂,部分固定装置省略).

(1)装置B中浓硫酸的作用是吸收从A中溢出的水蒸气.
(2)装置C处氧化铜的作用是将葡萄糖不完全燃烧产生的少量CO氧化成CO2,保证葡萄糖中的碳都转化为CO2.
【方案评价】
(1)用充有空气的储气球代替装置A,是否更有利于实验的进行?原因是否;空气中的CO2会干扰实验结果的测定.
【数据处理】下表是同学们填写的实验报告,请你帮助完成.
| 实验事实 | 数据分析及结论 |
| 1.8g葡萄糖完全燃烧,得到2.64g CO2和1.08g H2O | 根据数据分析可得出结论: 葡萄糖中含有C、H、O元素. |
从定量实验的角度看,为了尽量减少误差:,该实验是否可进一步改进?请简要写出一个改进意见:
将F换成装有NaOH的干燥管,同时吸收空气中的CO2和H2O,减少实验误差.
3.某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了两个实验:CuSO4溶液分别与NaOH溶液、BaCl2溶液反应.实验结束后将两实验中的废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色.
(1)写出废液混合后使滤液变无色时一定发生的反应的化学方程式:CuCl2+2NaOH=Cu(OH)2↓+2NaCl.
(2)取少量滤液于试管中,滴入紫色石蕊试液,石蕊溶液仍为紫色,则滤液呈中性(填“酸”、“中”、“碱”).
(3)该小组的同学对滤液中溶质的成分继续进行了如下探究实验:
【提出问题】滤液中溶质的成分是什么?
【作出猜想】猜想Ⅰ:NaCl;猜想ⅡNaCl、BaCl2;猜想ⅢNaCl、Na2SO4.
【实验探究】
在实验②的溶液中滴加无色酚酞溶液,观察到酚酞溶液变成红色.
【交流拓展】要使蓝色溶液变成无色,还可以用不同于上述原理的方法,即在蓝色溶液中加入足量的锌.
0 150446 150454 150460 150464 150470 150472 150476 150482 150484 150490 150496 150500 150502 150506 150512 150514 150520 150524 150526 150530 150532 150536 150538 150540 150541 150542 150544 150545 150546 150548 150550 150554 150556 150560 150562 150566 150572 150574 150580 150584 150586 150590 150596 150602 150604 150610 150614 150616 150622 150626 150632 150640 211419
(1)写出废液混合后使滤液变无色时一定发生的反应的化学方程式:CuCl2+2NaOH=Cu(OH)2↓+2NaCl.
(2)取少量滤液于试管中,滴入紫色石蕊试液,石蕊溶液仍为紫色,则滤液呈中性(填“酸”、“中”、“碱”).
(3)该小组的同学对滤液中溶质的成分继续进行了如下探究实验:
【提出问题】滤液中溶质的成分是什么?
【作出猜想】猜想Ⅰ:NaCl;猜想ⅡNaCl、BaCl2;猜想ⅢNaCl、Na2SO4.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 实验①:取少量滤液于试管中,加入适量的纯碱溶液,振荡. | 无明显现象 | 猜想Ⅱ不成立 |
| 实验②取少量滤液于试管中,加入适量的氢氧化钡溶液,振荡 | 产生白色沉淀 | 猜想Ⅲ成立 |
【交流拓展】要使蓝色溶液变成无色,还可以用不同于上述原理的方法,即在蓝色溶液中加入足量的锌.
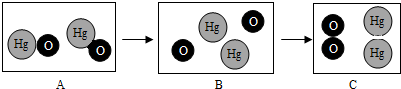
 ”和“
”和“ ”分别表示氧原子和汞原子,如图是氧化汞在加热条件下发生分解反应的微观模拟图.请回答下列问题:
”分别表示氧原子和汞原子,如图是氧化汞在加热条件下发生分解反应的微观模拟图.请回答下列问题: