18.实验室中区分下列各组物质的两种方法不都正确的是( )
| 选项 | 需要区分的物质 | 实验方法 | |
| A | 磷酸钙和氯化铵 | 溶于水 | 与熟石灰混合研磨 |
| B | 氢氧化钠固体和熟石灰 | 将两种固体溶于水 | 溶于水,向所得溶液中分别吹入CO2气体 |
| C | 硫酸钾和碳酸钾 | 加硝酸钡溶液 | 加水溶解 |
| D | 硬水和软水 | 肥皂水 | 加热、煮沸 |
| A. | A | B. | B | C. | C | D. | D |
17.下列实验操作叙述正确的是( )
| A. | 实验用剩的药品应放回原试剂瓶中 | |
| B. | 切割白磷时应该在水下进行 | |
| C. | 测某酸性溶液的pH时,先用水将pH试纸湿润 | |
| D. | 在“粗盐中难溶性杂质的去除”实验中,将蒸发皿中的溶液直接蒸干 |
16.对下列事实的微观解释正确的是( )
| 选项 | 事实 | 解释 |
| A | CO有毒,而CO2无毒 | 两物质的组成元素不同,分子构成不同 |
| B | KNO3溶液能导电 | 溶液中存在自由移动的粒子 |
| C | KCl溶液和KMnO4溶液颜色不同 | 溶液中阴离子不同 |
| D | 稀硫酸和稀盐酸具有相似的化学性质 | 因为它们都含氢元素 |
| A. | A | B. | B | C. | C | D. | D |
15.雯雯在自学碳酸钠性质时,查到了以下资料:
①CO2+Na2CO3+H2O═2NaHCO3,CO2通入饱和碳酸钠溶液会产生白色沉淀,CO2不溶于饱和碳酸氢钠溶液.
②碳酸钠、碳酸氢钠在不同温度下的溶解度
【进行实验1】验证CO2通入饱和碳酸钠溶液会产生白色沉淀
①配制碳酸钠溶液:取100g 20℃的水,加入35g碳酸钠固体,搅拌后,静置,取上层清液.
②利用装置一进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2.
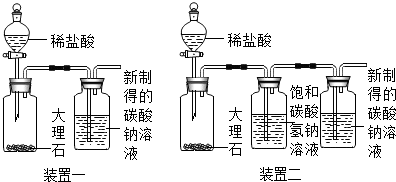
【发现问题】实验中,始终没有看到沉淀现象,原因是什么呢?雯雯进行了以下实验探究.
【进行实验2】
(1)在0℃~30℃,Na2CO3和NaHCO3的溶解度受温度变化影响较大的是碳酸钠.
(2)大理石与稀盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)装置二中饱和碳酸氢钠溶液的作用是吸收氯化氢气体,从而排除氯化氢气体对实验的干扰.
【进行实验3】
(4)雯雯在最初的实验中没有看到沉淀现象的原因是配制的碳酸钠溶液没有达到饱和.
(5)CO2通入饱和碳酸钠溶液会产生白色沉淀的原因是碳酸氢钠溶解度小于碳酸钠,水减少,生成的碳酸氢钠的质量大于反应的碳酸钠.
(6)请你依据题中信息,写出一种能够区分碳酸钠和碳酸氢钠固体的实验方案.
①CO2+Na2CO3+H2O═2NaHCO3,CO2通入饱和碳酸钠溶液会产生白色沉淀,CO2不溶于饱和碳酸氢钠溶液.
②碳酸钠、碳酸氢钠在不同温度下的溶解度
| 0℃ | 10℃ | 20℃ | 30℃ | |
| Na2CO3 | 7.1 | 12.2 | 21.8 | 39.7 |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 |
①配制碳酸钠溶液:取100g 20℃的水,加入35g碳酸钠固体,搅拌后,静置,取上层清液.
②利用装置一进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2.

【发现问题】实验中,始终没有看到沉淀现象,原因是什么呢?雯雯进行了以下实验探究.
【进行实验2】
| 实验操作 | 实验现象 |
| ①取100g 20℃的水,加入35g碳酸钠固体,搅拌后,静置,取上层清液 ②利用装置二进行实验,连续5分钟向新制得的碳酸钠溶液中通入CO2 | 没有出现白色沉淀 |
(2)大理石与稀盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)装置二中饱和碳酸氢钠溶液的作用是吸收氯化氢气体,从而排除氯化氢气体对实验的干扰.
【进行实验3】
| 实验操作 | 实验现象 |
| ①取100g热开水,加入35g碳酸钠固体,完全溶解,再降温至20℃,取上层清液 ②利用装置一和装置二分别进行实验,连续3分钟向新制得的碳酸钠溶液中通入CO2 | 装置一和装置二中的碳酸钠溶液中均出现白色沉淀 |
(5)CO2通入饱和碳酸钠溶液会产生白色沉淀的原因是碳酸氢钠溶解度小于碳酸钠,水减少,生成的碳酸氢钠的质量大于反应的碳酸钠.
(6)请你依据题中信息,写出一种能够区分碳酸钠和碳酸氢钠固体的实验方案.
14.学校化学兴趣小组知道二氧化锰能做过氧化氢分解的催化剂后,在想探究其他一些物质如氧化铝是否也可做过氧化氢的催化剂.请你一起参与他们的探究过程,并填写下列空白.
(1)【问题】氧化铝能不能做过氧化氢分解的催化剂?
(2)【猜想】氧化铝能做过氧化氢分解的催化剂
(3)【实验验证】
(4)【结论】氧化铝能加快过氧化氢的分解速率,故氧化铝能做过氧化氢分解的催化剂
(5)【讨论与反思】经过讨论,有的同学认为只有上述两个证据,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:【实验目的】探究Al2O3在反应前后质量是否改变.
【实验步骤】①准确称量氧化铝(少量)的质量;②完成实验二③待反应结束,将实验而试管里的物质进行过滤,洗涤,干燥,称量;对比反应前后氧化铝的质量.
【讨论】如果氧化铝在反应前后质量不变,则说明氧化铝可以作过氧化氢分解的催化剂.
(6)但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究Al2O3的化学性质在反应前后是否改变.
(1)【问题】氧化铝能不能做过氧化氢分解的催化剂?
(2)【猜想】氧化铝能做过氧化氢分解的催化剂
(3)【实验验证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 将带火星的木条伸入装有过氧化氢溶液的试管中 不用填 | 木条不复燃 | 常温下过氧化氢溶液分解速率太 慢,产生的氧气太少 |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量氧化铝,再将带火星木条 伸入试管中 | 木条复燃 | Al2O3能作过氧化氢分解的催化剂 不用填 |
(5)【讨论与反思】经过讨论,有的同学认为只有上述两个证据,不能证明氧化铝能作过氧化氢分解的催化剂,还要补充一个探究实验:
实验三:【实验目的】探究Al2O3在反应前后质量是否改变.
【实验步骤】①准确称量氧化铝(少量)的质量;②完成实验二③待反应结束,将实验而试管里的物质进行过滤,洗涤,干燥,称量;对比反应前后氧化铝的质量.
【讨论】如果氧化铝在反应前后质量不变,则说明氧化铝可以作过氧化氢分解的催化剂.
(6)但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验:探究Al2O3的化学性质在反应前后是否改变.
9.在题后横线上简要说明下列操作可能造成的不良后果.
(1)倾倒细口瓶里的药液时,标签没向着手心药品腐蚀标签
(2)实验剩余的药品放回原瓶污染原瓶药品
(3)将块状的固体药品直接投入竖直的试管中将试管砸破.
0 150435 150443 150449 150453 150459 150461 150465 150471 150473 150479 150485 150489 150491 150495 150501 150503 150509 150513 150515 150519 150521 150525 150527 150529 150530 150531 150533 150534 150535 150537 150539 150543 150545 150549 150551 150555 150561 150563 150569 150573 150575 150579 150585 150591 150593 150599 150603 150605 150611 150615 150621 150629 211419
(1)倾倒细口瓶里的药液时,标签没向着手心药品腐蚀标签
(2)实验剩余的药品放回原瓶污染原瓶药品
(3)将块状的固体药品直接投入竖直的试管中将试管砸破.
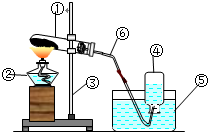 如图是实验室用加热高锰酸钾的方法制取氧气的装置图
如图是实验室用加热高锰酸钾的方法制取氧气的装置图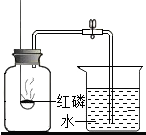 如图是实验室测定空气中氧气的体积分数的实验装置
如图是实验室测定空气中氧气的体积分数的实验装置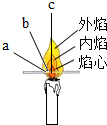 某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格.
某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格.