12. 小明查阅资料得知,过氧化氢分解反应的催化剂除二氧化锰外,还有氯化铁溶液、氯化铜溶液中的金属离子和土豆中含有的过氧化氢酶等.他通过如下实验进行相关研究.
小明查阅资料得知,过氧化氢分解反应的催化剂除二氧化锰外,还有氯化铁溶液、氯化铜溶液中的金属离子和土豆中含有的过氧化氢酶等.他通过如下实验进行相关研究.
(1)对二氧化锰在过氧化氢分解反应中的作用,下列分析正确的是B.
A.二氧化锰能使过氧化氢分解产生的氧气总质量增加
B.二氧化锰能使过氧化氢分解速度变大,但是产生氧气总质量不变
C.二氧化锰能使过氧化氢分解速度变大,产生的氧气总质量变大
(2)研究催化剂的某些因素对过氧化氢分解速率的影响
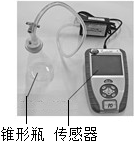
实验一:分别取20mL 5%的过氧化氢溶液于3个大小相同的锥形瓶中.向其中两个锥形瓶中分别加入含相同数目金属离子的氯化铁溶液和氯化铜溶液,分别连接传感器测体系压强(如图所示).
测定数据如下表所示:
①加入含相同数目金属离子的氯化铁溶液和氯化铜溶液,该步操作的实验目的是控制催化剂中金属离子的数量相同,对比它们种类对过氧化氢分解的速率影响.
②根据上表数据得出的结论是铁离子对过氧化氢的催化效果强于铜离子.
实验二:从一块土豆的同一部位取2个质量均为1.7g的正方体土豆块,将其中一块切成若干片,片与片相连不断开,将两份土豆同时分别放入盛30mL 5%过氧化氢溶液的50mL量筒中.观察到两量筒内均有气泡生成,一段时间后,只有土豆片不断上升,而土豆块不能上浮.通过实验得出的结论是反应物和催化剂的接触面积越大,反应速率越快.
 小明查阅资料得知,过氧化氢分解反应的催化剂除二氧化锰外,还有氯化铁溶液、氯化铜溶液中的金属离子和土豆中含有的过氧化氢酶等.他通过如下实验进行相关研究.
小明查阅资料得知,过氧化氢分解反应的催化剂除二氧化锰外,还有氯化铁溶液、氯化铜溶液中的金属离子和土豆中含有的过氧化氢酶等.他通过如下实验进行相关研究.(1)对二氧化锰在过氧化氢分解反应中的作用,下列分析正确的是B.
A.二氧化锰能使过氧化氢分解产生的氧气总质量增加
B.二氧化锰能使过氧化氢分解速度变大,但是产生氧气总质量不变
C.二氧化锰能使过氧化氢分解速度变大,产生的氧气总质量变大
(2)研究催化剂的某些因素对过氧化氢分解速率的影响
实验一:分别取20mL 5%的过氧化氢溶液于3个大小相同的锥形瓶中.向其中两个锥形瓶中分别加入含相同数目金属离子的氯化铁溶液和氯化铜溶液,分别连接传感器测体系压强(如图所示).
测定数据如下表所示:
| 时间/s 试剂 压强/KPa | 0 | 60 | 120 | 180 | 240 | 300 |
| 20mL 5%的过氧化氢溶液 | 101.86 | 102.99 | 103.42 | 103.67 | 103.99 | 104.00 |
| 加入氯化铁溶液 | 102.21 | 105.35 | 115.40 | 129.69 | 145.52 | 163.99 |
| 加入氯化铜溶液 | 101.50 | 102.73 | 107.53 | 114.78 | 122.49 | 130.39 |
②根据上表数据得出的结论是铁离子对过氧化氢的催化效果强于铜离子.
实验二:从一块土豆的同一部位取2个质量均为1.7g的正方体土豆块,将其中一块切成若干片,片与片相连不断开,将两份土豆同时分别放入盛30mL 5%过氧化氢溶液的50mL量筒中.观察到两量筒内均有气泡生成,一段时间后,只有土豆片不断上升,而土豆块不能上浮.通过实验得出的结论是反应物和催化剂的接触面积越大,反应速率越快.
9.某学校的化学学习小组在实验时,用到了三个分别盛有Na2CO3溶液、NaOH溶液和NaCl溶液的试剂瓶,李铭发现王潇在取用溶液时,用一支滴管分别取用了三种溶液,且在取用时没有将滴管进行清洗,他认为王潇的操作不规范,这样会使试剂瓶中的溶液受污染而无法再次使用,于是学习小组就盛有NaCl溶液的试剂瓶是否被另外两种溶液污染了而进行如下探究:
【提出问题】该滴瓶中溶质的成分是什么?
【提出猜想】
猜想Ⅰ:溶质成分只有:NaCl.
猜想Ⅱ:溶质成分为:NaCl和NaOH.
猜想Ⅲ:溶质成分为:NaCl和Na2CO3
猜想Ⅳ:溶质成分为:NaCl、NaOH和Na2CO3
【实验探究】为验证猜想,李铭设计了如下的实验方案,请你极爱你过实验步骤补充完整.
步骤(2)中发生的化学反应方程式为BaCl2+Na2CO3═BaCO3↓+2NaCl.
【得出结论】猜想Ⅳ成立.
【实验反思】王潇认为凭借上述的实验步骤并不能排除猜想Ⅲ成立的可能性,因为碳酸钠的溶液碱性.
【实验改进】
找出问题后,该实验小组同学将实验步骤进行了调整,他们先进行了步骤(2),再进行步骤(1),为保证结论准确且实验现象便于观察,先加入的试剂应该足量(选填“足量”或“少量”),且两个步骤之间需要进行的实验操作是过滤,请写出该步骤需要用到的一种玻璃仪器玻璃棒.
【提出问题】该滴瓶中溶质的成分是什么?
【提出猜想】
猜想Ⅰ:溶质成分只有:NaCl.
猜想Ⅱ:溶质成分为:NaCl和NaOH.
猜想Ⅲ:溶质成分为:NaCl和Na2CO3
猜想Ⅳ:溶质成分为:NaCl、NaOH和Na2CO3
【实验探究】为验证猜想,李铭设计了如下的实验方案,请你极爱你过实验步骤补充完整.
| 实验操作 | 实验结果 |
| (1)取少量试剂瓶内溶液于试管中,并加入过量酚酞试液. | 溶液呈红色 |
| (2)再向上述溶液中加入适量BaCl2溶液. | 有白色沉淀生成 |
【得出结论】猜想Ⅳ成立.
【实验反思】王潇认为凭借上述的实验步骤并不能排除猜想Ⅲ成立的可能性,因为碳酸钠的溶液碱性.
【实验改进】
找出问题后,该实验小组同学将实验步骤进行了调整,他们先进行了步骤(2),再进行步骤(1),为保证结论准确且实验现象便于观察,先加入的试剂应该足量(选填“足量”或“少量”),且两个步骤之间需要进行的实验操作是过滤,请写出该步骤需要用到的一种玻璃仪器玻璃棒.
7.为研究影响化学反应快慢的因素,小明选取成分相同的大理石碎屑、块状大理石两种样品各6克,分别与足量的、溶质质量分数相同的稀盐酸反应(样品中杂质不与稀盐酸反应),实验装置如图.每2分钟测量C装置中吸收到的由反应过程中产生的二氧化碳的质量,并记录前18分钟数据如表.(碳酸钙与稀盐酸反应的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑)
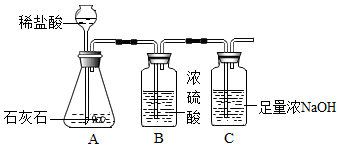
(1)B装置的作用是吸收水分,干燥气体.
(2)本实验测量石灰石中CaCO3的质量分数比实际石灰石中CaCO3的质量分数小.试分析可能原因是反应装置中生成的二氧化碳没有全部被排出.
(3)结合表格分析,块状大理石与稀盐酸反应最多能生成多少克二氧化碳?简要说明判断的理由:2.40g,大理石碎屑生成的CO2质量是2.40g,而块状大理石和大理石碎屑的成分、质量相同..

| 时间/分 | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 |
| 大理石碎屑生成的CO2质量/克 | 0 | 1.45 | 1.75 | 1.98 | 2.18 | 2.30 | 2.36 | 2.40 | 2.40 | 2.40 |
| 块状大理石生成的CO2质量/克 | 0 | 0.45 | 0.80 | 1.10 | 1.36 | 1.60 | 1.81 | 1.98 | 2.11 | 2.20 |
(2)本实验测量石灰石中CaCO3的质量分数比实际石灰石中CaCO3的质量分数小.试分析可能原因是反应装置中生成的二氧化碳没有全部被排出.
(3)结合表格分析,块状大理石与稀盐酸反应最多能生成多少克二氧化碳?简要说明判断的理由:2.40g,大理石碎屑生成的CO2质量是2.40g,而块状大理石和大理石碎屑的成分、质量相同..
6.随着人们对酒驾危害认识的加深,司法机关对于酒驾、醉驾的处罚将日趋加重.醉酒的原因是酒中含有的乙醇对人的神经系统有刺激作用.交警对呼气酒精检验的原理是:
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸.小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】
材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性.在加热条件下,可以把氧化铜还原为单质铜.
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性.
【提出猜想】
猜想1:只有乙醇
猜想2:只有乙酸
猜想3:乙醇和乙酸.
【实验探究】
【实验反思】
(1)操作①能否改为“将加热后的表面有黑色氧化铜的铜丝插入盛有白酒的试管中”?不能,理由是乙酸也能使铜丝表面由黑色变为红色.
(2)K2Cr2O7中铬元素的化合价为+6.
白酒是乙醇的水溶液,酒中的乙醇在微生物作用下能被氧化成乙酸.小刚家有一瓶密封存放的白酒,他想知道该白酒的组成情况,于是进行如下实验探究:
【提出问题】该白酒中的溶质主要有哪些?
【查阅资料】
材料一:乙醇(C2H5OH),俗称酒精,易溶于水,水溶液呈中性.在加热条件下,可以把氧化铜还原为单质铜.
材料二:乙酸(CH3COOH),又名醋酸,易溶于水,具有酸的通性.
【提出猜想】
猜想1:只有乙醇
猜想2:只有乙酸
猜想3:乙醇和乙酸.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量白酒于试管中,滴入几滴橙色的K2Cr2O7酸性溶液 | 溶液变成蓝绿色 | 猜想1成立 |
| ②取少量白酒于试管中,滴入几滴紫色石蕊试液 | 石蕊试液不变色 |
(1)操作①能否改为“将加热后的表面有黑色氧化铜的铜丝插入盛有白酒的试管中”?不能,理由是乙酸也能使铜丝表面由黑色变为红色.
(2)K2Cr2O7中铬元素的化合价为+6.
5.已知2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3 被称为“铝热反应”.镁和氧化铜也能发生类似的反应,其化学方程式是Mg+CuO$\frac{\underline{\;高温\;}}{\;}$Cu+MgO.
某小组同学在实验室中进行镁和氧化铜反应的实验,充分反应后对于固体剩余物进行了实验探究.
【提出问题】固体剩余物是什么?
【猜想假设】假设①铜和氧化镁;假设②铜、氧化镁和氧化铜;假设③铜、氧化镁和镁.
【查阅资料一】大多数金属氧化物都能与盐酸反应生成金属氯化物和水(反应中元素化合价不发生改变).【实验探究】请完成下列实验.
【思考】是否任何一种金属单质都能与另一种金属氧化物反应?
【查阅资料二】该小组同学通过查阅资料,获得以下几组反应信息.
【总结】根据上表对比分析得出:金属单质与金属氧化物能发生反应,需满足的条件是金属单质的活动性比金属氧化物中所含金属的活动性强.
某小组同学在实验室中进行镁和氧化铜反应的实验,充分反应后对于固体剩余物进行了实验探究.
【提出问题】固体剩余物是什么?
【猜想假设】假设①铜和氧化镁;假设②铜、氧化镁和氧化铜;假设③铜、氧化镁和镁.
【查阅资料一】大多数金属氧化物都能与盐酸反应生成金属氯化物和水(反应中元素化合价不发生改变).【实验探究】请完成下列实验.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体剩余物于试管中, 向其中加入足量的稀盐酸. | 固体部分溶解,溶液为无色. | 假设①成立. |
| 固体部分溶解,溶液为蓝色. | 假设②成立. | |
| 固体部分溶解,有气泡产生,溶液为无色. | 假设③成立. |
【查阅资料二】该小组同学通过查阅资料,获得以下几组反应信息.
| 实验组别 | I | II | III | IV | V |
| 药 品 | Al | Fe | Ag | Al | Cu |
| CuO | CuO | CuO | Fe2O3 | Fe2O3 | |
| 相同条件下是否反应 | 是 | 是 | 否 | 是 | 否 |
4.牙膏是一种日用必需品.某研究性学习小组对某一品牌牙膏中所含摩擦剂的成分进行了如下探究.
【查阅资料】
(1)牙膏常用氢氧化铝、碳酸钙、二氧化硅等物质作摩擦剂,牙膏中其它成分遇到盐酸时无气体生成;
(2)氢氧化铝是两性氢氧化物,在常温下它既能与强酸,又能与强碱反应.如与氢氧化钠可发生如下反应:Al(OH)3+NaOH=NaAlO2+2H2O.(NaAlO2溶于水)
【提出问题】该品牌牙膏的酸碱性如何?其中含有什么摩擦剂?
【实验与猜想】
(1)取少量牙膏膏体于小烧杯中,加入10毫升蒸馏水,充分搅拌,静置一段时间,分离上层清液和沉淀,待用;
(2)用pH试纸测定所得溶液的pH大于7,正确的操作方法是:在白瓷板或玻璃片上放一小片pH试纸,利用干燥、洁净的玻璃棒蘸取溶液,粘在pH试纸上,把试纸显示的颜色与标准比色卡对照,读出溶液的pH.
(3)取少量沉淀物加入过量的稀盐酸,沉淀物全部溶解并有大量气泡产生,同时得到澄清溶液A,则该品牌牙膏中一定含有碳酸钙,一定不含有二氧化硅.
(4)进行猜想:摩擦剂成分可能是
a.只含碳酸钙 b.含有碳酸钙和氢氧化铝
【设计实验】
【实验结论】该品牌牙膏所含摩擦剂的成分为碳酸钙和氢氧化铝.
0 150258 150266 150272 150276 150282 150284 150288 150294 150296 150302 150308 150312 150314 150318 150324 150326 150332 150336 150338 150342 150344 150348 150350 150352 150353 150354 150356 150357 150358 150360 150362 150366 150368 150372 150374 150378 150384 150386 150392 150396 150398 150402 150408 150414 150416 150422 150426 150428 150434 150438 150444 150452 211419
【查阅资料】
(1)牙膏常用氢氧化铝、碳酸钙、二氧化硅等物质作摩擦剂,牙膏中其它成分遇到盐酸时无气体生成;
(2)氢氧化铝是两性氢氧化物,在常温下它既能与强酸,又能与强碱反应.如与氢氧化钠可发生如下反应:Al(OH)3+NaOH=NaAlO2+2H2O.(NaAlO2溶于水)
【提出问题】该品牌牙膏的酸碱性如何?其中含有什么摩擦剂?
【实验与猜想】
(1)取少量牙膏膏体于小烧杯中,加入10毫升蒸馏水,充分搅拌,静置一段时间,分离上层清液和沉淀,待用;
(2)用pH试纸测定所得溶液的pH大于7,正确的操作方法是:在白瓷板或玻璃片上放一小片pH试纸,利用干燥、洁净的玻璃棒蘸取溶液,粘在pH试纸上,把试纸显示的颜色与标准比色卡对照,读出溶液的pH.
(3)取少量沉淀物加入过量的稀盐酸,沉淀物全部溶解并有大量气泡产生,同时得到澄清溶液A,则该品牌牙膏中一定含有碳酸钙,一定不含有二氧化硅.
(4)进行猜想:摩擦剂成分可能是
a.只含碳酸钙 b.含有碳酸钙和氢氧化铝
【设计实验】
| 实验步骤 | 实验现象 | 解释与结论 |
| 取澄清溶液A逐滴滴入一定量氢氧化钠溶液 | 开始无明显现象,后产生白色沉淀 | 原因是NaOH+HCl═NaCl+H2O,AlCl3+3NaOH=Al(OH)3↓+3NaCl. (用化学方程式表示) |
| 继续滴入氢氧化钠溶液直至过量 | 白色沉淀溶解 | 摩擦剂中还含有氢氧化铝 |