2.在高温下,铁与水蒸气能发生反应生成一种常见铁的氧化物和一种气体,某化学 学习小组的同学对此反应甩感兴趣,在小组集体协作下设计了如下实验,以探究铁粉与水蒸气反应后的产物,也邀请你一起来完成下列探究: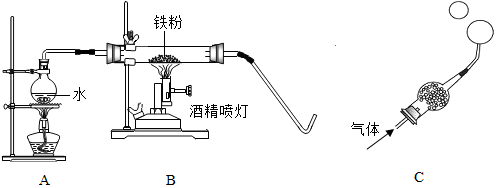
(1)A装置的作用四产生水蒸气;
(2)探究生成的气体是什么?
【猜想与假设】猜想一:生成的气体可能是氢气;
猜想二:生成的气体可能是氧气;
【实验探究】将生成的气体通入C装置,球形管里装有碱石灰干燥剂,导管口蘸些肥皂水(或洗涤剂溶液),控制气体流速,吹出肥皂泡,当肥皂泡吹到一定大时,轻轻摆动导管,肥皂泡脱离管口后,气泡上升.用燃着的木条靠近肥皂泡,有爆鸣声.
【推断】生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
【初步验证】试管中剩余固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe和Fe3O4;
猜想二:剩余固体是:Fe3O4.
【实验探究】
[实检结论]铁与水蒸气反应的化学方程式为:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.
【反思与交流】该黑色固体不可能是FeO、Fe2O3,理由是FeO、Fe2O3都不能被磁铁吸引,氧化铁是红棕色粉末.

(1)A装置的作用四产生水蒸气;
(2)探究生成的气体是什么?
【猜想与假设】猜想一:生成的气体可能是氢气;
猜想二:生成的气体可能是氧气;
【实验探究】将生成的气体通入C装置,球形管里装有碱石灰干燥剂,导管口蘸些肥皂水(或洗涤剂溶液),控制气体流速,吹出肥皂泡,当肥皂泡吹到一定大时,轻轻摆动导管,肥皂泡脱离管口后,气泡上升.用燃着的木条靠近肥皂泡,有爆鸣声.
【推断】生成的气体是氢气.
(3)探究试管中剩余固体成分是什么?
【查阅资料】
| 常见铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 颜色、状态 | 黑色粉末 | 红棕色粉末 | 黑色晶体 |
| 能否被进磁铁吸引 | 否 | 否 | 能 |
| 能否与盐酸反应 | 能 | 能 | 能 |
【猜想与假设】猜想一:剩余固体是Fe和Fe3O4;
猜想二:剩余固体是:Fe3O4.
【实验探究】
| 实验操作 | 实验现象及结论 |
【反思与交流】该黑色固体不可能是FeO、Fe2O3,理由是FeO、Fe2O3都不能被磁铁吸引,氧化铁是红棕色粉末.
20.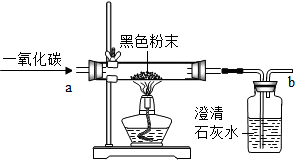 在探究课上,老师给同学们一包黑色粉末,该粉末是由铁粉和氧化铜粉末中的一种或两种组成,为了确定该粉末的成分,同学们进行如下探究,请回答下列问题:
在探究课上,老师给同学们一包黑色粉末,该粉末是由铁粉和氧化铜粉末中的一种或两种组成,为了确定该粉末的成分,同学们进行如下探究,请回答下列问题:
【猜想假设】(1)黑色粉末是铁粉
(2)黑色粉末是氧化铜粉末
(3)黑色粉末是铁粉和氧化铜粉末
【设计方案】取少量黑色粉末,放入硬质玻璃管中,通入一氧化碳气体,片刻后加热充分反应(实验装置如图所示)
请填写下表空白:(不考虑铁粉和氧化铜粉末可能发生反应)
【实验结论】经过分析实验现象,确认猜想(3)成立.
【反思评价】
(1)实验完毕后,先停止加热,继续通入一氧化碳直至玻璃管冷却至室温.继续通入一氧化碳的目的是防止生成的铜再次被氧化、澄清的石灰水倒吸入玻璃管中.
(2)从环保角度上看,上述设置有不足之处,改进措施是在b处放一只燃着的酒精灯(或安装尾气处理装置或在b处导管处绑一个小气球等).
(3)猜想(2)玻璃管中发生反应的化学方程式是CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
 在探究课上,老师给同学们一包黑色粉末,该粉末是由铁粉和氧化铜粉末中的一种或两种组成,为了确定该粉末的成分,同学们进行如下探究,请回答下列问题:
在探究课上,老师给同学们一包黑色粉末,该粉末是由铁粉和氧化铜粉末中的一种或两种组成,为了确定该粉末的成分,同学们进行如下探究,请回答下列问题:【猜想假设】(1)黑色粉末是铁粉
(2)黑色粉末是氧化铜粉末
(3)黑色粉末是铁粉和氧化铜粉末
【设计方案】取少量黑色粉末,放入硬质玻璃管中,通入一氧化碳气体,片刻后加热充分反应(实验装置如图所示)
请填写下表空白:(不考虑铁粉和氧化铜粉末可能发生反应)
| 实验中可能出现的现象 | 结论 |
| 黑色粉末不变红,澄清的石灰水不变浑浊 | 猜想(1)成立 |
| 黑色粉末全部变红,澄清的石灰水变浑浊 | 猜想(2)成立(填成立或不成立) |
| 黑色粉末部分变红,澄清的石灰水变浑浊 | 猜想(3)成立 |
【反思评价】
(1)实验完毕后,先停止加热,继续通入一氧化碳直至玻璃管冷却至室温.继续通入一氧化碳的目的是防止生成的铜再次被氧化、澄清的石灰水倒吸入玻璃管中.
(2)从环保角度上看,上述设置有不足之处,改进措施是在b处放一只燃着的酒精灯(或安装尾气处理装置或在b处导管处绑一个小气球等).
(3)猜想(2)玻璃管中发生反应的化学方程式是CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2.
19.小明和同学们做了实验室炼铁的实验.

(1)实验前应先做的是检查装置的气密性.
(2)实验中可观察到的现象是红色固体变黑,澄清的石灰水变浑浊,尾气燃烧,产生蓝色火焰.
(3)小龙认为刚通入CO时不能马上进行尾气处理,这样不安全,他的理由是装置中含有空气,此时的尾气中含有空气,点燃含有空气的一氧化碳时易发生爆炸.
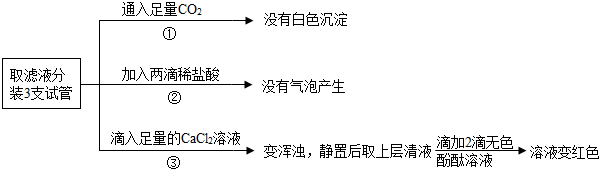
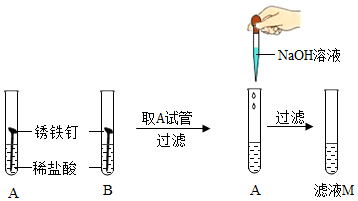
小丽用上述实验中得到的铁与过量的硫酸铜溶液反应,结果发现有部分黑色固体剩余,于是提出了疑问:
【提出问题】炼铁过程中除了生成铁以外还生成了什么?
【查阅质量】
①铁在高温条件下可与水蒸气反应生成一种铁的氧化物和氢气.
②铁和铁的氧化物中只有铁、Fe3O4能被磁铁吸引.
【猜想与假设】
①可能是FeO;
②可能是Fe2O3;
③可能是Fe3O4.
【实验探究】
(4)小丽马上排除了猜想②,理由是Fe2O3是红色粉末.
(5)写出生成该黑色固体的化学方程式3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2.

(1)实验前应先做的是检查装置的气密性.
(2)实验中可观察到的现象是红色固体变黑,澄清的石灰水变浑浊,尾气燃烧,产生蓝色火焰.
(3)小龙认为刚通入CO时不能马上进行尾气处理,这样不安全,他的理由是装置中含有空气,此时的尾气中含有空气,点燃含有空气的一氧化碳时易发生爆炸.
小丽用上述实验中得到的铁与过量的硫酸铜溶液反应,结果发现有部分黑色固体剩余,于是提出了疑问:
【提出问题】炼铁过程中除了生成铁以外还生成了什么?
【查阅质量】
①铁在高温条件下可与水蒸气反应生成一种铁的氧化物和氢气.
②铁和铁的氧化物中只有铁、Fe3O4能被磁铁吸引.
【猜想与假设】
①可能是FeO;
②可能是Fe2O3;
③可能是Fe3O4.
【实验探究】
(4)小丽马上排除了猜想②,理由是Fe2O3是红色粉末.
| 实验方案 | 现象与结论 |
| 观察到黑色粉末全部被磁铁吸引,说明猜想③正确. | |
18.关于催化剂有关问题的探究
(1)小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题.她设计并完成了如表所示的探究实验:
①请你帮小丽同学填写上表中未填完的空格.
②在小丽的探究实验中,“实验一”和“实验二”起的作用是对比(或对照等).
③小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是:比较MnO2在过氧化氢分解前后的质量.
第二方面的实验是利用“实验 三”反应后试管内的剩余物继续实验.接下来的实验操作、现象和结论是:倾倒掉反应后的液体,向剩余的固体中重新加入过氧化氢溶液,有大量气泡产生,说明MnO2仍然能加快过氧化氢的分解速率(化学性质没变).
(2)小红继续对过氧化氢分解生成水和氧气的实验条件进行探究.下表是她进行实验时采集的一组数据:
用10mL双氧水制取150mL氧气所需的时间(秒)
请你分析回答:
①小红在设计方案时,考虑了反应物的浓度、温度、催化剂等因素对过氧化氢分解速率的影响.
②通过该实验可得出的结论:
ⅰ.反应物的浓度越大,过氧化氢分解速率越快;
ⅱ.通过对比第2组和第3组实验数据可知,二氧化锰催化剂可加快分解速率.
ⅲ.温度越高,过氧化氢分解得越快.
(1)小丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题.她设计并完成了如表所示的探究实验:
| 1 | 实验操作 | 实验现象 | 实验结论或总结 | |
| 结论 | 总结 | |||
| 实验一 | 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 | 有气泡产生,木条不复燃 | 过氧化氢分解产生氧气,但是慢. | 二氧化锰是过氧化氢分解的催化剂 |
| 实验二 | 向盛水的试管中加入二氧化锰,伸入带火星的木条 | 没有明显现象 | 二氧化锰加入水中不产生氧气 | |
| 实验三 | 向盛有5mL5%过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条 | 有大量气泡产生,带火星的木条迅速复燃 | 二氧化锰能加快过氧化氢的分解 | |
②在小丽的探究实验中,“实验一”和“实验二”起的作用是对比(或对照等).
③小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明.
第一方面的实验操作中包含了两次称量,其目的是:比较MnO2在过氧化氢分解前后的质量.
第二方面的实验是利用“实验 三”反应后试管内的剩余物继续实验.接下来的实验操作、现象和结论是:倾倒掉反应后的液体,向剩余的固体中重新加入过氧化氢溶液,有大量气泡产生,说明MnO2仍然能加快过氧化氢的分解速率(化学性质没变).
(2)小红继续对过氧化氢分解生成水和氧气的实验条件进行探究.下表是她进行实验时采集的一组数据:
用10mL双氧水制取150mL氧气所需的时间(秒)
| 序号 | 双氧水的浓度 | 30% | 15% | 10% | 5% |
| 1 | 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 2 | 无催化剂、加热 | 360 | 480 | 540 | 720 |
| 3 | 二氧化锰催化剂、加热 | 10 | 25 | 60 | 120 |
①小红在设计方案时,考虑了反应物的浓度、温度、催化剂等因素对过氧化氢分解速率的影响.
②通过该实验可得出的结论:
ⅰ.反应物的浓度越大,过氧化氢分解速率越快;
ⅱ.通过对比第2组和第3组实验数据可知,二氧化锰催化剂可加快分解速率.
ⅲ.温度越高,过氧化氢分解得越快.
17.某同学做了“用过氧化氢(H2O2)溶液和二氧化锰(MnO2)制氧气”的实验后,展开了下列思考与探究:
(1)催化剂MnO2的用量对反应速率有没有影响呢?
他做了这样一组实验:每次均用30mL10%的H2O2溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
请分析表中数据回答:MnO2的用量对反应速率有没有影响呢?如果有,是怎样影响的呢?
答:有影响.在一定范围内,二氧化锰的用量越大,反应越快.
(2)H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验.记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
请分析表中数据回答:H2O2溶液的溶质质量分数对反应速率有没有影响呢?如果有,是怎样影响的呢?
答:有影响.过氧化氢溶液的溶质质量分数越大,反应越快.
由表中数据还可看出,该反应是个放热反应(填“放热”或“吸热”).
(3)还有哪些因素可能影响该反应的速率呢?
请说出你的一个猜想:二氧化锰颗粒大小(环境温度、气压、是否振荡等).
(1)催化剂MnO2的用量对反应速率有没有影响呢?
他做了这样一组实验:每次均用30mL10%的H2O2溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2用量(克) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间(秒) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
答:有影响.在一定范围内,二氧化锰的用量越大,反应越快.
(2)H2O2溶液的溶质质量分数对反应速率有没有影响呢?
他又做了一组实验:每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验.记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
| 实验次序 | H2O2溶液溶质质量分数 | MnO2粉末用量(克) | 收集540mL气体所用时间 | 反应后液体温度(℃) |
| 1 | 1% | 0.2 | 660秒 | 24 |
| 2 | 3% | 0.2 | 220秒 | 34 |
| 3 | 5% | 0.2 | 205秒 | 39 |
| 4 | 10% | 0.2 | 80秒 | 56 |
| 5 | 15% | 0.2 | 25秒 | 65 |
| 6 | 20% | 0.2 | 9秒 | 67 |
| 7 | 25% | 0.2 | 4秒 | 69 |
| 8 | 30% | 0.2 | 3秒 | 70 |
答:有影响.过氧化氢溶液的溶质质量分数越大,反应越快.
由表中数据还可看出,该反应是个放热反应(填“放热”或“吸热”).
(3)还有哪些因素可能影响该反应的速率呢?
请说出你的一个猜想:二氧化锰颗粒大小(环境温度、气压、是否振荡等).
16.某校化学活动小组准备探究气体的测定和数据处理方法.
【提出问题】如何利用石灰石与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过下列两个实验分别测定CO2的质量和体积:
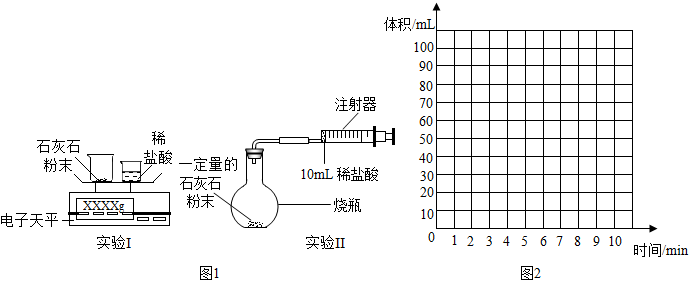
【分析与表达】
(1)上述两个实验中,反应的化学方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O.
(2)实验Ⅰ中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是最后一次加入稀盐酸,仍没有气泡产生.
(3)实验Ⅱ中,先连接好装置,在检查装置的气密性(请简述方法将注射器往右拉,松开时活塞回到之前的刻度,则气密性良好),然后装好药品,最后将10mL稀盐酸快速推入烧杯中,若稀盐酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀盐酸难以完全推入烧瓶中或仪器连接处脱落.
【记录与处理】
(4)已知实验Ⅰ反应前的总质量【m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)】,要计算生成CO2的质量,至少还需要的数据是AC
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(5)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定)
据以上实验过程和实验数据综合分析,最终生成CO2的体积是80mL
注意:若答对下面题奖励4分,但化学总分不超过60分.
(6)根据你的认识,在图2中坐标图中绘制出0~10min生成CO2体积随时间变化的曲线.
【反思与评价】
(7)经过分析,你认为实验Ⅰ的优点是巧妙利用质量守恒定律测出气体的质量,实验Ⅱ的优点是用十分简单的装置,利用前后气体体积差测得二氧化碳的体积.
【提出问题】如何利用石灰石与稀盐酸反应来测定生成CO2的质量和体积,并处理数据.
【实验设计】通过下列两个实验分别测定CO2的质量和体积:

【分析与表达】
(1)上述两个实验中,反应的化学方程式为CaCO3+2HCl═CaCl2+CO2↑+H2O.
(2)实验Ⅰ中,将小烧杯中的所有稀盐酸分几次加入到大烧杯中,并不断搅拌,判断石灰石中CaCO3完全反应的实验现象是最后一次加入稀盐酸,仍没有气泡产生.
(3)实验Ⅱ中,先连接好装置,在检查装置的气密性(请简述方法将注射器往右拉,松开时活塞回到之前的刻度,则气密性良好),然后装好药品,最后将10mL稀盐酸快速推入烧杯中,若稀盐酸是缓慢推入的,则可能造成的后果是烧瓶内气压增大,稀盐酸难以完全推入烧瓶中或仪器连接处脱落.
【记录与处理】
(4)已知实验Ⅰ反应前的总质量【m(大烧杯+石灰石粉末)+m(小烧杯+稀盐酸)】,要计算生成CO2的质量,至少还需要的数据是AC
A.m(小烧杯) B.m(大烧杯) C.m(大烧杯+反应后剩余物)
(5)实验Ⅱ的实验记录如下(表中数据在相同温度、相同压强条件下测定)
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 注射器读数/ml | 60.0 | 85.0 | 88.0 | 89.0 | 89.5 | 89.8 | 89.9 | 90.0 | 90.0 | 90.0 |
注意:若答对下面题奖励4分,但化学总分不超过60分.
(6)根据你的认识,在图2中坐标图中绘制出0~10min生成CO2体积随时间变化的曲线.
【反思与评价】
(7)经过分析,你认为实验Ⅰ的优点是巧妙利用质量守恒定律测出气体的质量,实验Ⅱ的优点是用十分简单的装置,利用前后气体体积差测得二氧化碳的体积.
15.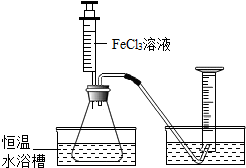 FeCl3溶液对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.
FeCl3溶液对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.
【定性探究】分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,可通过观察产生气泡的快慢来定性比较两者的反应速率.
【定量探究】为进一步判断上述实验结论的准确性,小刚同学进行了如下实验方案设计.如图所示.
【方案一】在不同过氧化氢浓度下,测定收集相同气体体积所需时间.
【方案二】在不同过氧化氢浓度下,测定相同时间收集气体体积的多少.
方案二的实验测量结果:
表中x=3,y=5.
实验结论:通过测量,若V1>V2(填“>”、“=”或“<”),说明在其他条件相同的情况下过氧化氢溶液浓度越大反应速率越快.
0 150257 150265 150271 150275 150281 150283 150287 150293 150295 150301 150307 150311 150313 150317 150323 150325 150331 150335 150337 150341 150343 150347 150349 150351 150352 150353 150355 150356 150357 150359 150361 150365 150367 150371 150373 150377 150383 150385 150391 150395 150397 150401 150407 150413 150415 150421 150425 150427 150433 150437 150443 150451 211419
 FeCl3溶液对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.
FeCl3溶液对过氧化氢的分解起催化作用,某小组拟在相同浓度FeCl3溶液的催化下,探究过氧化氢浓度对过氧化氢分解速率的影响.【定性探究】分别取相同体积、不同浓度的过氧化氢溶液于锥形瓶中,注入相同体积、相同浓度的FeCl3溶液,可通过观察产生气泡的快慢来定性比较两者的反应速率.
【定量探究】为进一步判断上述实验结论的准确性,小刚同学进行了如下实验方案设计.如图所示.
【方案一】在不同过氧化氢浓度下,测定收集相同气体体积所需时间.
【方案二】在不同过氧化氢浓度下,测定相同时间收集气体体积的多少.
方案二的实验测量结果:
| 序号 | H2O2溶液的体积/mL | H2O2溶液的浓度/% | 2%FeCl3溶液的体积/mL | 反应的时间/min | 生成O2的体积m/L |
| 1 | 10 | 30 | x | 5 | V1 |
| 2 | 10 | 15 | 3 | y | V2 |
实验结论:通过测量,若V1>V2(填“>”、“=”或“<”),说明在其他条件相同的情况下过氧化氢溶液浓度越大反应速率越快.