3.将下列符号的意义及符号中数字“2”的意义填入表中:
| 符号 | 符号的意义 | 符号中“2”的意义 |
| O2- | 氧离子 | 一个氧离子带有2个单位的负电荷 |
| 2O | 2个氧原子 | 氧原子的个数是2 |
| O2 | 氧气 | 一个氧分子中含有2个氧原子 |
| H2O | 水 | 一个水分子中含有2个氢原子 |
| 2HCl | 2个氯化氢分子 | 氯化氢分子的个数为2 |
1.在消防知识中有一个词叫做“物理性爆炸”,是指在没有发生化学反应的情况下发生的爆炸,下列各项描述中属于物理性爆炸的是( )
| A. | 煤矿中因遇到明火而发生的瓦斯爆炸 | |
| B. | 节日的烟花在空中爆炸 | |
| C. | 高压锅因排气孔堵塞而爆炸 | |
| D. | 厨房中因燃气泄漏而爆炸 |
20.下列变化中,有一种变化和其他三种变化有着本质上的不同,它是( )
| A. | 纸张燃烧 | B. | 粮食酿酒 | C. | 火药爆炸 | D. | 洗衣服晾干 |
19.碳酸氢钠和碳酸氢铵是制作油条和油饼时常用的膨松剂,化学兴趣小组对这两种膨松剂受热后的产物进行了探究:
【查阅资料】1、碱石灰是氢氧化钠固体和氧化钙的混合物,不与氨气反应.
2、碳酸氢钠溶液能与氢氧化钙或氢氧化钡溶液反应,有沉淀产生.
3、碳酸氢盐易溶于水
【进行实验】按如图所示连接好装置(夹持仪器略去).
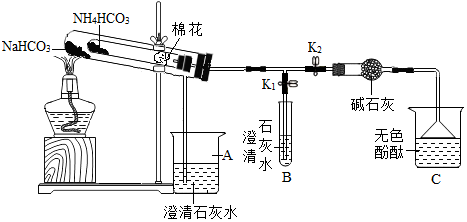
【实验反思】
(1)根据实验结果,化学兴趣小组的同学认为:与碳酸氢铵相比,碳酸氢钠更适宜作食品蓬松剂,其理由是碳酸氢铵受热分解会产生氨气,有刺激性的气味,且会污染空气.
(2)为了确定外层大试管内残留的该固体中有Na2CO3,接下来应进行实验是取少量残留固体于试管中,加入BaCl2溶液(合理即可),产生白色沉淀..
【查阅资料】1、碱石灰是氢氧化钠固体和氧化钙的混合物,不与氨气反应.
2、碳酸氢钠溶液能与氢氧化钙或氢氧化钡溶液反应,有沉淀产生.
3、碳酸氢盐易溶于水
【进行实验】按如图所示连接好装置(夹持仪器略去).

| 实验操作 | 主要实验现象 | 实验结论及解释 | |
| ① | 连接好装置,关闭K1,打开K2,微热左侧双层试管; | AC中出现气泡 | 装置的气密性良好. |
| 打开K1,关闭K2,停止加热. | A、B烧杯中的导管内均形成一段稳定的液柱. | ||
| ② | 在试管中加入两种膨松剂,打开K1,关闭K2,点燃酒精灯加热双层试管; | 内层小试管中白色固体明显减少,A、B中澄清的石灰水变浑浊. | 均有二氧化碳生成. |
| ③ | 关闭K1,打开K2; | 无色酚酞试液变红. | 碳酸氢铵分解有氨气产生. |
| ④ | 继续加热一段时间. | 内层小试管中固体消失,外层大试管中仍有固体残留. | 碳酸氢钠和碳酸氢铵的化学性质均是受热易分解. |
(1)根据实验结果,化学兴趣小组的同学认为:与碳酸氢铵相比,碳酸氢钠更适宜作食品蓬松剂,其理由是碳酸氢铵受热分解会产生氨气,有刺激性的气味,且会污染空气.
(2)为了确定外层大试管内残留的该固体中有Na2CO3,接下来应进行实验是取少量残留固体于试管中,加入BaCl2溶液(合理即可),产生白色沉淀..
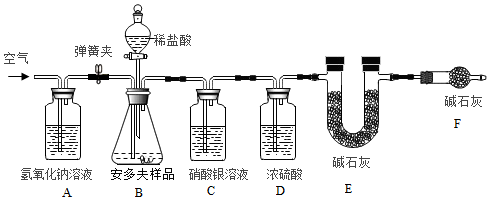
18. “双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气等.化学兴趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如图所示.同学们对这包久置的“双吸剂”固体样品很好奇,设计实验进行探究.
“双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气等.化学兴趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如图所示.同学们对这包久置的“双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置“双吸剂”固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究1】下表是小明设计的实验方案和记录的实验报告,请你补充完整.
【实验质疑】小组同学通过讨论认为实验并不能得出一定不含Fe2O3的结论,理由是:Fe2O3+6HCl═2FeCl3+3H2O、Fe+2FeCl3═3FeCl2(用化学方程式表示).
为进一步确定这包久置的“双吸剂”固体的成分迸行如下定量实验.
【实验探究2】取3g样品研碎,并用磁铁充分吸引后,得到剩余固体2.6g,按照如图流程进行实验:

(1)操作一、操作二为相同的操作,该操作为过滤;
(2)固体C的成分是CaCO3、Fe2O3(填化学式,下同);
(3)溶液A中加入碳酸钠溶液反应方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,检验所加碳酸钠溶液是否过量的方法是:静置向上层清夜中加Na2CO3溶液(或碳酸钾溶液),若无沉淀生成,则已过量;
(4)确定固体D是否洗涤干净的方法是:取最后一次洗涤液加BaCl2或CaCl2或稀盐酸或无色酚酞试液等,如无现象,则已洗净(合理即可);
(5)依据实验探究1、2中现象的分析及数据计算判断出这包久置“双吸剂”固体的成分是Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验反思】下列对实验探究1、2的反思,不正确的是D(填字母序号).
A.对物质成分的探究有时需要定性与定量实验的结合
B.实验探究2溶液B中的溶质为Na2CO3和NaOH
C.实验探究1、2中都有气体产生,但生成的气体成分不同
D.在原样品中加入足量稀盐酸有4个反应发生.
 “双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气等.化学兴趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如图所示.同学们对这包久置的“双吸剂”固体样品很好奇,设计实验进行探究.
“双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气等.化学兴趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如图所示.同学们对这包久置的“双吸剂”固体样品很好奇,设计实验进行探究.【提出问题】久置“双吸剂”固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究1】下表是小明设计的实验方案和记录的实验报告,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品放入试管中,滴加一定量的 稀盐酸,用带导管的单孔橡皮塞塞紧试管口,导管另一端伸入澄清石灰水中 | 试管中固体逐渐溶解,有大量气泡产生,得到浅绿色溶液,澄清石灰水变浑浊. | 样品中一定含有 Fe、CaCO3, 不含Fe2O3. |
| ②取少量样品放入试管中,加水,静置向上层清液中滴加无色酚酞试液 | 放出大量的热量,试管底部有不溶物,酚酞试液由无色变为红色. | 样品中含有 氧化钙或氢氧化钙或二者都有. |
为进一步确定这包久置的“双吸剂”固体的成分迸行如下定量实验.
【实验探究2】取3g样品研碎,并用磁铁充分吸引后,得到剩余固体2.6g,按照如图流程进行实验:

(1)操作一、操作二为相同的操作,该操作为过滤;
(2)固体C的成分是CaCO3、Fe2O3(填化学式,下同);
(3)溶液A中加入碳酸钠溶液反应方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,检验所加碳酸钠溶液是否过量的方法是:静置向上层清夜中加Na2CO3溶液(或碳酸钾溶液),若无沉淀生成,则已过量;
(4)确定固体D是否洗涤干净的方法是:取最后一次洗涤液加BaCl2或CaCl2或稀盐酸或无色酚酞试液等,如无现象,则已洗净(合理即可);
(5)依据实验探究1、2中现象的分析及数据计算判断出这包久置“双吸剂”固体的成分是Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验反思】下列对实验探究1、2的反思,不正确的是D(填字母序号).
A.对物质成分的探究有时需要定性与定量实验的结合
B.实验探究2溶液B中的溶质为Na2CO3和NaOH
C.实验探究1、2中都有气体产生,但生成的气体成分不同
D.在原样品中加入足量稀盐酸有4个反应发生.
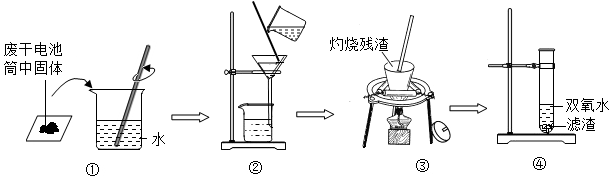
14. 小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则检验b试管中产生的气体的方法是带火星的木条.
小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则检验b试管中产生的气体的方法是带火星的木条.
小慧在做实验时误将氯化钠当成硫酸钠加入水中,结果在检验b气体时闻到一股刺激性气味.在老师的指导下小华和小慧一起就这一异常现象开展了研究.
【定性研究】
1.小慧猜想刺激性气味气体是氯化氢或氨气.小华则认为一定不是氨气,理由是根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气.在老师指导下得知:①食盐水通电时发生反应:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
②氯气是一种有刺激性气味的有毒气体.由此可推测该刺激性气味的气体是氯气.
2.为确定剩余溶液中的溶质,小慧进行如下实验,请帮她将实验报告补充完整.
小华则认为实验②不能确定一定有氯化钠,理由是①的反应中氯化铜和氢氧化钠反应,生成氯化钠和氢氧化铜,生成物中有氯化钠,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液,产生白色沉淀,所以不能证明原溶液中含有氯化钠.
【定量研究】

两位同学按如图所示的实验步骤进行实验:
(1)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取上层溶液,滴加氢氧化钠溶液,如果产生白色沉淀,说明氯化镁过量,如果没有明显现象,说明氯化镁不过量(写出实验步骤、现象和结论).
(2)计算待测液中氢氧化钠的质量分数1.6%.
(3)若步骤④中缺少洗涤干燥的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
0 150156 150164 150170 150174 150180 150182 150186 150192 150194 150200 150206 150210 150212 150216 150222 150224 150230 150234 150236 150240 150242 150246 150248 150250 150251 150252 150254 150255 150256 150258 150260 150264 150266 150270 150272 150276 150282 150284 150290 150294 150296 150300 150306 150312 150314 150320 150324 150326 150332 150336 150342 150350 211419
 小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则检验b试管中产生的气体的方法是带火星的木条.
小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则检验b试管中产生的气体的方法是带火星的木条.小慧在做实验时误将氯化钠当成硫酸钠加入水中,结果在检验b气体时闻到一股刺激性气味.在老师的指导下小华和小慧一起就这一异常现象开展了研究.
【定性研究】
1.小慧猜想刺激性气味气体是氯化氢或氨气.小华则认为一定不是氨气,理由是根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气.在老师指导下得知:①食盐水通电时发生反应:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑;
②氯气是一种有刺激性气味的有毒气体.由此可推测该刺激性气味的气体是氯气.
2.为确定剩余溶液中的溶质,小慧进行如下实验,请帮她将实验报告补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量剩余溶液,滴入氯化铜溶液. | 产生蓝色絮状沉淀 | 溶液中含有氢氧化钠 |
| ②将①中反应后混合物过滤,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液 | 产生白色沉淀 | 溶液中含有氯化钠 |
【定量研究】

两位同学按如图所示的实验步骤进行实验:
(1)步骤②加入的氯化镁溶液必需足量,其目的是使氢氧化钠完全反应.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,取上层溶液,滴加氢氧化钠溶液,如果产生白色沉淀,说明氯化镁过量,如果没有明显现象,说明氯化镁不过量(写出实验步骤、现象和结论).
(2)计算待测液中氢氧化钠的质量分数1.6%.
(3)若步骤④中缺少洗涤干燥的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
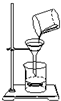 请指出如图过滤装置中的两处明显错误:
请指出如图过滤装置中的两处明显错误: