4. 酸、碱是日常生活和实验中常用的两类物质.
酸、碱是日常生活和实验中常用的两类物质.
(1)硫酸是化学实验中常备的试剂,从化工商店买回来的一般是浓硫酸,某浓硫酸标签上的部分内容如图所示.如果要配制1kg10%的稀硫酸,需要这种浓硫酸的体积约为54.3mL(结果精确到0.1mL).配制稀硫酸时,正确的操作是先将量取的900mL水倒入烧杯中,然后将量取的54.3mL浓硫酸沿着烧杯壁慢慢注入水中,并不断的用玻璃棒进行搅拌.(2)氢氧化钠是一种常见的碱,俗名苛性钠、火碱或烧碱.请写出一条氢氧化钠在工业上的用途造纸、纺织、制肥皂等.
(3)为探究“酸碱中和反应”,某班同学进行了如下实验,将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【提出问题】实验中无明显现象反应后溶液中的溶质是什么?
【做出猜想】①只有Na2SO4;②Na2SO4和H2SO4;③Na2SO4和NaOH;④Na2SO4、H2SO4和NaOH
不合理的猜想是④.
【实验探究】取烧杯中的溶液于试管中,滴加CuSO4溶液后无明显变化,则溶液中一定没有NaOH,为了验证其余猜想,同学们进行了如下三个实验方案的探究:
【结论与反思】通过探究,可确定猜想②是正确的,请指出以上实验探究中存在的两处错误pH试纸浸入溶液中,BaCl2与Na2SO4反应也会生成白色沉淀,不能证明一定有H2SO4存在.
(4)完全中和溶质质量分数为5%的氢氧化钠溶液16g,需溶质质量分数为4.9%的稀硫酸多少克?
 酸、碱是日常生活和实验中常用的两类物质.
酸、碱是日常生活和实验中常用的两类物质.(1)硫酸是化学实验中常备的试剂,从化工商店买回来的一般是浓硫酸,某浓硫酸标签上的部分内容如图所示.如果要配制1kg10%的稀硫酸,需要这种浓硫酸的体积约为54.3mL(结果精确到0.1mL).配制稀硫酸时,正确的操作是先将量取的900mL水倒入烧杯中,然后将量取的54.3mL浓硫酸沿着烧杯壁慢慢注入水中,并不断的用玻璃棒进行搅拌.(2)氢氧化钠是一种常见的碱,俗名苛性钠、火碱或烧碱.请写出一条氢氧化钠在工业上的用途造纸、纺织、制肥皂等.
(3)为探究“酸碱中和反应”,某班同学进行了如下实验,将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【提出问题】实验中无明显现象反应后溶液中的溶质是什么?
【做出猜想】①只有Na2SO4;②Na2SO4和H2SO4;③Na2SO4和NaOH;④Na2SO4、H2SO4和NaOH
不合理的猜想是④.
【实验探究】取烧杯中的溶液于试管中,滴加CuSO4溶液后无明显变化,则溶液中一定没有NaOH,为了验证其余猜想,同学们进行了如下三个实验方案的探究:
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 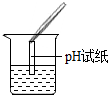 | 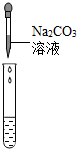 | 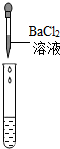 |
| 实验现象 | 试纸变色,对比标准比色卡:pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
(4)完全中和溶质质量分数为5%的氢氧化钠溶液16g,需溶质质量分数为4.9%的稀硫酸多少克?
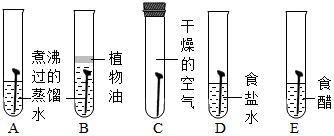
3.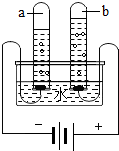 小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则b试管中产生的气体是O2(填化学式),检验这种气体的方法是带火星的木条.
小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则b试管中产生的气体是O2(填化学式),检验这种气体的方法是带火星的木条.
小慧在做实验时误将氯化钠当成硫酸钠加入水中,结果在检验b气体时闻到一股刺激性气味.在老师的指导下小华和小慧一起就这一异常现象开展了研究.
【定性研究】
1.小慧猜想刺激性气味气体是氯化氢或氨气.小华则认为一定不是氨气,理由是根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气.
在老师指导下得知:①食盐水通电时发生反应:2NaCl+2H2O═2NaOH+H2↑+Cl2↑;
②氯气是一种有刺激性气味的有毒气体.由此可推测该刺激性气味的气体是氯气.
2.定剩余溶液中的溶质,小慧进行如下实验,请帮她将实验报告补充完整.
小华则认为实验②不能确定一定有氯化钠,理由是①的反应中氯化铜和氢氧化钠反应,生成氯化钠和氢氧化铜,生成物中有氯化钠,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液,产生白色沉淀,所以不能证明原溶液中含有氯化钠.
【定量研究】
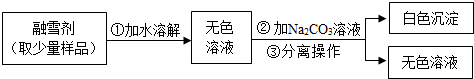
两位同学按如图所示的实验步骤进行实验:
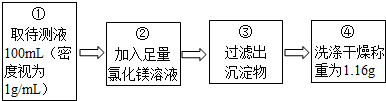
(1)步骤②加入的氯化镁溶液必需足量,其目的是.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,(写出实验步骤、现象和结论).
(2)计算待测液中氢氧化钠的质量分数(写出计算过程).
(3)若步骤④中缺少洗涤干燥的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
 小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则b试管中产生的气体是O2(填化学式),检验这种气体的方法是带火星的木条.
小华和小慧两位同学分别用如图所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体.则b试管中产生的气体是O2(填化学式),检验这种气体的方法是带火星的木条.小慧在做实验时误将氯化钠当成硫酸钠加入水中,结果在检验b气体时闻到一股刺激性气味.在老师的指导下小华和小慧一起就这一异常现象开展了研究.
【定性研究】
1.小慧猜想刺激性气味气体是氯化氢或氨气.小华则认为一定不是氨气,理由是根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气.
在老师指导下得知:①食盐水通电时发生反应:2NaCl+2H2O═2NaOH+H2↑+Cl2↑;
②氯气是一种有刺激性气味的有毒气体.由此可推测该刺激性气味的气体是氯气.
2.定剩余溶液中的溶质,小慧进行如下实验,请帮她将实验报告补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量剩余溶液,滴入氯化铜溶液. | 产生蓝色絮状沉淀 | 溶液中含有氢氧化钠 |
| ②将①中反应后混合物过滤,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液 | 产生白色沉淀 | 溶液中含有氯化钠 |
【定量研究】
两位同学按如图所示的实验步骤进行实验:

(1)步骤②加入的氯化镁溶液必需足量,其目的是.滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否足量的具体操作:静置,(写出实验步骤、现象和结论).
(2)计算待测液中氢氧化钠的质量分数(写出计算过程).
(3)若步骤④中缺少洗涤干燥的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”).
1. 酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这两类化合物进行了一系列的探究活动.
酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这两类化合物进行了一系列的探究活动.
(1)同学们打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是为什么?
(2)如图是某试剂瓶标签上的内容.要把10 g这种浓硫酸稀释为20%的硫酸,需要水的质量为39g.
稀释浓硫酸时,不可将水倒进浓硫酸里,请解释其原因.
(3)氢氧化钠暴露在空气中会变质,写出氢氧化钠变质的化学方程式:2NaOH+CO2═Na2CO3+H2O.
①取少量该固体样品置于试管中,向其中加入一种无色溶液,发现有气泡产生,说明该样品中含有碳酸钠,由此可确定该固体已发生变质.则无色溶液可能是盐酸.
②为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如表所示的实验.已知碳酸钠的水溶液呈碱性,它的存在会对氢氧化钠的检验造成干扰.请根据如图部分物质的溶解性表(20℃)所提供的信息,将如表填写完整.
(4)若73 g质量分数为20%的盐酸与127g氢氧化钠溶液恰好完全中和,试计算反应后所得溶液中溶质的质量分数.
0 150080 150088 150094 150098 150104 150106 150110 150116 150118 150124 150130 150134 150136 150140 150146 150148 150154 150158 150160 150164 150166 150170 150172 150174 150175 150176 150178 150179 150180 150182 150184 150188 150190 150194 150196 150200 150206 150208 150214 150218 150220 150224 150230 150236 150238 150244 150248 150250 150256 150260 150266 150274 211419
 酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这两类化合物进行了一系列的探究活动.
酸、碱、盐是有广泛用途的重要化合物.某化学活动小组的同学围绕这两类化合物进行了一系列的探究活动.(1)同学们打开盛浓盐酸和浓硫酸试剂瓶的瓶盖,立即就能把它们区分开来,这是为什么?
(2)如图是某试剂瓶标签上的内容.要把10 g这种浓硫酸稀释为20%的硫酸,需要水的质量为39g.
稀释浓硫酸时,不可将水倒进浓硫酸里,请解释其原因.
(3)氢氧化钠暴露在空气中会变质,写出氢氧化钠变质的化学方程式:2NaOH+CO2═Na2CO3+H2O.
①取少量该固体样品置于试管中,向其中加入一种无色溶液,发现有气泡产生,说明该样品中含有碳酸钠,由此可确定该固体已发生变质.则无色溶液可能是盐酸.
②为探究该固体中是否还有未变质的氢氧化钠,同学们又进行了如表所示的实验.已知碳酸钠的水溶液呈碱性,它的存在会对氢氧化钠的检验造成干扰.请根据如图部分物质的溶解性表(20℃)所提供的信息,将如表填写完整.
| 阳离子 | OH | N03- | C1- | SO42- | C03- |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不溶 | 不溶 |
| 实验目的 | 实验操作 | 现象 | 结论或化学方程式 |
除去碳酸钠 | 取少量该固体样品溶于水配成溶液,滴加适量的氯化钡溶液 充分反应后过滤 | 有白色沉淀生成 | 有关反应的化学方程式为 Na2CO3+BaCl2=BaCO3↓+2NaCl |
| 检验是否含有氢氧化钠 | 在滤液中滴加酚酞溶液 | 溶液变红色 | 该样品中含有氢氧化钠 |