12.下列有关溶液的说法正确的是( )
| A. | 将植物油与水混合,得到的是溶液 | |
| B. | 物质溶解时,温度一定升高 | |
| C. | 将一杯食盐溶液倒出一多半,则倒出的溶液较稀,留在杯中的溶液较浓 | |
| D. | 食盐溶液不易结冰的原因是食盐溶液的凝固点比水低 |
11.学习碳酸钠的性质之后,知道碳酸钠溶液中主要含有H2O、Na+、CO32-,能使无色酚酞试液变红.为什么碳酸钠能使无色酚酞试液变红色?某兴趣小组想进一步探究是碳酸钠溶液中哪一种粒子是无色酚酞试液变红色?
【提出猜想】猜想①:可能是H2O;猜想②:可能是Na+;猜想③:可能是CO32-.
【实验验证】
【讨论反思】
(1)如果在实验③后的溶液中加入适量的氯化钙溶液,产生的现象是产生白色沉淀,溶液由红色变成无色,反应的化学方程式是Na2CO3+CaCl2═CaCO3↓+2NaCl.
(2)碳酸钠溶液能使物色酚酞变红色的原因是碳酸钠与水反应生成了少量OH-.
【提出猜想】猜想①:可能是H2O;猜想②:可能是Na+;猜想③:可能是CO32-.
【实验验证】
| 实验操作 | 实验现象 | 结论 |
| ①用试管取少量蒸馏水,滴入1-2滴无色酚酞试液,振荡 | 试管内溶液仍无色 | 水分子不能使无色酚酞试液变红色 |
| ②用试管取少量 氯化钠溶液,滴入1-2滴无色酚酞试液,振荡 | 试管内溶液仍无色 | Na+不能使无色酚酞试液变红色 |
| ③用试管取少量碳酸钠溶液,滴入1-2滴无色酚酞试液 | 酚酞试液变红色 | CO32-能使酚酞试液变红色 |
(1)如果在实验③后的溶液中加入适量的氯化钙溶液,产生的现象是产生白色沉淀,溶液由红色变成无色,反应的化学方程式是Na2CO3+CaCl2═CaCO3↓+2NaCl.
(2)碳酸钠溶液能使物色酚酞变红色的原因是碳酸钠与水反应生成了少量OH-.
10.小明在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的实验
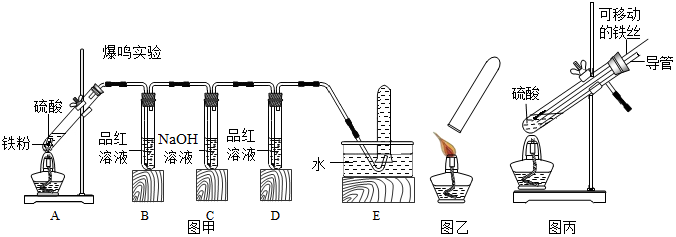
请帮助小明完成下表:
【实验结论】铁与不同浓度的硫酸反应,生成的气体产物可能不同,当硫酸溶液浓度达到足够大时,生成的气体产物中有二氧化硫.
【交流反思】(1)写出实验三中铁与硫酸溶液反应的化学方程式Fe+H2SO4═FeSO4+H2↑,
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】小明又将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液面以下的原因防止生成的气体从导管逸出
,该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸.
0 149828 149836 149842 149846 149852 149854 149858 149864 149866 149872 149878 149882 149884 149888 149894 149896 149902 149906 149908 149912 149914 149918 149920 149922 149923 149924 149926 149927 149928 149930 149932 149936 149938 149942 149944 149948 149954 149956 149962 149966 149968 149972 149978 149984 149986 149992 149996 149998 150004 150008 150014 150022 211419
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的实验

请帮助小明完成下表:
| A中硫酸的浓度 | 实验现象 | A中生成气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | ① | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | ② |
| 实验三 | 25% | ③ | 不褪色 | ④ | 只有H2 |
【交流反思】(1)写出实验三中铁与硫酸溶液反应的化学方程式Fe+H2SO4═FeSO4+H2↑,
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】小明又将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液面以下的原因防止生成的气体从导管逸出
,该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸.

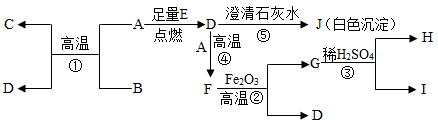

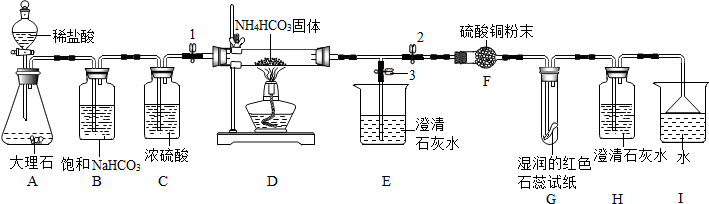

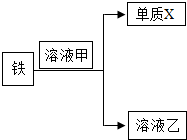 钢铁是生产、生活中使用非常广泛的金属.
钢铁是生产、生活中使用非常广泛的金属.