18.高纯氧化钙是用于电子工业重要的无机化工原料.用硝酸钙溶液制备高纯氧化钙的工艺流程如下:
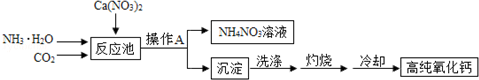
下列说法中不正确的是( )

下列说法中不正确的是( )
| A. | 反应池中的化学方程式为:CO2+2NH3•H2O+Ca(NO3)2═2NH4NO3+CaCO3↓ | |
| B. | 操作A为蒸发结晶 | |
| C. | 该工艺流程中可以循环使用的物质是CO2 | |
| D. | 冷却需在干燥的环境中进行,否则制得的高纯氧化钙中会混有杂质Ca(OH)2 |
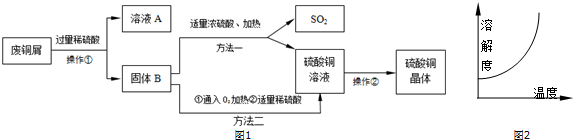
17.以硫酸钙晶体(石膏的主要成分)与氯化钾为原料制备硫酸钾的流程如图:
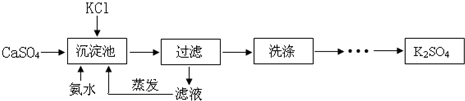
已知硫酸钾在不同温度下在水溶液、氨溶液中的溶解度(g)
(1)氨水显碱性(填“酸性”、“碱性”或“中性”),向水中连续通氨气达两个小时可得高浓度氨水,氨气不断溶解使溶液pH增大(填“增大”、“减小”或“不变”).上表中“非常压”指需增大气压才能形成30℃的氨(35%)溶液,常压下不能形成30℃的氨(35%)溶液的原因是常压30℃时氨气在水中达到饱和时浓度小于35%.
(2)沉淀池中氨水浓度常常控制在25%至40%,其原因是氨水浓度越大,硫酸钾溶解度越小,沉淀池温度适宜保持
低温(选填“低温”或“高温”).
(3)滤液经蒸发后产生可以循环使用的气体,其化学式为NH3;滤液中的副产品氯化钙可转化成碳酸钙固体,与HNO3反应制备Ca(NO3)2•6H2O晶体,为确保制备过程中既不补充水,也无多余的水,所用硝酸溶液中溶质与溶剂的质量比为7:5.
(4)实验室进行过滤操作需要的玻璃仪器有烧杯、玻璃棒、漏斗,其中玻璃棒在稀释浓硫酸时也用到,稀释浓硫酸时用到玻璃棒的主要作用为使溶解产生的热量及时散发,防止局部过热而引起液体飞溅.
(5)检验沉淀是否洗净的试剂是AB(填序号)
A.酚酞试液 B碳酸钠溶液 C氯化钡溶液
(6)烟气脱硫能有效减少二氧化硫的排放,能将其转化为石膏(CaSO4•2H2O)等产品,实现“变废为宝”.二氧化硫的排放会导致的环境问题是形成酸雨,可用高锰酸钾溶液检验烟气中二氧化硫.
(7)某电厂用煤200吨(含硫质量分数为2.5%),若燃烧时煤中的硫全部转化成二氧化硫,烟气脱硫中有96%的硫转化为石膏(CaSO4•2H2O),则可生产石膏多少吨?

已知硫酸钾在不同温度下在水溶液、氨溶液中的溶解度(g)
| 温度(℃) | 0 | 10 | 26 | 30 |
| 水溶液 | 7.31 | 9.28 | 11.03 | 12.98 |
| 氨(8%)溶液 | 1.41 | 1.58 | 2.25 | 3.36 |
| 氨(35%)溶液 | 0.44 | 0.75 | 0.82 | 非常压 |
(2)沉淀池中氨水浓度常常控制在25%至40%,其原因是氨水浓度越大,硫酸钾溶解度越小,沉淀池温度适宜保持
低温(选填“低温”或“高温”).
(3)滤液经蒸发后产生可以循环使用的气体,其化学式为NH3;滤液中的副产品氯化钙可转化成碳酸钙固体,与HNO3反应制备Ca(NO3)2•6H2O晶体,为确保制备过程中既不补充水,也无多余的水,所用硝酸溶液中溶质与溶剂的质量比为7:5.
(4)实验室进行过滤操作需要的玻璃仪器有烧杯、玻璃棒、漏斗,其中玻璃棒在稀释浓硫酸时也用到,稀释浓硫酸时用到玻璃棒的主要作用为使溶解产生的热量及时散发,防止局部过热而引起液体飞溅.
(5)检验沉淀是否洗净的试剂是AB(填序号)
A.酚酞试液 B碳酸钠溶液 C氯化钡溶液
(6)烟气脱硫能有效减少二氧化硫的排放,能将其转化为石膏(CaSO4•2H2O)等产品,实现“变废为宝”.二氧化硫的排放会导致的环境问题是形成酸雨,可用高锰酸钾溶液检验烟气中二氧化硫.
(7)某电厂用煤200吨(含硫质量分数为2.5%),若燃烧时煤中的硫全部转化成二氧化硫,烟气脱硫中有96%的硫转化为石膏(CaSO4•2H2O),则可生产石膏多少吨?
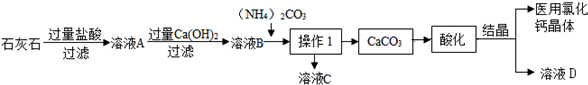
16.医用CaCl2•2H2O可用于补钙、抗过敏和消炎等,以某碳酸钙样品(其中含少量Al3+、Fe3+等杂质)生产医用CaCl2•2H2O的工艺流程为:
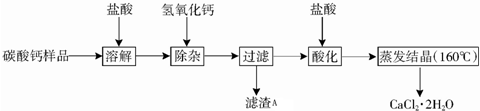
已知:查阅资料得知氢氧化物沉淀及溶解时的pH为:
(1)在实验室进行溶解时玻璃棒的作用是搅拌,加速溶解,过滤时用到的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)除杂操作是加入稍过量的氢氧化钙,调节溶液的pH使Al3+、Fe3+全部转化为沉淀,此时应该控制溶液的pH值X的范围是4.0~7.8;滤渣A的主要成分的化学式为Fe(OH)3、Al(OH)3.
(3)酸化时加盐酸的主要目的为了将氢氧化钙转化为氯化钙.
(4)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则样品中碳酸钙的质量分数最大为多少?(写出计算过程)

已知:查阅资料得知氢氧化物沉淀及溶解时的pH为:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 |
| 开始沉淀时的pH | 2.3 | 4.0 | 7.8 |
| 完全沉淀时的pH | 3.7 | 5.2 | 10.8 |
(2)除杂操作是加入稍过量的氢氧化钙,调节溶液的pH使Al3+、Fe3+全部转化为沉淀,此时应该控制溶液的pH值X的范围是4.0~7.8;滤渣A的主要成分的化学式为Fe(OH)3、Al(OH)3.
(3)酸化时加盐酸的主要目的为了将氢氧化钙转化为氯化钙.
(4)若所用碳酸钙样品12.5Kg,最后所得的产物中含氯化钙11.1Kg,则样品中碳酸钙的质量分数最大为多少?(写出计算过程)
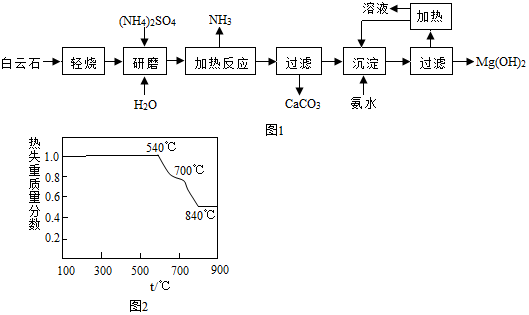
13.汽车安全气囊中装有叠氮化钠(NaN3)等固体粉末.工业上将金属钠与无水的液氨(NH3)反应得氨基钠(NaNH2),再将氨基钠与一氧化二氮反应可生成叠氮化钠、氢氧化钠和氨气.下列说法中,不正确的是( )
| A. | 安全气囊中选用叠氮化钠的原因可能是NaN3迅速分解产生大量NH3 | |
| B. | 钠可与水反应 | |
| C. | 制备叠氮化钠反应中,主要涉及的化学方程式为:Na+NH3 $\frac{\underline{\;\;△\;\;}}{\;}$NaNH2+H2↑ 2NaNH2+N2O$\frac{\underline{\;\;△\;\;}}{\;}$NaN3+NaOH+NH3↑ | |
| D. | 工业级NaN3中可能含有Na2CO3 |
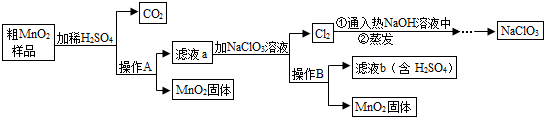
10.工业上常利石灰浆[主要成分为Ca(OH)2]制备化工原料KClO3和超细CaCO3.
Ⅰ.制备KClO3的流程如图1所示:

已知:①反应1为:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O.
②有关物质在常温下的溶解度如表:
(1)操作a的名称是过滤,在实验室中完成此操作需要的玻璃仪器有烧杯、玻璃棒、漏斗,该操作中玻璃棒的作用是引流.
(2)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和KClO3(填化学式),你认为该反应能得到KClO3晶体的原因是相同条件下,氯酸钾的溶解度最小.
(3)洗涤KClO3晶体时,可选用下列C洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如图2所示:已知:NH4Cl溶液呈酸性.
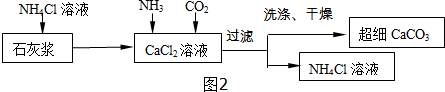
(1)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+H2O+CO2+2NH3═CaCO3↓+2NH4Cl.该流程可循环使用的物质是氯化铵溶液.
(2)检验CaCO3是否洗涤干净的方法是:取最后一次洗涤液,向其中滴加B(填写序号),观察,根据实验现象推断是否洗干净.
A.Na2CO3溶液 B.AgNO3溶液 C.酚酞试液.
0 149648 149656 149662 149666 149672 149674 149678 149684 149686 149692 149698 149702 149704 149708 149714 149716 149722 149726 149728 149732 149734 149738 149740 149742 149743 149744 149746 149747 149748 149750 149752 149756 149758 149762 149764 149768 149774 149776 149782 149786 149788 149792 149798 149804 149806 149812 149816 149818 149824 149828 149834 149842 211419
Ⅰ.制备KClO3的流程如图1所示:

已知:①反应1为:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O.
②有关物质在常温下的溶解度如表:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(2)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和KClO3(填化学式),你认为该反应能得到KClO3晶体的原因是相同条件下,氯酸钾的溶解度最小.
(3)洗涤KClO3晶体时,可选用下列C洗涤剂(填字母编号).
A.KCl饱和溶液 B.冰水 C.饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如图2所示:已知:NH4Cl溶液呈酸性.

(1)向CaCl2溶液中通入两种气体,生成超细CaCO3的化学方程式CaCl2+H2O+CO2+2NH3═CaCO3↓+2NH4Cl.该流程可循环使用的物质是氯化铵溶液.
(2)检验CaCO3是否洗涤干净的方法是:取最后一次洗涤液,向其中滴加B(填写序号),观察,根据实验现象推断是否洗干净.
A.Na2CO3溶液 B.AgNO3溶液 C.酚酞试液.