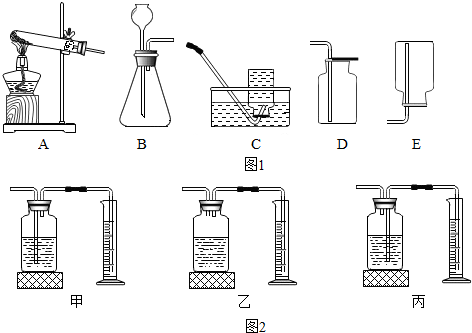
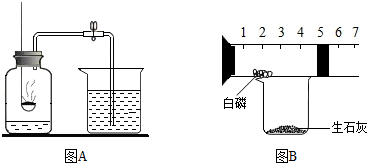
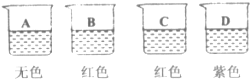
14.下列物质中属于纯净物的是( )
| A. | 某品牌纯净水 | B. | 清新的空气 | C. | 石灰水 | D. | 蒸馏水 |
13.某些金属工艺品的外观有银白色的金属光泽,同学们认为它可能和铁一样,有磁性.在讨论时,有同学提出“我们可以先拿磁铁来吸一下”.就“拿磁铁来吸一下”这一过程而言,属于科学探究环节中的( )
| A. | 建立假设 | B. | 收集证据 | C. | 实验 | D. | 做出结论 |
12.日常生活中的下列变化,属于物理变化的是( )
| A. | 香水挥发 | B. | 蜡烛燃烧 | C. | 食物腐败 | D. | 钢铁生锈 |
8.下面是四位同学对所学化学知识进行的归纳,你认为其中完全正确的是B.
| A.物质组成的差异性决定物质性质的差异性 | B.实验安全注意事项 |
| 金刚石与石墨---元素种类不同 一氧化碳与二氧化碳---分子构成不同 | 制取气体-先检查装置的气密性 点燃可燃性气体-先检验气体的纯度 |
| C.化学物质中的“三” | D.化学物质与俗名 |
| 三大化石燃料-煤、石油、天然气 三种黑色物质-氧化铜、二氧化锰、三氧化二铁 | 氧化钙-生石灰 碳酸钠-纯碱 |
6.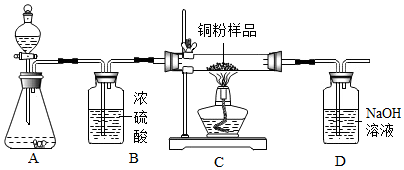 某化学兴趣小组用过氧化氢溶液(MnO2作催化剂)制取干燥的氧气,并用来测定10g某铜粉样品(含杂质碳)中铜的质量分数,实验装置如图所示.
某化学兴趣小组用过氧化氢溶液(MnO2作催化剂)制取干燥的氧气,并用来测定10g某铜粉样品(含杂质碳)中铜的质量分数,实验装置如图所示.
(1)装置B中浓硫酸的作用是吸收水蒸气.
(2)装置D中发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.小刚同学认为通过称量反应前后装置D的质量,进行计算便可求出样品中铜的质量分数.小婷同学认为小刚的方法有缺陷,原因是空气中含有的二氧化碳会进入D中被氢氧化钠溶液吸收,通过讨论,认为如果要用小刚同学的方法准确求出铜的质量分数,则应该在装置D之后连接一个装有碱石灰的干燥管消除影响.
(3)实验完毕,小聪同学误将用剩的H2O2溶液和装置C中的剩余固体仪器倒入烧杯中,发现有大量的气泡产生,经检验确认产生的气体是氧气.小明和小红两位同学对此颇感兴趣,进而展开了他们的探究之旅.
【提出问题】是粉末中的哪种物质加快了H2O2的分解速率?
【大胆猜想】猜想Ⅰ:剩余固体中的氧化剂加快了H2O2的分解速率;
猜想Ⅱ:剩余固体中的铜粉加快了H2O2的分解速率;
【实验设计】
【烦死拓展】同学们讨论后认为,上述实验还不能够确切地说明氧化铜就是过氧化氢分解制取氧气的催化剂,理由是不能确定反应前后氧化铜的质量和化学性质是否改变.
 某化学兴趣小组用过氧化氢溶液(MnO2作催化剂)制取干燥的氧气,并用来测定10g某铜粉样品(含杂质碳)中铜的质量分数,实验装置如图所示.
某化学兴趣小组用过氧化氢溶液(MnO2作催化剂)制取干燥的氧气,并用来测定10g某铜粉样品(含杂质碳)中铜的质量分数,实验装置如图所示.(1)装置B中浓硫酸的作用是吸收水蒸气.
(2)装置D中发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.小刚同学认为通过称量反应前后装置D的质量,进行计算便可求出样品中铜的质量分数.小婷同学认为小刚的方法有缺陷,原因是空气中含有的二氧化碳会进入D中被氢氧化钠溶液吸收,通过讨论,认为如果要用小刚同学的方法准确求出铜的质量分数,则应该在装置D之后连接一个装有碱石灰的干燥管消除影响.
(3)实验完毕,小聪同学误将用剩的H2O2溶液和装置C中的剩余固体仪器倒入烧杯中,发现有大量的气泡产生,经检验确认产生的气体是氧气.小明和小红两位同学对此颇感兴趣,进而展开了他们的探究之旅.
【提出问题】是粉末中的哪种物质加快了H2O2的分解速率?
【大胆猜想】猜想Ⅰ:剩余固体中的氧化剂加快了H2O2的分解速率;
猜想Ⅱ:剩余固体中的铜粉加快了H2O2的分解速率;
【实验设计】
| 实验操作 | 实验现象 | 分析及结论 |
| 实验一:将带火星的木条伸入盛有5mL5%H2O2溶液的试管 | 带火星的木条不能复燃 | H2O2溶液常温下产生氧气的量很少,不足以使带火星的木条复燃 |
| 实验二:向盛有5mL5%H2O2溶液的试管中加入1g氧化铜固体,将一根带火星的木条伸入试管 | 产生大量气泡,带火星的木条复燃 | 氧化铜能够加快过氧化氢的分解速率 |
| 实验三: 向盛有5mL5%H2O2溶液的试管中加入1g铜粉,将一根带火星的木条伸入试管 | 带火星的木条不能复燃 | 猜想Ⅱ不成立 |
5.在浓硫酸的催化作用下,固体草酸(H2C2O4)受热分解生成碳的氧化物和水.某课外兴趣小组对生成物中碳的氧化物种类等问题进行了如下探究:
【提示】①CO2+2NaOH═Na2CO3+H2O;②NaOH易溶于水;③浓硫酸能吸水.
【提出问题】生成物中有哪几种碳的氧化物?
【设计实验】兴趣小组同学设计了如下实验:

【实验探究】
(1)观察到A装置(填字母)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.该装置中发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
(2)观察到:①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;
②E装置中出现红色粉末变成黑色的现象.上述现象都能分别证明草酸分解的气体中含有CO.其中E装置中发生反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
【实验结论】猜测3成立.
0 149640 149648 149654 149658 149664 149666 149670 149676 149678 149684 149690 149694 149696 149700 149706 149708 149714 149718 149720 149724 149726 149730 149732 149734 149735 149736 149738 149739 149740 149742 149744 149748 149750 149754 149756 149760 149766 149768 149774 149778 149780 149784 149790 149796 149798 149804 149808 149810 149816 149820 149826 149834 211419
【提示】①CO2+2NaOH═Na2CO3+H2O;②NaOH易溶于水;③浓硫酸能吸水.
【提出问题】生成物中有哪几种碳的氧化物?
| 猜想1 | 猜想2 | 猜想3 |
| 只有CO | 只有CO2 | CO和CO2 |

【实验探究】
(1)观察到A装置(填字母)中的澄清石灰水变浑浊,证明草酸分解有CO2气体生成.该装置中发生反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
(2)观察到:①C装置中澄清石灰水不变浑浊,F装置中澄清石灰水变浑浊;
②E装置中出现红色粉末变成黑色的现象.上述现象都能分别证明草酸分解的气体中含有CO.其中E装置中发生反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
【实验结论】猜测3成立.