6. 某氮肥硫酸铵中混有硫酸氢氨.为测定该氮肥的含氮量,一化学研究性学习小组一定量氮肥样品,研磨使其混合均匀,备用.已知:
某氮肥硫酸铵中混有硫酸氢氨.为测定该氮肥的含氮量,一化学研究性学习小组一定量氮肥样品,研磨使其混合均匀,备用.已知:
a.氢氧化钠少量时:2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+2H2O
b.氢氧化钠过量时:NH4HSO4+2NaOH=Na2SO4+NH3↑+2H2O
c.四氯化碳是一种不溶于水和酸的有机溶剂,密度大于硫酸,氨气不溶于有四氯化碳.
d.碱石灰是氢氧化钠和氢氧化钙的固体混合物.
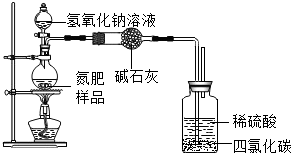
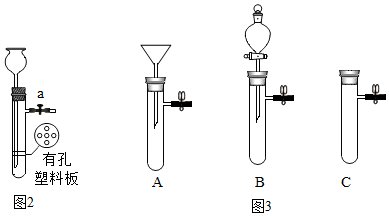
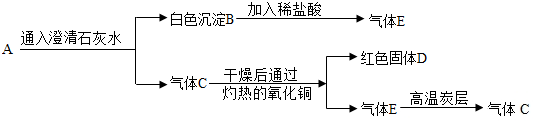
(1)同学们设计的实验装置如图所示,请回答相关问题.
①装置中碱石灰的作用是干燥氨气.
②广口瓶内四氯化碳的作用是防止液体倒吸.若不用四氯化碳只用稀硫酸吸收,装置可以如何改进导管最下端加倒置的漏斗.
③指导老师指出,用该装置进行实验,即使氢氧化钠足量且实验过程中无氨气外泄,测得的样品含氮量仍将偏低,其原因可能是残留在发生装置里的氨气没有被稀硫酸吸收.
(2)同学们改进实验装置后(改进装置图略),进行如下实验.称取不同质量的上述样品分别与40g相同浓度的氢氧化钠溶液相混合,完全溶解后,加热充分反应(此温度下铵盐不分解),并使生成的氨气全部被稀硫酸吸收,测得氨气的质量.部分实验数据如下:
请计算:样品中的氮元素的质量分数是19.87%.
 某氮肥硫酸铵中混有硫酸氢氨.为测定该氮肥的含氮量,一化学研究性学习小组一定量氮肥样品,研磨使其混合均匀,备用.已知:
某氮肥硫酸铵中混有硫酸氢氨.为测定该氮肥的含氮量,一化学研究性学习小组一定量氮肥样品,研磨使其混合均匀,备用.已知:a.氢氧化钠少量时:2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+2H2O
b.氢氧化钠过量时:NH4HSO4+2NaOH=Na2SO4+NH3↑+2H2O
c.四氯化碳是一种不溶于水和酸的有机溶剂,密度大于硫酸,氨气不溶于有四氯化碳.
d.碱石灰是氢氧化钠和氢氧化钙的固体混合物.
(1)同学们设计的实验装置如图所示,请回答相关问题.
①装置中碱石灰的作用是干燥氨气.
②广口瓶内四氯化碳的作用是防止液体倒吸.若不用四氯化碳只用稀硫酸吸收,装置可以如何改进导管最下端加倒置的漏斗.
③指导老师指出,用该装置进行实验,即使氢氧化钠足量且实验过程中无氨气外泄,测得的样品含氮量仍将偏低,其原因可能是残留在发生装置里的氨气没有被稀硫酸吸收.
(2)同学们改进实验装置后(改进装置图略),进行如下实验.称取不同质量的上述样品分别与40g相同浓度的氢氧化钠溶液相混合,完全溶解后,加热充分反应(此温度下铵盐不分解),并使生成的氨气全部被稀硫酸吸收,测得氨气的质量.部分实验数据如下:
| 氢氧化钠溶液体积/mL | 40.00 | ||
| 样品质量/g | 7.750 | 15.50 | 23.25 |
| 氨气质量/g | 1.870 | 1.870 | 1.700 |
4.如图为某化工企业生产流程示意图,下列说法正确的是( )
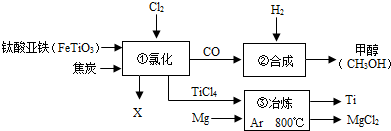

| A. | ③中氩气(Ar)作反应物 | |
| B. | 钛酸亚铁是铁和钛的合金 | |
| C. | ②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为7:1 | |
| D. | ①中反应为:2FeTiO3+6C+7Cl2$\frac{\underline{\;一定条件\;}}{\;}$2X+2TiCl4+6CO,则X为FeCl2 |
3.下列操作会引起所配制的食盐溶液溶质质量分数偏低的是( )
| A. | 用托盘天平称量6.2 g食盐固体,误将砝码放在左盘并使用游码 | |
| B. | 称量时,两盘分别垫上大小质量相同的纸 | |
| C. | 用量筒量水时,俯视凹液面的最低处读数 | |
| D. | 将配好的溶液转移到试剂瓶时,不慎洒出 |
2.某实验小组的同学在实验室进行中和反应实验时,将稀盐酸滴入到盛有氢氧化钡溶液的烧杯中,发现无明显变化,对于烧杯中溶液中溶质的成分,小组同学提出不同的意见:
【提出猜想】
猜想1:HCl和BaCl2
猜想2:HCl、Ba(OH)2和BaCl2
猜想3:只有BaCl2
你的猜想是Ba(OH)2和BaCl2(填化学式)
上述猜想中,你认为不合理的猜想是猜想2;原因是2HCl+Ba(OH)2=BaCl2+2H2O(用化学方程式表示).
【查阅资料】BaCl2溶液呈中性
【实验设计】依据上述猜想,实验小组同学分别设计了如表方案.
【实验反思】
(1)小王同学提出,上述实验过程中步骤a所得出的结论不正确,原因是稀盐酸显酸性,不能使酚酞试液变色.
(2)为了证明你的猜想是否正确,除了使用酸碱指示剂外,请再设计一个实验方案:
除了以上使用的试剂外,你还可以采用两种不同类别的试剂或方法是利用二氧化碳,方法是:取少量烧杯内的溶液于试管中,通入二氧化碳气体,不产生沉淀,溶液中不含有氢氧化钡;
利用pH试纸,方法是:利用玻璃棒蘸取烧杯中的溶液,滴在pH试纸上,与标准比色卡对照,pH=7,溶液中不含有氢氧化钡.
0 149529 149537 149543 149547 149553 149555 149559 149565 149567 149573 149579 149583 149585 149589 149595 149597 149603 149607 149609 149613 149615 149619 149621 149623 149624 149625 149627 149628 149629 149631 149633 149637 149639 149643 149645 149649 149655 149657 149663 149667 149669 149673 149679 149685 149687 149693 149697 149699 149705 149709 149715 149723 211419
【提出猜想】
猜想1:HCl和BaCl2
猜想2:HCl、Ba(OH)2和BaCl2
猜想3:只有BaCl2
你的猜想是Ba(OH)2和BaCl2(填化学式)
上述猜想中,你认为不合理的猜想是猜想2;原因是2HCl+Ba(OH)2=BaCl2+2H2O(用化学方程式表示).
【查阅资料】BaCl2溶液呈中性
【实验设计】依据上述猜想,实验小组同学分别设计了如表方案.
| 实验步骤 | 预期实验现象 | 结论 |
| a.取少量烧杯内的溶液与试管中,滴加无色酚酞试液 | 无明显变化 | 猜想3正确 |
| b.另取少量烧杯内的溶液于试管中,滴加足量的碳酸钠溶液 | 先有气泡产生,再有白色沉淀产生. | 猜想1成立 |
(1)小王同学提出,上述实验过程中步骤a所得出的结论不正确,原因是稀盐酸显酸性,不能使酚酞试液变色.
(2)为了证明你的猜想是否正确,除了使用酸碱指示剂外,请再设计一个实验方案:
| 实验步骤 | 实验现象 |
| 取少量烧杯内的溶液于试管中,滴加适量的氯化铜溶液 | 不产生沉淀 |
利用pH试纸,方法是:利用玻璃棒蘸取烧杯中的溶液,滴在pH试纸上,与标准比色卡对照,pH=7,溶液中不含有氢氧化钡.
 :
: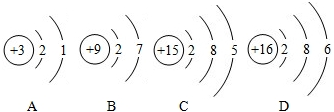
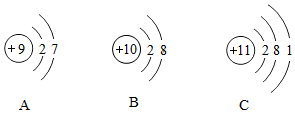
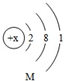
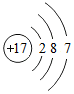 该元素原子核外有3个电子层,最外电子层上有7个电子,在化合物中可以表现的化合价为-1.下列与该元素的化学性质相似的是A(填字母编号):
该元素原子核外有3个电子层,最外电子层上有7个电子,在化合物中可以表现的化合价为-1.下列与该元素的化学性质相似的是A(填字母编号):