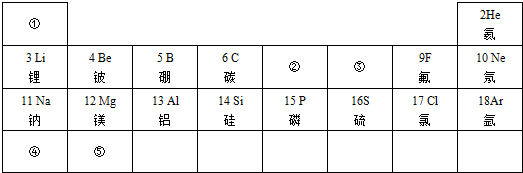
2.根据实验要求,分析作答.
(1)如图是实验室制取气体的一组装置图,按要求回答问题:
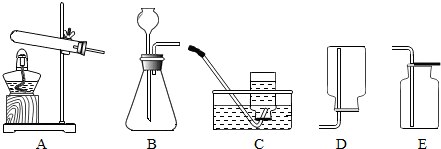
①若用装置B来制备气体,指出其中的错误:长颈漏斗下端没有伸入到锥形瓶的底部.
②H2、O2、CO2是初中常见的三种气体,实验室可选用装置B来制备的气体有H2、O2、CO2(填化学式),若制备的气体既可用装置C来收集,又可用装置D来收集,则其反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑.
③实验室常用加热氯化铵和熟石灰两种固体混合物来制取氨气,化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2.则实验室制取氨气的发生装置可选用装置A(选填字母),收集氨气只能用装置D,据此氨气具有的物理性质是易溶于水且密度比空气小.
(2)某兴趣小组为了测定葡萄糖的元素组成,取一定量的葡萄糖与氧气反应,并通过测定生成CO2和H2O的质量来确定葡萄糖中元素的组成.实验装置如图,其中CuO的作用是防止反应不完全生成CO,NaOH固体、CaCl2固体、碱石灰都是常用的干燥剂.回答下列问题:
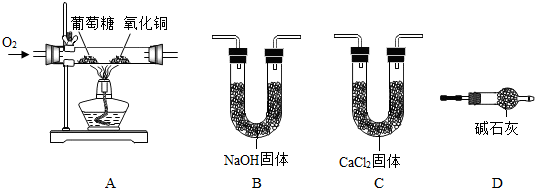
①将如图装置连接成整套实验装置,连接顺序依次为A→C→B→D(填字母).
②实验过程中数据记录如下:
反应中生成水的质量是n-mg.(用M、N或m、n表示)
③若实验不连接装置D,则测得的CO2质量偏大,原因是装置B中的氢氧化钠固体吸收了空气中的二氧化碳和水.
(1)如图是实验室制取气体的一组装置图,按要求回答问题:

①若用装置B来制备气体,指出其中的错误:长颈漏斗下端没有伸入到锥形瓶的底部.
②H2、O2、CO2是初中常见的三种气体,实验室可选用装置B来制备的气体有H2、O2、CO2(填化学式),若制备的气体既可用装置C来收集,又可用装置D来收集,则其反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑.
③实验室常用加热氯化铵和熟石灰两种固体混合物来制取氨气,化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$2NH3↑+2H2O+CaCl2.则实验室制取氨气的发生装置可选用装置A(选填字母),收集氨气只能用装置D,据此氨气具有的物理性质是易溶于水且密度比空气小.
(2)某兴趣小组为了测定葡萄糖的元素组成,取一定量的葡萄糖与氧气反应,并通过测定生成CO2和H2O的质量来确定葡萄糖中元素的组成.实验装置如图,其中CuO的作用是防止反应不完全生成CO,NaOH固体、CaCl2固体、碱石灰都是常用的干燥剂.回答下列问题:

①将如图装置连接成整套实验装置,连接顺序依次为A→C→B→D(填字母).
②实验过程中数据记录如下:
| 装置 | 反应前装置的质量/g | 反应后装置的质量/g |
| B | M | N |
| C | m | n |
③若实验不连接装置D,则测得的CO2质量偏大,原因是装置B中的氢氧化钠固体吸收了空气中的二氧化碳和水.
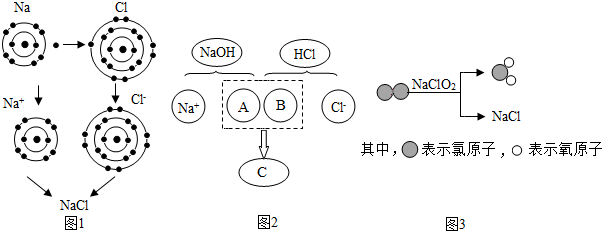
17.化学是在分子、原子、离子水平上研究物质及其变化的科学.
(1)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图所示.下列说法正确的是BE(选填字母).
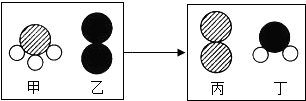
A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(2)胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异.
①Mg(OH)2起抗酸作用的微粒是OH-(填微粒符号,下同).
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.
则铝碳酸镁起抗酸作用的两种微粒是OH-;、CO32-.
(1)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图所示.下列说法正确的是BE(选填字母).

A.反应前后共有4种原子
B.该反应有单质生成
C.反应前后元素化合价都不变
D.化学变化中分子和原子均可再分
E.该化学反应中,甲、丁两种分子的个数比是2:3
(2)胃酸过多须服用抗酸药.下表为两种抗酸药的有效成分及其构成微粒:
| 抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2+、OH-、CO32- |
①Mg(OH)2起抗酸作用的微粒是OH-(填微粒符号,下同).
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑.
则铝碳酸镁起抗酸作用的两种微粒是OH-;、CO32-.
14.柠檬酸(C6H8O7)是一种工业原料,广泛应用于食品、医药等行业.下图是制备一水柠檬酸晶体(C6H8O7•H2O)的工艺流程图.回答相关问题:
【钙盐法制备】
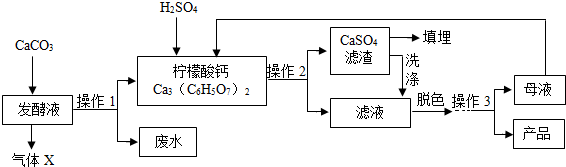
【资料卡片】
①柠檬酸水溶液显酸性.
②工业生产柠檬酸,原料预处理后,得到的发酵液中含有柠檬酸及其他可溶性杂质.
③水柠檬酸在不同温度下的溶解度如下表:
(1)实验室检验X气体的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
(2)在发酵液中加入CaCO3,同时升温至90℃,这样做的目的是使反应更充分进行.
(3)加入硫酸反应的化学方程式为3H2SO4+Ca3(C6H5O7)2=3CaSO4↓+2C6H8O7,是复分解(填基本反应类型)反应.
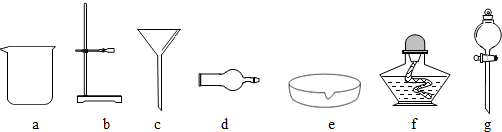
(4)操作1、2的名称是过滤,实验室完成此操作,需要用到的玻璃仪器有ac(选填字母)及玻璃棒.
(5)操作3的目的是得到一水柠檬酸晶体,操作顺序是b→c→a.
a.过滤 b.加热浓缩 c.冷却结晶 d.蒸发结晶
(6)工业生产中,可加入活性炭(填物质名称)进行脱色处理.
(7)母液可以循环使用,其中一定含有的溶质是柠檬酸(或C6H8O7).
0 149517 149525 149531 149535 149541 149543 149547 149553 149555 149561 149567 149571 149573 149577 149583 149585 149591 149595 149597 149601 149603 149607 149609 149611 149612 149613 149615 149616 149617 149619 149621 149625 149627 149631 149633 149637 149643 149645 149651 149655 149657 149661 149667 149673 149675 149681 149685 149687 149693 149697 149703 149711 211419
【钙盐法制备】

【资料卡片】
①柠檬酸水溶液显酸性.
②工业生产柠檬酸,原料预处理后,得到的发酵液中含有柠檬酸及其他可溶性杂质.
③水柠檬酸在不同温度下的溶解度如下表:
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | … |
| 溶解度/g | 96 | 118 | 146 | 183 | 216 | … |
(2)在发酵液中加入CaCO3,同时升温至90℃,这样做的目的是使反应更充分进行.
(3)加入硫酸反应的化学方程式为3H2SO4+Ca3(C6H5O7)2=3CaSO4↓+2C6H8O7,是复分解(填基本反应类型)反应.
(4)操作1、2的名称是过滤,实验室完成此操作,需要用到的玻璃仪器有ac(选填字母)及玻璃棒.

(5)操作3的目的是得到一水柠檬酸晶体,操作顺序是b→c→a.
a.过滤 b.加热浓缩 c.冷却结晶 d.蒸发结晶
(6)工业生产中,可加入活性炭(填物质名称)进行脱色处理.
(7)母液可以循环使用,其中一定含有的溶质是柠檬酸(或C6H8O7).
 如图是初中化学中常见物质间的转化关系,其中甲、乙、丙为单质;A、B、C、D、E为化合物,且A与B的组成元素相同,D与E的组成元素也相同.已知C、丙均为黑色粉末,C和E在高温条件下可生成丙和D,其余反应条件、部分反应物和生成物均已略去.试推断:
如图是初中化学中常见物质间的转化关系,其中甲、乙、丙为单质;A、B、C、D、E为化合物,且A与B的组成元素相同,D与E的组成元素也相同.已知C、丙均为黑色粉末,C和E在高温条件下可生成丙和D,其余反应条件、部分反应物和生成物均已略去.试推断:
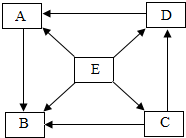 如图是一些物质的转化关系,“→”表示一种物质转化成另一种物质.其中A、B、C、D、E都含有同一种元素,且A、B、C、D属于同类别的化合物.A在生活中可用作调味品.C、D、E的水溶液能使酚酞溶液变红.部分反应物、生成物及反应条件已省略.
如图是一些物质的转化关系,“→”表示一种物质转化成另一种物质.其中A、B、C、D、E都含有同一种元素,且A、B、C、D属于同类别的化合物.A在生活中可用作调味品.C、D、E的水溶液能使酚酞溶液变红.部分反应物、生成物及反应条件已省略.