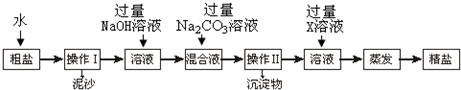
20.小明需配制100g10%的NaOH溶液来制作“叶脉书签”.在配制溶液的过程中,下列做法正确的是( )
| A. | 在托盘上垫纸并称量10gNaOH固体 | |
| B. | 称量时发现指针向右偏转,应调节砝码游码使天平平衡 | |
| C. | 用100mL的量筒量取90mL的水 | |
| D. | 把NaOH固体倒入装有90mL水的量筒中溶解 |
19.根据原子的结构示意图(如图),不能确定的是( )


| A. | 质子数 | B. | 相对原子质量 | C. | 原子序数 | D. | 元素种类 |
18.下列有关化学观念的叙述,错误的是( )
| A. | 几千万年前地球上一条恐龙体内某个原子可能在你的身体里 | |
| B. | 用刀切西瓜的过程中,个别原子被分成了更小的微粒 | |
| C. | 当自己的实验结果与多数人不同时,应查找原因、重新实验 | |
| D. | 化学不仅研究物质的组成、结构、性质和变化,还研究变化过程中伴随的能量变化 |
17.下列有关资源、能源的叙述错误的是( )
0 149052 149060 149066 149070 149076 149078 149082 149088 149090 149096 149102 149106 149108 149112 149118 149120 149126 149130 149132 149136 149138 149142 149144 149146 149147 149148 149150 149151 149152 149154 149156 149160 149162 149166 149168 149172 149178 149180 149186 149190 149192 149196 149202 149208 149210 149216 149220 149222 149228 149232 149238 149246 211419
| A. | 海洋是巨大的资源宝库,其中海洋约占地球表面的71% | |
| B. | 太阳能、风能、地热能等的利用,解决了化石能源面临耗尽的问题,并在一定程度上减少了对环境的污染 | |
| C. | 现在世界上每年因腐蚀而报废的金属设备和材料相当于年产量的20%--40% | |
| D. | 有石油的地方一定有天然气存在 |

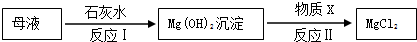
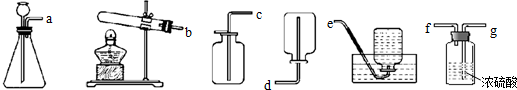
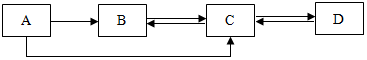 A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素.其中A为无色气体单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分.它们之间的部分转化关系如下图所示(图中反应条件及部分反应物、生成物已省略).
A、B、C、D是初中化学常见的物质,这四种物质中均含有同一种元素.其中A为无色气体单质,B、C为氧化物,且B为有毒气体,D是大理石的主要成分.它们之间的部分转化关系如下图所示(图中反应条件及部分反应物、生成物已省略).