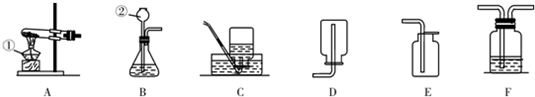
20.漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,既可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,易分解生成HCl和一种常见的单质气体.HClO具有漂白性,能使品红等有色物质褪色.
【漂白粉制取的研究】
有人提出可以利用海水(含NaCl)和石灰石为原料制取漂白粉,该方法流程如下:
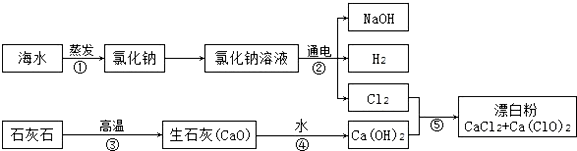
(1)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小(填“增大”或“减小”或“不变”).
(2)⑤中的反应是2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2X,X的化学式为H2O,其中Ca(ClO)2中氯元素的化合价为+1.
(3)实际工业生产中,反应⑤的反应物Ca(OH)2最好用石灰乳,(填“饱和石灰水”或“石灰乳”)并不断搅拌.
【定性研究】
有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】
【定量研究】
已知漂白粉有效成分能与浓盐酸发生如下反应Ca(ClO)2+4HCl═CaCl2+2Cl2↑+2H2O,某同学通过查阅资料,设计一个最简单的实验,测定漂白粉有效成分的质量分数.
【资料】Cl2能溶于水,但在饱和食盐水中的溶解性非常小.实验条件下Cl2的密度为3.17g/L.氯化氢气体易溶于水.
【实验探究】
(4)甲同学准确称取0.5g漂白粉样品,检查装置气密性后装入图A中,进行实验.实验结束后,量筒内收集到89.6mL食盐水.据此计算,此样品中有效成分的质量分数.(写出计算过程,结果精确到0.1%)
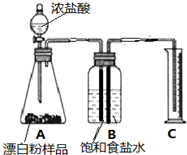
(5)在读取量筒的刻度数时,应注意①视线与凹液面最低点应齐平;②装置内气体应恢复至室温;③B、C两仪器内的液面应齐平.
(6)实验结束后,同学们发现,此装置存在着明显的不足:ABC(填序号)
A没有考虑到盐酸占据的体积对测定结果的影响.
B没有考虑到残留在导管中的液体和导管本身的体积对测定结果的影响.
C没有考虑到氯气中可能混有的二氧化碳气体对测定结果的影响
D没有考虑到氯气中可能混有的氯化氢气体对实验结果的影响.
【漂白粉制取的研究】
有人提出可以利用海水(含NaCl)和石灰石为原料制取漂白粉,该方法流程如下:

(1)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小(填“增大”或“减小”或“不变”).
(2)⑤中的反应是2Ca(OH)2+2Cl2═CaCl2+Ca(ClO)2+2X,X的化学式为H2O,其中Ca(ClO)2中氯元素的化合价为+1.
(3)实际工业生产中,反应⑤的反应物Ca(OH)2最好用石灰乳,(填“饱和石灰水”或“石灰乳”)并不断搅拌.
【定性研究】
有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 取少量样品于试管中,滴加足量的稀盐酸. | 有气体产生,气体使石灰水变浑浊. | 猜想2成立 |
| 在上述反应后的试管中加少量品红溶液. | 红色变浅或消失. |
已知漂白粉有效成分能与浓盐酸发生如下反应Ca(ClO)2+4HCl═CaCl2+2Cl2↑+2H2O,某同学通过查阅资料,设计一个最简单的实验,测定漂白粉有效成分的质量分数.
【资料】Cl2能溶于水,但在饱和食盐水中的溶解性非常小.实验条件下Cl2的密度为3.17g/L.氯化氢气体易溶于水.
【实验探究】
(4)甲同学准确称取0.5g漂白粉样品,检查装置气密性后装入图A中,进行实验.实验结束后,量筒内收集到89.6mL食盐水.据此计算,此样品中有效成分的质量分数.(写出计算过程,结果精确到0.1%)

(5)在读取量筒的刻度数时,应注意①视线与凹液面最低点应齐平;②装置内气体应恢复至室温;③B、C两仪器内的液面应齐平.
(6)实验结束后,同学们发现,此装置存在着明显的不足:ABC(填序号)
A没有考虑到盐酸占据的体积对测定结果的影响.
B没有考虑到残留在导管中的液体和导管本身的体积对测定结果的影响.
C没有考虑到氯气中可能混有的二氧化碳气体对测定结果的影响
D没有考虑到氯气中可能混有的氯化氢气体对实验结果的影响.
19.下列物质的化学式书写正确的是( )
| A. | 氧化铁:FeO | B. | 碳酸钠:NaCO3 | C. | 氢氧化钠:Na(OH) | D. | 硫酸铝:Al2(SO4)3 |
17.下列有关物质的化学式、名称、俗名不完全对应的是( )
| A. | NaCl 氯化钠 食盐 | B. | CaO 氧化钙 熟石灰 | ||
| C. | Na2CO3 碳酸钠 纯碱 | D. | NaOH 氢氧化钠 烧碱 |
16.长途运输鱼苗时,人们常在水中加入少量过氧化钙(CaO2)固体.甲、乙两位同学发现往水中投入过氧化钙时产生气泡.
(1)提出问题:当把过氧化钙投入足量水中时,最终会生成什么物质呢?
(2)进行猜想:甲同学认为:生成氧化钙和氧气;
乙同学认为:生成氢氧化钙[Ca(OH)2]和氧气.
你认为甲同学的猜想是错误的,其理由是氧化钙能与水反应生成氢氧化钙,最终产物不可能是氧化钙.
(3)设计实验:验证另一个同学的猜想是正确的,并填入下表空格中.
0 149010 149018 149024 149028 149034 149036 149040 149046 149048 149054 149060 149064 149066 149070 149076 149078 149084 149088 149090 149094 149096 149100 149102 149104 149105 149106 149108 149109 149110 149112 149114 149118 149120 149124 149126 149130 149136 149138 149144 149148 149150 149154 149160 149166 149168 149174 149178 149180 149186 149190 149196 149204 211419
(1)提出问题:当把过氧化钙投入足量水中时,最终会生成什么物质呢?
(2)进行猜想:甲同学认为:生成氧化钙和氧气;
乙同学认为:生成氢氧化钙[Ca(OH)2]和氧气.
你认为甲同学的猜想是错误的,其理由是氧化钙能与水反应生成氢氧化钙,最终产物不可能是氧化钙.
(3)设计实验:验证另一个同学的猜想是正确的,并填入下表空格中.
| 实验方法 | 实验现象 | 实验结论 |
| 取少量过氧化钙放入试管中,加足量水,将带火星的木条伸进试管中. | ①木条复燃 | 有氧气生成 |
| 取实验静置后的上层清夜,②通入二氧化碳气体. | ③出现浑浊 | ④有氢氧化钙生成 |