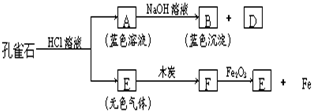
8.结合如图回答有关在实验室里制取气体的问题.
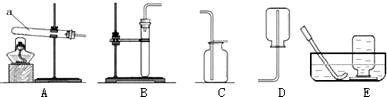
(1)仪器a的名称是试管;
(2)对实验室里制取气体进行归纳总结,填补表中空白:
(3)在实验室里用氯化铵和消石灰的混合物制取氨气时,选择的发生装置是A,由此推测,药品的状态为固体.

(1)仪器a的名称是试管;
(2)对实验室里制取气体进行归纳总结,填补表中空白:
| 制取气体 | 反应的化学方程式 | 反应物状态 | 反应条件 | 发生装置 | 气体的物理性质 | 收集装置 |
| O2 | ①2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑ | 固体 | 加热 | A | 不易溶于水密度比空气略大 | ②E(或C) |
| CO2 | CaCO3+2HCl═CaCl2+H2O+CO2↑ | 固体液体 | 常温 | ③B | 可溶于水密度比空气大 | C |
5.某化工厂用氨碱法生产的纯碱(碳酸钠)产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验:取12.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8g.
(2)该产品中碳酸钠的质量分数是否合格?(相对原子质量:Na-23 Cl-35.5 C-12 O-16 H-1要求写出计算过程,结果精确到0.1%)
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 盐酸的质量/g | 25 | 25 | 25 | 25 |
| 烧杯及所盛物质总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
(1)第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8g.
(2)该产品中碳酸钠的质量分数是否合格?(相对原子质量:Na-23 Cl-35.5 C-12 O-16 H-1要求写出计算过程,结果精确到0.1%)
1.某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用12.0g石灰石样品,把40.0g一定质量分数的稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如表:
请计算:(1)12.0g石灰石样品中碳酸钙的质量为10g,石灰石中碳酸钙的质量分数为83.3%.
(2)请你继续计算反应生成物溶液的溶质的质量分数(计算过程和结果均保留一位小数).
0 149007 149015 149021 149025 149031 149033 149037 149043 149045 149051 149057 149061 149063 149067 149073 149075 149081 149085 149087 149091 149093 149097 149099 149101 149102 149103 149105 149106 149107 149109 149111 149115 149117 149121 149123 149127 149133 149135 149141 149145 149147 149151 149157 149163 149165 149171 149175 149177 149183 149187 149193 149201 211419
| 实验次数 | 1 | 2 | 3 | 4 | 5 |
| 稀盐酸的累计加入量 | 8.0g | 16.0g | 24.0g | 32.0g | 40.0g |
| 剩余固体的质量 | 9g | 6g | 3g | 2g | 2g |
(2)请你继续计算反应生成物溶液的溶质的质量分数(计算过程和结果均保留一位小数).

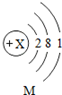 元素的单质可用于原子反应堆的导热剂,其原子结构示意图如图:
元素的单质可用于原子反应堆的导热剂,其原子结构示意图如图: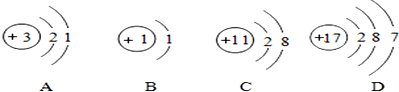
 小政同学在复习Ca(OH)2化学性质时,归纳出了Ca(OH)2与其它物质间相互反应的关系如图(图中“--”表示相连的两种物质能发生反应).
小政同学在复习Ca(OH)2化学性质时,归纳出了Ca(OH)2与其它物质间相互反应的关系如图(图中“--”表示相连的两种物质能发生反应).