10.“塑化剂”是一种工业原料,一些厂商在饮料中违法添加了“塑化剂”,对人体会造成严重危害.已知“塑化剂”的主要成分是邻苯二甲酸二辛酯,化学式为C24H38O4,有关邻苯二甲酸二辛酯说法错误的是( )
| A. | 它是一种有机物 | |
| B. | 它是由C、H、O三种元素组成 | |
| C. | 一个邻苯二甲酸二辛酯分子中共有66个原子 | |
| D. | 邻苯二甲酸二辛酯由24个碳原子、38个氢原子、4个氧原子构成 |
9.已知:X和Y两种物质共40g,在一定 条件下恰好完全反应,生成Z与W的质量比为9:11,且反应中消耗X的质量是生成Z的质量的$\frac{4}{9}$,则反应中消耗Y的质量为( )
| A. | 8g | B. | 18g | C. | 22g | D. | 32g |
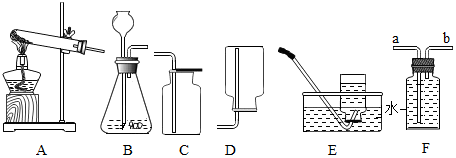
8. 用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.
用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.
已知:白磷的着火点为 40℃.
(1)H2O2稀溶液与MnO2接触时发生反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;.
(2)实验中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是温度未达着火点、未与氧气接触; 推入H2O2溶液后,观察的现象是D(填序号).
A.燃烧匙内白磷、水中白磷均燃烧 B.燃烧匙内白磷、水中白磷均不燃烧
C.燃烧匙内白磷燃烧、水中白磷不燃烧 D.燃烧匙内白磷不燃烧、水中白磷燃烧
(3)实验2中,推入H2O2溶液后,观察到硫磺燃烧得更剧烈,发出蓝紫色 火焰,由此得出氧气的性质是支持燃烧;硫磺熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶.该实验中,集气瓶内压强的变化过程是先变大后变小.
 用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.
用如图所示装置,在常温下,分别进行研究燃烧条件和研究氧气性质的实验.已知:白磷的着火点为 40℃.
| 内容 步骤 | 【实验 1】研究燃烧条件 | 【实验 2】研究氧气性质 |
Ⅰ | 烧杯中盛有 80℃的热水,分别在燃烧匙和烧杯中导管口放置一小块白磷,塞紧瓶塞 | 烧杯中盛有 NaOH 溶液,燃烧匙中放入硫磺,点燃硫后迅速将燃烧匙伸入瓶中,塞紧瓶塞 |
| Ⅱ | 推入适量H2O2溶液 | 推入适量H2O2溶液 |
(2)实验中,推入H2O2溶液前,燃烧匙和水中的白磷均不燃烧,原因分别是温度未达着火点、未与氧气接触; 推入H2O2溶液后,观察的现象是D(填序号).
A.燃烧匙内白磷、水中白磷均燃烧 B.燃烧匙内白磷、水中白磷均不燃烧
C.燃烧匙内白磷燃烧、水中白磷不燃烧 D.燃烧匙内白磷不燃烧、水中白磷燃烧
(3)实验2中,推入H2O2溶液后,观察到硫磺燃烧得更剧烈,发出蓝紫色 火焰,由此得出氧气的性质是支持燃烧;硫磺熄灭后冷却一段时间,烧杯中的部分溶液流入集气瓶.该实验中,集气瓶内压强的变化过程是先变大后变小.
6. 实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.
实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.
为确定该液体成分,同学们继续进行了如下实验探究:
 实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.
实验室中有一瓶标签受损的无色液体,如图所示.这瓶无色液体是什么呢?实验员老师告诉大家,该液体只能是过氧化氢溶液、稀硫酸.为确定该液体成分,同学们继续进行了如下实验探究:
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取该液体适量于试管中,向其中加入少 量二氧化锰粉末. | 没有气泡产生. | 该液体不是过氧化氢溶液. |
| 步骤二:取该液体适量于试管中,向其中滴加少量硝酸钡溶液. | 有白色沉淀生成 | 该液体是稀硫酸. |
4.世界是物质的,物质是变化的,化学是研究物质变化的,下列物质的变化属于化学变化的是( )
0 148784 148792 148798 148802 148808 148810 148814 148820 148822 148828 148834 148838 148840 148844 148850 148852 148858 148862 148864 148868 148870 148874 148876 148878 148879 148880 148882 148883 148884 148886 148888 148892 148894 148898 148900 148904 148910 148912 148918 148922 148924 148928 148934 148940 148942 148948 148952 148954 148960 148964 148970 148978 211419
| A. | 石油分馏出汽油、柴油等 | B. | 利用渗透膜从海水中获得淡水 | ||
| C. | 铁矿石冶炼成铁 | D. | 工业上从空气中分离出氧气 |
 如图是三种粒子的结构示意图:(注:(1)(2)用字母序号填空,(3)用元素符号和数字表示)
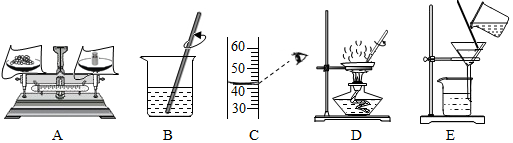
如图是三种粒子的结构示意图:(注:(1)(2)用字母序号填空,(3)用元素符号和数字表示) 砝码是化学实验室中的常用实验器材,如图所示是一盒砝码的实物图.请你回答下列问题:
砝码是化学实验室中的常用实验器材,如图所示是一盒砝码的实物图.请你回答下列问题: