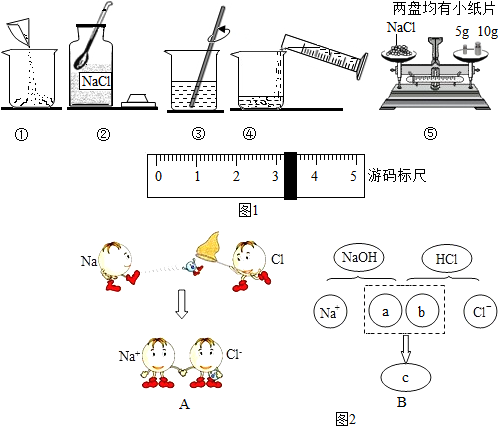
11.已知某合金粉末含有铝、铁、铜中的两种或三种,某兴趣小组在老师的指导下,对合金粉末的成分进行探究.
查阅资料:铝与氢氧化钠溶液能发生反应,化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑(NaAlO2能溶于水,溶液呈无色);该反应前后化合价升高的元素是铝,Fe、Cu不与氢氧化钠溶液反应.
(2)提出合理假设.
假设1:该合金粉末中含有铝、铁;.
假设2:该合金粉末中含有铝、钢
假设3:该合金粉末中含有铁、铜.
假设4:该合金粉末中含有铝、铁、铜.
(3)设计并完成实验方案:请填写实验操作,与表中结论相符的预期现象.限选试剂:稀盐酸、NaOH溶液、蒸馏水、AgNO3溶液.
上述实验中,反应前后溶液颜色发生变化的原因是Fe+2HCl=FeCl2+H2↑(用化学方程式表示).
查阅资料:铝与氢氧化钠溶液能发生反应,化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑(NaAlO2能溶于水,溶液呈无色);该反应前后化合价升高的元素是铝,Fe、Cu不与氢氧化钠溶液反应.
(2)提出合理假设.
假设1:该合金粉末中含有铝、铁;.
假设2:该合金粉末中含有铝、钢
假设3:该合金粉末中含有铁、铜.
假设4:该合金粉末中含有铝、铁、铜.
(3)设计并完成实验方案:请填写实验操作,与表中结论相符的预期现象.限选试剂:稀盐酸、NaOH溶液、蒸馏水、AgNO3溶液.
| 实验方案 | 预期现象 | 结论 |
| 步骤1:取一定量的合金粉末,加过量的氢氧化钠溶液 | 固体部分溶解,有气泡产生 | 合金中一定含有铝 |
| 步骤2:取少量合金粉末,加过量的稀盐酸 | 固体部分溶解,有气泡产生,溶液由无色变为浅绿色 | 假设4成立 |
10.为了探究“铁、铜、锌金属性强弱”,某学习小组设计了下列四个实验方案,其中不合理的( )
| A. | 分别将Zn和Cu加入到FeCl2溶液中 | B. | 分别将Fe和Cu加入到ZnSO4溶液中 | ||
| C. | 将Fe分别加入ZnSO4和CuSO4溶液中 | D. | 分别把Fe、Cu、Zn加入到稀盐酸中 |
9.类推是化学学习中常用的思维方法.下列类推结果正确的是( )
0 148762 148770 148776 148780 148786 148788 148792 148798 148800 148806 148812 148816 148818 148822 148828 148830 148836 148840 148842 148846 148848 148852 148854 148856 148857 148858 148860 148861 148862 148864 148866 148870 148872 148876 148878 148882 148888 148890 148896 148900 148902 148906 148912 148918 148920 148926 148930 148932 148938 148942 148948 148956 211419
| A. | 离子是带电的原子或原子团→带电的粒子就是离子 | |
| B. | 酸碱盐之间的复分解反应一定有盐生成→有盐生成的反应一定是复分解反应 | |
| C. | 点燃H2和O2的混合气体可能爆炸→点燃CH4和O2的混合气体也可能爆炸 | |
| D. | 稀有气体的原子最外电子层一般是8个电子→最外电子层是8个电子的粒子一定是稀有气体的原子 |
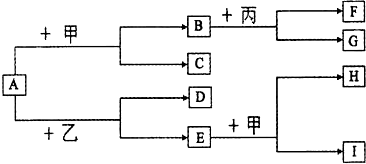
 已知AF六种物质均为初中化学常见物质,其中B、D为氧化物,A、B、E、F为不同类别的化合物,A、B、E放入水中能使酚酞变红,下图是它们之间的关系 (部分反应物和产物已省略;“→”表示转化,“”表示相互反应),请回答:
已知AF六种物质均为初中化学常见物质,其中B、D为氧化物,A、B、E、F为不同类别的化合物,A、B、E放入水中能使酚酞变红,下图是它们之间的关系 (部分反应物和产物已省略;“→”表示转化,“”表示相互反应),请回答: