6.某化学兴趣小组在实验室做了如图所示的A、B两个实验.
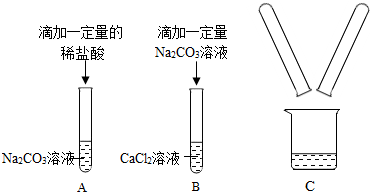
A、B两个实验结束后,小明同学将两支试管中的物质同时加入一洁净的烧杯中(如图C所示).混合后,观察到烧杯中白色沉淀明显增加,同学们将烧杯内的物质过滤,对所得滤液中溶质的成分进行探究.
【分析】A实验结束后,反应物中一定有剩余的是Na2CO3(填化学式).B实验中发生反应的化学方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl.
【猜想】小明猜想:滤液中的溶质是NaCl、Na2CO3;
小滨猜想:滤液中的溶质是NaCl、CaCl2;
小英猜想:滤液中的溶质是NaCl、CaCl2、HCl;
你的猜想:滤液中的溶质是NaCl.
【讨论】你认为小英的猜想一定不合理,请说出理由若有HCl剩余,则二者溶液混合后,白色沉淀不会增加.
【实验】若要验证小明的猜想,请完成下表的方案.

A、B两个实验结束后,小明同学将两支试管中的物质同时加入一洁净的烧杯中(如图C所示).混合后,观察到烧杯中白色沉淀明显增加,同学们将烧杯内的物质过滤,对所得滤液中溶质的成分进行探究.
【分析】A实验结束后,反应物中一定有剩余的是Na2CO3(填化学式).B实验中发生反应的化学方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl.
【猜想】小明猜想:滤液中的溶质是NaCl、Na2CO3;
小滨猜想:滤液中的溶质是NaCl、CaCl2;
小英猜想:滤液中的溶质是NaCl、CaCl2、HCl;
你的猜想:滤液中的溶质是NaCl.
【讨论】你认为小英的猜想一定不合理,请说出理由若有HCl剩余,则二者溶液混合后,白色沉淀不会增加.
【实验】若要验证小明的猜想,请完成下表的方案.
| 实验步骤 | 预想的实验现象 | 实验结论 |
| 取少量滤液于试管中,滴入稀盐酸 | 溶液中有气泡产生 | 小明的猜想正确 |
5.做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中溶质的成分进行了探究,请和他们一起探究并完成以下各空;
【提出问题】溶液中溶质的成分是什么?
【做出猜想】(1)只有Na2SO4;
(2)Na2SO4和H2SO4两种物质;
(3)Na2SO4和NaOH两种物质.
【实验验证】
丙同学对甲、乙两同学结论不同产生质疑.
【查阅资料】①Na2SO4溶液显中性;②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气,反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
【交流反思】①丙同学肯定猜想(1)不成立(填“成立”或“不成立”);
②丁同学认为猜想(2)不成立,其理由是滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸;
③该组同学经过充分讨论,一致认为猜想(3)成立;
④甲同学的实验是铝片和NaOH溶液反应.
【提出问题】溶液中溶质的成分是什么?
【做出猜想】(1)只有Na2SO4;
(2)Na2SO4和H2SO4两种物质;
(3)Na2SO4和NaOH两种物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 甲同学实验 | 取适量中和反应后的溶液滴于试管中,将表面打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出 | 猜想(2)成立 |
| 乙同学实验 | 取中和反应后的溶液少许于另一试管中,并滴加几滴无色酚酞试液 | 溶液变红色 | 猜想(3)成立 |
【查阅资料】①Na2SO4溶液显中性;②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气,反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
【交流反思】①丙同学肯定猜想(1)不成立(填“成立”或“不成立”);
②丁同学认为猜想(2)不成立,其理由是滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸;
③该组同学经过充分讨论,一致认为猜想(3)成立;
④甲同学的实验是铝片和NaOH溶液反应.
4.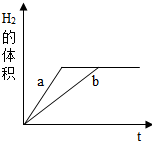 质量相等的铁和锌分别和质量相等,溶质质量分数也相等的稀盐酸反应,反应情况如图所示,则下列叙述中正确的是( )
质量相等的铁和锌分别和质量相等,溶质质量分数也相等的稀盐酸反应,反应情况如图所示,则下列叙述中正确的是( )
 质量相等的铁和锌分别和质量相等,溶质质量分数也相等的稀盐酸反应,反应情况如图所示,则下列叙述中正确的是( )
质量相等的铁和锌分别和质量相等,溶质质量分数也相等的稀盐酸反应,反应情况如图所示,则下列叙述中正确的是( )| A. | 图线a、b分别表示铁、锌的反应情况 | B. | 盐酸均反应完,一定有铁剩余 | ||
| C. | 盐酸均反应完,一定有锌剩余 | D. | 锌、铁均反应完,盐酸有剩余 |
3.下列关于空气的说法中正确的是( )
| A. | 红磷在空气中燃烧产生蓝色火焰 | |
| B. | 从空气中分离出的氮气可用作食品防腐剂 | |
| C. | SO2约占空气体积的0.03%,能产生温室效应 | |
| D. | 香肠采用真空包装的主要目的是为了隔绝水蒸气 |
20.空气中氧气含量测定的再认识.

【实验回顾】如图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的化学方程式4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】
有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计如图2实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
【交流表达】
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2.
(2)根据如表数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%).
(3)从实验原理角度分析,改进后的实验结果比前者(用红磷燃烧来测定空气中氧气含量)准确度更髙的原因是:①铁的缓慢氧化使集气瓶中的氧气消耗更彻底,使实验结果更准确;②测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.

【实验回顾】如图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的化学方程式4P+5O2 $\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】
有实验资料表明:燃烧过程中当氧气体积分数低于7%时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计如图2实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2.
(2)根据如表数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%).
(3)从实验原理角度分析,改进后的实验结果比前者(用红磷燃烧来测定空气中氧气含量)准确度更髙的原因是:①铁的缓慢氧化使集气瓶中的氧气消耗更彻底,使实验结果更准确;②测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确.
18.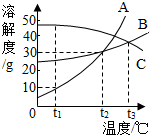 如图所示是A、B、C三种固体物质的溶解度曲线,说法正确的是( )
如图所示是A、B、C三种固体物质的溶解度曲线,说法正确的是( )
0 148527 148535 148541 148545 148551 148553 148557 148563 148565 148571 148577 148581 148583 148587 148593 148595 148601 148605 148607 148611 148613 148617 148619 148621 148622 148623 148625 148626 148627 148629 148631 148635 148637 148641 148643 148647 148653 148655 148661 148665 148667 148671 148677 148683 148685 148691 148695 148697 148703 148707 148713 148721 211419
 如图所示是A、B、C三种固体物质的溶解度曲线,说法正确的是( )
如图所示是A、B、C三种固体物质的溶解度曲线,说法正确的是( )| A. | 将接近饱和的C溶液变成饱和溶液,可采用升高温度的方法 | |
| B. | t2℃时,A、B溶液溶质的质量分数相等 | |
| C. | t2℃时,A、B的饱和溶液降温至t1℃,甲析出的固体比乙多 | |
| D. | 将t1℃时A、B、C的饱和溶液升温至t2℃,溶液中溶质的质量分数均不变 |
 某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示.
某纯碱样品中含有少量NaCl,小丽同学取该样品23g全部溶解于150g水中,再逐滴加入160g稀盐酸,反应中产生的气体的质量与盐酸的用量关系如图所示. 传统干电池在日常生活中有多方面的应用,如图显示的是干电池的内部构造,请回答下列问题:
传统干电池在日常生活中有多方面的应用,如图显示的是干电池的内部构造,请回答下列问题: