12.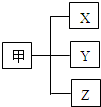 归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )
归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )
 归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )
归类是我们经常用到的一种学习方法.若用如图所示的形式对所学知识进行归类,则表中的选项与图相符的是( ) | 选项 | 甲 | X | Y | Z |
| A | 常见的碱 | 烧碱 | 纯碱 | 熟石灰 |
| B | 常见的矿物燃料 | 煤 | 石油 | 天然气 |
| C | 常见的合金 | 钢铁 | 生铁 | 氧化铁 |
| D | 常见的行星 | 地球 | 太阳 | 月球 |
| A. | A | B. | B | C. | C | D. | D |
11.受蒙古气旋和冷空气影响,2010年3月19日,我国出现了今年以来最强的一次沙尘暴天气.以下关于( )
| A. | 沙尘漂浮在空气中是由于分子运动造成的 | |
| B. | 为了防止沙尘暴的发生,应保护草原植被 | |
| C. | 出现沙尘暴时,外出要戴好口罩,以免沙尘伤害呼吸道 | |
| D. | 沙尘掉落在叶片上会使植物的光合作用减弱 |
10. 上海世博会上的“冰壶”展馆(如图)体现了芬兰的生态创新.所有的建筑材料都是在环保理念上经过精挑细选的,其中采用的纸塑复合材料属于( )
上海世博会上的“冰壶”展馆(如图)体现了芬兰的生态创新.所有的建筑材料都是在环保理念上经过精挑细选的,其中采用的纸塑复合材料属于( )
 上海世博会上的“冰壶”展馆(如图)体现了芬兰的生态创新.所有的建筑材料都是在环保理念上经过精挑细选的,其中采用的纸塑复合材料属于( )
上海世博会上的“冰壶”展馆(如图)体现了芬兰的生态创新.所有的建筑材料都是在环保理念上经过精挑细选的,其中采用的纸塑复合材料属于( )| A. | 金属材料 | B. | 无机非金属材料 | C. | 有机合成材料 | D. | 新型超导材料 |
9.2010年4月15日,科学家成功合成了第117号新元素,填补了第116号元素之间的空缺.推测该元素为117号元素的依据是( )
0 148421 148429 148435 148439 148445 148447 148451 148457 148459 148465 148471 148475 148477 148481 148487 148489 148495 148499 148501 148505 148507 148511 148513 148515 148516 148517 148519 148520 148521 148523 148525 148529 148531 148535 148537 148541 148547 148549 148555 148559 148561 148565 148571 148577 148579 148585 148589 148591 148597 148601 148607 148615 211419
| A. | 中子数 | B. | 质子数 | C. | 电子数 | D. | 中子数和质子数 |
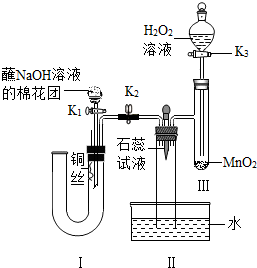 某硫酸化工厂附近居民反映:近来空气中有异味,庄稼枯黄,某学习小组对该厂附近的雨水进行检测,测得pH约为5.1,说明该区域的雨水呈酸性(填“酸性”或“碱性”或“中性”)
某硫酸化工厂附近居民反映:近来空气中有异味,庄稼枯黄,某学习小组对该厂附近的雨水进行检测,测得pH约为5.1,说明该区域的雨水呈酸性(填“酸性”或“碱性”或“中性”)