2. 如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是 )
如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是 )
 如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是 )
如图是甲、乙、丙三种物质的溶解度曲线,下列说法中正确的是 )| A. | P点表示甲、丙两种物质的饱和溶液质量相等 | |
| B. | t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液 | |
| C. | t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4 | |
| D. | 将三种物质的溶液从t2℃降至t1℃,析出晶体最多的是甲物质 |
18. 实验室有一瓶标签受到腐蚀的无色溶液,如图所示.这瓶无色溶液是放在存放盐溶液的柜子里.化学兴趣小组开展探究:
实验室有一瓶标签受到腐蚀的无色溶液,如图所示.这瓶无色溶液是放在存放盐溶液的柜子里.化学兴趣小组开展探究:
【提出问题】这瓶无色溶液究竟是什么盐的溶液?
【猜想与假设】该无色溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【初步分析】
(1)库尔班同学根据标签上的组成元素认为一定不是氯化钠溶液.
(2)艾力同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
【实验结论】
(3)该瓶无色溶液的溶质是Na2CO3(填化学式).生成白色沉淀的化学反应方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(4)玉素甫同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
(5)白燕同学经查阅资料得知:氯化钠、硫酸钠、硝酸钠溶液呈中性,碳酸钠、碳酸氢钠溶液呈碱性,提出测溶液的酸碱性来确定更简便.她采用pH试纸测量溶液的pH值>7(填>、=、<),则结论与以上同学一致.
 实验室有一瓶标签受到腐蚀的无色溶液,如图所示.这瓶无色溶液是放在存放盐溶液的柜子里.化学兴趣小组开展探究:
实验室有一瓶标签受到腐蚀的无色溶液,如图所示.这瓶无色溶液是放在存放盐溶液的柜子里.化学兴趣小组开展探究:【提出问题】这瓶无色溶液究竟是什么盐的溶液?
【猜想与假设】该无色溶液可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【初步分析】
(1)库尔班同学根据标签上的组成元素认为一定不是氯化钠溶液.
(2)艾力同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
| 实验操作 | 实验现象 |
| ①取少重该无色溶液于试管中,慢慢滴加BaCl2溶液 ②静置后,向沉淀中滴加稀盐酸 | 产生白色沉淀 产生大量气泡,沉淀全部溶解. |
(3)该瓶无色溶液的溶质是Na2CO3(填化学式).生成白色沉淀的化学反应方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(4)玉素甫同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
| 实验操作 | 实验现象 |
| 取上述无色溶液少许于试管中,滴加少量的稀盐酸 | 溶液中没有气泡产生(或有气泡产生),该瓶无色溶液是硫酸钠溶液(或碳酸钠溶液) |
14.下列是学校化学兴趣小组实验室制取二氧化碳气体的研究过程,请你参与:
(一)回顾实验室制取二氧化碳气体过程中,回答下列问题:
(1)实验室制取二氧化碳气体选用稀盐酸,而不选用浓盐酸,是因为浓盐酸具有挥发性,否则会造成制取的二氧化碳气体不纯.
(2)大理石与稀盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(二)实验室制取二氧化碳通常不选用大理石与稀硫酸反应.为此,该小组同学以影响大理石与稀硫酸反应的因素为研究课题进行探究.
【因素一】硫酸钙的溶解性对反应的影响
同学们查阅硫酸钙在不同温度下的溶解度如表一:
【因素二】硫酸的浓度对反应的影响
操作:在28℃时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm大理
石的大试管中注入硫酸,记录15分钟内生成气体的体积,见表二:
【因素三】温度对反应的影响
操作:往盛有1g直径为2mm大理石的大试管中分别加入5mL相同合适浓度、
不同温度的硫酸溶液,观察反应的情况,记录如表三:
请根据本次活动的研究目的,分析处理以上三个表中数据,得出结论:
(3)利用表一提供的数据,实验室不选用稀硫酸制取CO2的原因:反应生成的硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止.
(4)硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为25%.
(5)另取一支盛有1g直径为2mm大理石的大试管,注入40%的硫酸5mL,15分钟内生成气体的体积<(填“>”或“<”)42mL.
(6)在合适的硫酸浓度下,应选择最合适的反应温度为70℃.
(7)你认为影响该反应速率的因素还可能有碳酸钙颗粒大小,请设计实验方案验证你的猜想分别取1g块状大理石和粉末状大理石于两支试管中,分别加入5mL25%的稀硫酸,比较产生气泡快慢.
0 148412 148420 148426 148430 148436 148438 148442 148448 148450 148456 148462 148466 148468 148472 148478 148480 148486 148490 148492 148496 148498 148502 148504 148506 148507 148508 148510 148511 148512 148514 148516 148520 148522 148526 148528 148532 148538 148540 148546 148550 148552 148556 148562 148568 148570 148576 148580 148582 148588 148592 148598 148606 211419
(一)回顾实验室制取二氧化碳气体过程中,回答下列问题:
(1)实验室制取二氧化碳气体选用稀盐酸,而不选用浓盐酸,是因为浓盐酸具有挥发性,否则会造成制取的二氧化碳气体不纯.
(2)大理石与稀盐酸反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(二)实验室制取二氧化碳通常不选用大理石与稀硫酸反应.为此,该小组同学以影响大理石与稀硫酸反应的因素为研究课题进行探究.
【因素一】硫酸钙的溶解性对反应的影响
同学们查阅硫酸钙在不同温度下的溶解度如表一:
| 温度/℃ | 10 | 20 | 30 | 40 |
| 溶解度/g | 0.244 | 0.255 | 0.264 | 0.265 |
操作:在28℃时,用装有5mL硫酸溶液的注射器向盛有1g直径为2mm大理
石的大试管中注入硫酸,记录15分钟内生成气体的体积,见表二:
| 试管编号 | 1 | 2 | 3 | 4 | 5 |
| 硫酸浓度(%) | 15 | 20 | 25 | 30 | 35 |
| 气体体积/mL | 35 | 47 | 55 | 51 | 42 |
操作:往盛有1g直径为2mm大理石的大试管中分别加入5mL相同合适浓度、
不同温度的硫酸溶液,观察反应的情况,记录如表三:
| 试管编号 | A | B | C | D | E |
| 温度/℃ | 40 | 50 | 60 | 70 | 80 |
| 现象和 比较 | 有少量气泡 | 气泡比A号试管多 | 气泡明显比B号试管多 | 大量气泡产生,与常温用盐酸反应相似 | 反应非常激烈,迅速产生大量气体 |
(3)利用表一提供的数据,实验室不选用稀硫酸制取CO2的原因:反应生成的硫酸钙微溶物覆盖在固体的表面,阻碍了大理石与稀硫酸的接触,反应速率逐渐减慢甚至停止.
(4)硫酸与大理石反应,在28℃时,选用硫酸的浓度最合适为25%.
(5)另取一支盛有1g直径为2mm大理石的大试管,注入40%的硫酸5mL,15分钟内生成气体的体积<(填“>”或“<”)42mL.
(6)在合适的硫酸浓度下,应选择最合适的反应温度为70℃.
(7)你认为影响该反应速率的因素还可能有碳酸钙颗粒大小,请设计实验方案验证你的猜想分别取1g块状大理石和粉末状大理石于两支试管中,分别加入5mL25%的稀硫酸,比较产生气泡快慢.
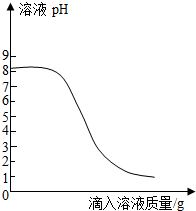 某化学兴趣小组对胃药“碳酸氢钠片”进行了探究,具体做法如下:
某化学兴趣小组对胃药“碳酸氢钠片”进行了探究,具体做法如下: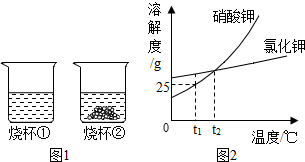 t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示.
t1℃时,将等质量的硝酸钾和氯化钾分别加入到各盛有100g水的两个烧杯中,充分搅拌后现象如图1所示,硝酸钾和氯化钾的溶解度曲线如图2所示.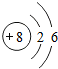 该元素的原子结构示意图如图所示.
该元素的原子结构示意图如图所示.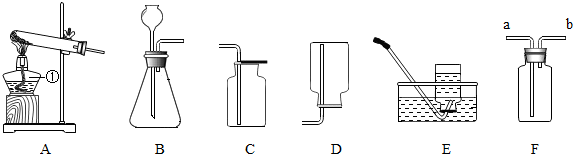

 新材料的出现促进了社会的进步,晶体硅是信息是被重要的材料.工业上生产高纯硅有以下两个重要环节;
新材料的出现促进了社会的进步,晶体硅是信息是被重要的材料.工业上生产高纯硅有以下两个重要环节;