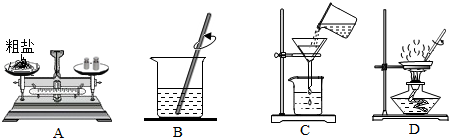
14.某兴趣小组在学习碱的化学性质时,进行了如图所示的实验.实验后,同学们将两个实验的废液倒入同一废液缸中,最终看到废液澄清并呈无色.

【提出问题】废液中含有哪些溶质?
(除指示剂外)
【交流讨论】(1)有Ca(OH)2;(2)有HCl 你的猜想:一定有NaCl、CaCl2.
【讨论】猜想1(填序号)是错误的,
理由是废液呈无色,不可能为碱性.
【验证】小刚补充以下实验来验证猜想2
小明选择了另一种不同类别的物质Zn(或Na2CO3溶液),也得到了结论.

【提出问题】废液中含有哪些溶质?
(除指示剂外)
【交流讨论】(1)有Ca(OH)2;(2)有HCl 你的猜想:一定有NaCl、CaCl2.
【讨论】猜想1(填序号)是错误的,
理由是废液呈无色,不可能为碱性.
【验证】小刚补充以下实验来验证猜想2
| 步骤 | 现象 | 结论 |
| 取少量废液,加入一定量的紫色石蕊振荡 | 紫色石蕊变为红色 | 有HCl |
10.已知木炭还原氧气铜实验中会发生如下反应:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.
某化学兴趣小组做该实验时所得产物是暗红色固体,没有观察到紫红色固体,于是他们对反应产物(假设反应物已完全反应)作如下实验探究:
信息提示:1氧化亚铜(Cu2O)为砖红色固体;
2Cu2O+H2SO4═CuSO4+Cu+H2O;
3碱石灰为氧化钙和氢氧化钠的混合物
[实验一]探究反应产物的成分
兴趣小组的同学讨论交流后,认为暗红色固体除了有铜外,还可能含有Cu2O(其中Cu的化合价是+1).为此,他们设计了以下实验:取少量暗红色固体于试管中,加入少量稀硫酸,振荡,如果观察到溶液由无色变为蓝色,说明暗红色固体中含有Cu2O.
[实验二]测定产物中Cu2O的含量
原理:Cu2O+H2$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+H2O,称取一定质量的固体产物,用下图装置进行实验(固定装置略去),通过测定反应前后装置d的质量达到实验目的.

(1)装置a中用稀硫酸而不用稀盐酸,原因是盐酸易挥发,挥发出的氯化氢能被碱石灰吸收,影响测定结果;写出装置a中反应的化学方程式:Zn+H2SO4═ZnSO4+H2↑.
(2)点燃酒精灯前,要先打开弹簧夹K1,关闭弹簧夹K2,对装置c通一会儿氢气,目的是:把装置中的空气排出去,以免加热时发生爆炸.
(3)装置b的作用是干燥氢气;装置d的质量在反应前后会发生改变,是因为它吸收了反应生成的水.
(4)反应前后,测得装置d的质量如表:
根据测得数据可行:产物中Cu2O的质量为1.44g.
(5)如果没有接上装置e,则实验得出结果将偏大(选填“偏大”、“偏小”或“不变”).
某化学兴趣小组做该实验时所得产物是暗红色固体,没有观察到紫红色固体,于是他们对反应产物(假设反应物已完全反应)作如下实验探究:
信息提示:1氧化亚铜(Cu2O)为砖红色固体;
2Cu2O+H2SO4═CuSO4+Cu+H2O;
3碱石灰为氧化钙和氢氧化钠的混合物
[实验一]探究反应产物的成分
兴趣小组的同学讨论交流后,认为暗红色固体除了有铜外,还可能含有Cu2O(其中Cu的化合价是+1).为此,他们设计了以下实验:取少量暗红色固体于试管中,加入少量稀硫酸,振荡,如果观察到溶液由无色变为蓝色,说明暗红色固体中含有Cu2O.
[实验二]测定产物中Cu2O的含量
原理:Cu2O+H2$\frac{\underline{\;\;△\;\;}}{\;}$2Cu+H2O,称取一定质量的固体产物,用下图装置进行实验(固定装置略去),通过测定反应前后装置d的质量达到实验目的.

(1)装置a中用稀硫酸而不用稀盐酸,原因是盐酸易挥发,挥发出的氯化氢能被碱石灰吸收,影响测定结果;写出装置a中反应的化学方程式:Zn+H2SO4═ZnSO4+H2↑.
(2)点燃酒精灯前,要先打开弹簧夹K1,关闭弹簧夹K2,对装置c通一会儿氢气,目的是:把装置中的空气排出去,以免加热时发生爆炸.
(3)装置b的作用是干燥氢气;装置d的质量在反应前后会发生改变,是因为它吸收了反应生成的水.
(4)反应前后,测得装置d的质量如表:
| 反应前 | 反应后 | |
| 装置d(含药品)的质量/g | 100.00 | 100.18 |
(5)如果没有接上装置e,则实验得出结果将偏大(选填“偏大”、“偏小”或“不变”).
9.实验室用蔗糖固体配制50.0g溶质质量分数为5%的蔗糖溶液(1g以下用游码),下列关于误差分析的说法正确的是( )
| A. | 溶解时,事先用蒸馏水润洗烧杯,导致溶质质量分数偏大 | |
| B. | 量取水的体积时,仰视刻度,导致溶质质量分数偏小 | |
| C. | 将配制好的溶液装入细口瓶,有少量液体溅出,导致溶质质量分数偏小 | |
| D. | 称量时,发现砝码与药品的位置放反,导致溶质质量分数偏大 |
8.“饮食健康”是人们普遍的生活追求,下列说法正确的是( )
| A. | 过量摄入油脂会使人发胖,应禁止食用油脂 | |
| B. | 海鲜产品从沿海运到衡阳过程中可以喷洒甲醛溶液防腐 | |
| C. | 在煲好的鸡汤中放入适量的加碘食盐 | |
| D. | 为了保持香肠肉质鲜美,添加过量的亚硝酸钠 |
7.下列有关溶液的说法正确的是( )
| A. | 溶液都是无色透明的液体 | |
| B. | 固体NaOH溶于水时,溶液温度升高 | |
| C. | 饱和溶液的质量分数一定比不饱和溶液的质量分数大 | |
| D. | 60℃时硝酸钾的溶解度为110g,其溶液中溶质与溶剂的质量比为11:21 |
6.水是生命之源,也是重要的溶剂,下列有关水的说法正确的是( )
| A. | 长期饮用蒸馏水有益身体健康 | |
| B. | 水电解生成氢气和氧气,说明水中含有氢分子和氧分子 | |
| C. | 将湘江水经过沉降、过滤、吸附、灭菌等净化操作后,可供人们生活用水 | |
| D. | 水体有一定的自净功能,造纸厂的污水可直接排放到湘江 |
5.以下是四种微粒的结构示意图,下列有关各微粒的说法中,错误的是( )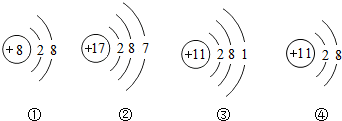
0 148368 148376 148382 148386 148392 148394 148398 148404 148406 148412 148418 148422 148424 148428 148434 148436 148442 148446 148448 148452 148454 148458 148460 148462 148463 148464 148466 148467 148468 148470 148472 148476 148478 148482 148484 148488 148494 148496 148502 148506 148508 148512 148518 148524 148526 148532 148536 148538 148544 148548 148554 148562 211419

| A. | ①④的化学性质比较稳定 | B. | ③④属于同种元素 | ||
| C. | ②容易得到电子 | D. | ④是一种阴离子 |