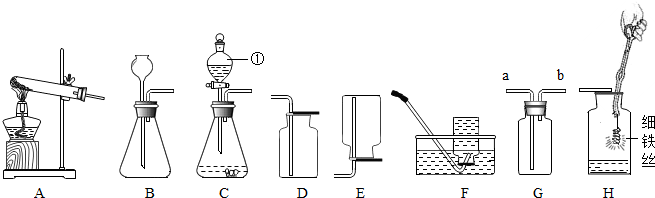
15.“垃圾是放错位置的资源”,下列垃圾分类不合理的是( )
| A. | 可回收垃圾:易拉罐 | B. | 不可回收垃圾:废报纸 | ||
| C. | 有害垃圾:废旧电池 | D. | 餐厨垃圾:剩余饭菜 |
14.现有A、B两种银白色的金属,某同学想要探究这两种金属的活动性.
【设计实验】
取大小相同的两块金属,用砂纸打磨光亮,分别放入两支试管中再加入等量的同种稀盐酸,操作与现象如表:
【思考结论】
(1)通过上述实验,判断出两种金属的活动性顺序是A<B(填“>”或“<”).
(2)假设其中的一种金属是铁,除观察到铁的表面有气泡产生外,还能观察到反应后的溶液呈浅绿色(填“浅绿色”或“黄色”)
(3)实验前用砂纸打磨金属片的目的是除去金属片表面的氧化物或污物.
(4)如果两种金属是镁和铁,还可以用镁和一种化合物的溶液来证明两者的金属活动性强弱,你认为该化合物可以是FeCl2(合理即可)(填化学式)
【设计实验】
取大小相同的两块金属,用砂纸打磨光亮,分别放入两支试管中再加入等量的同种稀盐酸,操作与现象如表:
| 实验 | 试管1 | 试管2 |
| 操作 | 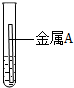 | 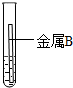 |
| 现象 | 金属表面产生气泡较慢 | 金属表面产生气泡较快 |
(1)通过上述实验,判断出两种金属的活动性顺序是A<B(填“>”或“<”).
(2)假设其中的一种金属是铁,除观察到铁的表面有气泡产生外,还能观察到反应后的溶液呈浅绿色(填“浅绿色”或“黄色”)
(3)实验前用砂纸打磨金属片的目的是除去金属片表面的氧化物或污物.
(4)如果两种金属是镁和铁,还可以用镁和一种化合物的溶液来证明两者的金属活动性强弱,你认为该化合物可以是FeCl2(合理即可)(填化学式)
12.下列化学方程式正确的是( )
| A. | KClO3$\frac{\underline{MnO_2}}{△}$KCl+O2↑ | B. | NaCl+KNO3═NaNO3+KCl | ||
| C. | 2Fe+6HCl═2FeCl3+3H2↑ | D. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O |
11.每年的6月5日是世界环境日,环境保护是我国的一项基本国策,生活中的下列做法不利于环境保护的是( )
| A. | 用布袋代替塑料袋购物 | B. | 对垃圾采取分类处理 | ||
| C. | 合理使用农药和化肥 | D. | 多使用含磷洗衣粉 |
10.某化学兴趣小组的同学在学习九年级《化学》下册中的资料卡片“石笋和钟乳石的形成”时,发现难溶于水的碳酸钙当遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙:CaCO3+CO2+H2O═Ca(HCO3)2,联想到实验室中澄清石灰水与二氧化碳反应会生成碳酸钙:Ca(OH)2+CO2═CaCO3↓+H2O,对长时间向碱溶液中通入CO2反应后溶液中的溶质组成产生了浓度的兴趣.
【提出问题】一定量CO2与NaOH溶液反应后的溶质组成是什么?
【查阅资料】(1)通入少量CO2反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O.
(2)通入过量CO2,反应的化学方程式为:Na2CO3+CO2+H2O═2NaHCO3.
(3)碳酸氢盐都是可溶于水的.BaCO3难溶于水.
(4)碳酸氢钠溶液呈碱性.
【提出猜想】(1)溶质为NaOH和Na2CO3;(2)溶质为Na2CO3;
(3)溶质为NaHCO3和Na2CO3(填化学式);(4)溶质为NaHCO3.
【设计实验】
【得出结论】猜想(3)成立.
【讨论交流】(1)有同学提出,实验步骤(1)是多余的.你认为该实验设计是否需要?不需要(填“需要”或“不需要”).
(2)同学们又一次把目光投向了教材,发现遇热或压强变小时:Ca(HCO3)2=CaCO3↓+CO2↑+H2O,纷纷提出,干粉灭火器中用NaHCO3灭火的反应原理与之相似,试写出NaHCO3受热分解的化学方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
【反思应用】(1)同学们回忆起实验室检验二氧化碳的情景,心想:如果向澄清石灰水中不断通入二氧化碳,会看到怎样的现象呢?请你描述一下:石灰水先变浑浊,后又变回澄清.
(2)老师投影图片-新化县的梅山龙宫,冷水江市的波月洞,涟源市的藏经阁,双峰县的药王洞…宛如人间仙境的美丽溶洞,竟然是文中两个简单的化学反应创造?!同学们不禁对大自然的鬼斧神工咋不决口,纷纷表示“娄底那么大,我想去看看”.
【提出问题】一定量CO2与NaOH溶液反应后的溶质组成是什么?
【查阅资料】(1)通入少量CO2反应的化学方程式为:CO2+2NaOH=Na2CO3+H2O.
(2)通入过量CO2,反应的化学方程式为:Na2CO3+CO2+H2O═2NaHCO3.
(3)碳酸氢盐都是可溶于水的.BaCO3难溶于水.
(4)碳酸氢钠溶液呈碱性.
【提出猜想】(1)溶质为NaOH和Na2CO3;(2)溶质为Na2CO3;
(3)溶质为NaHCO3和Na2CO3(填化学式);(4)溶质为NaHCO3.
【设计实验】
| 实验步骤 | 实验现象 | 实验结论 |
| (1)用玻璃棒蘸取反应后溶液,滴在pH试纸上 | pH=9 | 该溶液显碱性 |
| (2)取反应后溶液少许于试管中,向其中滴加过量的BaCl2溶液 | 有 白色沉淀生成 | 猜想(4)不成立 |
| (3)取步骤(2)中的上层清液,滴入稀盐酸 | 有气泡冒出 | 猜想(1)和(2)不成立 |
【讨论交流】(1)有同学提出,实验步骤(1)是多余的.你认为该实验设计是否需要?不需要(填“需要”或“不需要”).
(2)同学们又一次把目光投向了教材,发现遇热或压强变小时:Ca(HCO3)2=CaCO3↓+CO2↑+H2O,纷纷提出,干粉灭火器中用NaHCO3灭火的反应原理与之相似,试写出NaHCO3受热分解的化学方程式:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
【反思应用】(1)同学们回忆起实验室检验二氧化碳的情景,心想:如果向澄清石灰水中不断通入二氧化碳,会看到怎样的现象呢?请你描述一下:石灰水先变浑浊,后又变回澄清.
(2)老师投影图片-新化县的梅山龙宫,冷水江市的波月洞,涟源市的藏经阁,双峰县的药王洞…宛如人间仙境的美丽溶洞,竟然是文中两个简单的化学反应创造?!同学们不禁对大自然的鬼斧神工咋不决口,纷纷表示“娄底那么大,我想去看看”.
7.科学兴趣小组的同学在学了俗称为苏打的碳酸钠后,得知它还有一个俗称为小苏打的“兄弟”,这个“兄弟”的性质是否和它相似?它们之间能发生转化吗?
小明查阅了资料,将相关信息整理如表:
下面是小明同学进行的探究:
(1)用试管取适量NaHCO3溶液,向试管中滴加酚酞试液,观察试液颜色变化.此实验的目的是检验NaHCO3溶液是否显碱性.
(2)在研究Na2CO3与NaHCO3转化时,小明觉得Na2CO3转化为NaHCO3过程中,由于NaHCO3溶于水,整个过程不会有明显现象.老师笑着对小明说:“做实验吧,实验会告诉你答案.”于是小明
在老师的指导下,向饱和的Na2CO3溶液中通入CO2,起初无明显现象,继续不断地通入CO2,溶液中出现了白色沉淀.这让小明很疑惑:NaHCO3溶于水,为什么还有白色沉淀呢?小明经过思考,明白了白色沉淀产生的原因是碳酸钠与二氧化碳反应后要生成碳酸氢钠,而碳酸氢钠的溶解度小于碳酸钠,所以出现了白色沉淀.
(3)在小明同学的带动下,兴趣小组又对NaHCO3的其他性质进行了探究,发现两“兄弟”既有相似的性质也有不同的个性.从微观角度分析,造成两“兄弟”不同个性的原因是酸根离子不同.
0 148337 148345 148351 148355 148361 148363 148367 148373 148375 148381 148387 148391 148393 148397 148403 148405 148411 148415 148417 148421 148423 148427 148429 148431 148432 148433 148435 148436 148437 148439 148441 148445 148447 148451 148453 148457 148463 148465 148471 148475 148477 148481 148487 148493 148495 148501 148505 148507 148513 148517 148523 148531 211419
小明查阅了资料,将相关信息整理如表:
| 俗名 | 苏打 纯碱 | 小苏打 |
| 化学式 | Na2CO3 | NaHCO3 |
| 构成微粒 | Na+ CO32- | Na+ HCO3- |
| 溶解度(常温) | 21.5克 | 9.6克 |
| 两者的转化 | Na2CO3+CO2+H2O═2NaHCO3 | 2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+CO2+H2O |
(1)用试管取适量NaHCO3溶液,向试管中滴加酚酞试液,观察试液颜色变化.此实验的目的是检验NaHCO3溶液是否显碱性.
(2)在研究Na2CO3与NaHCO3转化时,小明觉得Na2CO3转化为NaHCO3过程中,由于NaHCO3溶于水,整个过程不会有明显现象.老师笑着对小明说:“做实验吧,实验会告诉你答案.”于是小明
在老师的指导下,向饱和的Na2CO3溶液中通入CO2,起初无明显现象,继续不断地通入CO2,溶液中出现了白色沉淀.这让小明很疑惑:NaHCO3溶于水,为什么还有白色沉淀呢?小明经过思考,明白了白色沉淀产生的原因是碳酸钠与二氧化碳反应后要生成碳酸氢钠,而碳酸氢钠的溶解度小于碳酸钠,所以出现了白色沉淀.
(3)在小明同学的带动下,兴趣小组又对NaHCO3的其他性质进行了探究,发现两“兄弟”既有相似的性质也有不同的个性.从微观角度分析,造成两“兄弟”不同个性的原因是酸根离子不同.