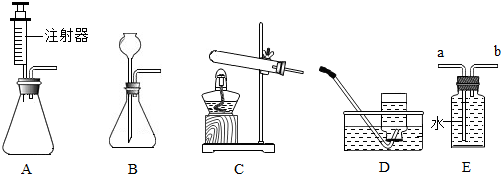
1.归纳法是一种非常好的学习化学的方法,下列归纳的结论错误的是( )
| A. | 任何化学反应都遵守质量守恒定律 | |
| B. | 化合反应一定是一种物质和氧气发生的反应 | |
| C. | 一定温度下,某物质的饱和溶液是不能再溶解该物质的溶液 | |
| D. | 含同种元素的两种物质,其物理性质和化学性质不一定相同 |
18. 在今天的化学兴趣小组活动中,指导老师拿来了一包已经失效的石灰干燥剂.为了确定该干燥剂的组成,同学们进行了如下的探究活动:
在今天的化学兴趣小组活动中,指导老师拿来了一包已经失效的石灰干燥剂.为了确定该干燥剂的组成,同学们进行了如下的探究活动:
小萌同学通过探究发现,此包装袋中的生石灰干燥剂已经完全变质失效.他采用的探究方法是:取少量样品于试管中,加入少量水,用手触摸试管外壁,没有明显的放热现象.此实验中加入的水必须是少量的,理由是如果所加的水较多,则水会吸收反应产生的热量,影响实验的结论.
【查阅资料】
石灰干燥剂的成分为CaO,请写出该干燥剂干燥原理CaO+H2O=Ca(OH)2(用化学方程式表示).
【提出猜想】①该干燥剂的成分为Ca(OH)2
②该干燥剂的成分为CaCO3
③你的猜想是CaCO3、Ca(OH)2;
【方案设计】小组成员设计了如下的实验方案:
方案一:取样滴加稀盐酸,有气泡产生,则白色固体只存在CaCO3;
方案二:取样滴加少量稀盐酸,没有气泡产生,则白色固体中只存在Ca(OH)2;
方案三:取样加入水中,振荡,静置,上层为清液,下层出现固体不溶物,取上层清液滴加酚酞试液,变红,则固体为CaCO3和Ca(OH)2的混合物.
【实验分析】小组成员经过讨论发现上述实验方案都存在着问题.
(1)上述方案一中存在的问题是不能说明白色固体中是否含有Ca(OH)2.
(2)上述方案二的结论是错误的,原因是由于加入的盐酸是少量的,可能只是与氢氧化钙发生了反应,还没有与碳酸钙反应,无法证明没有碳酸钙的存在.
(3)实验方案三中的结论也有些不妥,是因为不能说明白色固体中含有CaCO3,因为不溶物可能是微溶于水的氢氧化钙.
(4)实验证实,该固体是CaCO3和Ca(OH)2的混合物,请你再设计一种实验方案予以证明,只要写出实验步骤和现象即可.
【数据分析】
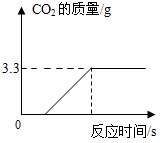
为了进一步确定该混合物中CaCO3的质量分数,实验小组的同学取了15克样品,加入足量的稀盐酸,实验测得生成CO2气体的质量如图所示,请据图计算该混合物中CaCO3的质量分数.
【反思与评价】
实验中造成计算结果与实际值相比偏小,则可能的原因是有部分生成的二氧化碳气体因溶解于水而没有全部逸出.
 在今天的化学兴趣小组活动中,指导老师拿来了一包已经失效的石灰干燥剂.为了确定该干燥剂的组成,同学们进行了如下的探究活动:
在今天的化学兴趣小组活动中,指导老师拿来了一包已经失效的石灰干燥剂.为了确定该干燥剂的组成,同学们进行了如下的探究活动:小萌同学通过探究发现,此包装袋中的生石灰干燥剂已经完全变质失效.他采用的探究方法是:取少量样品于试管中,加入少量水,用手触摸试管外壁,没有明显的放热现象.此实验中加入的水必须是少量的,理由是如果所加的水较多,则水会吸收反应产生的热量,影响实验的结论.
【查阅资料】
石灰干燥剂的成分为CaO,请写出该干燥剂干燥原理CaO+H2O=Ca(OH)2(用化学方程式表示).
【提出猜想】①该干燥剂的成分为Ca(OH)2
②该干燥剂的成分为CaCO3
③你的猜想是CaCO3、Ca(OH)2;
【方案设计】小组成员设计了如下的实验方案:
方案一:取样滴加稀盐酸,有气泡产生,则白色固体只存在CaCO3;
方案二:取样滴加少量稀盐酸,没有气泡产生,则白色固体中只存在Ca(OH)2;
方案三:取样加入水中,振荡,静置,上层为清液,下层出现固体不溶物,取上层清液滴加酚酞试液,变红,则固体为CaCO3和Ca(OH)2的混合物.
【实验分析】小组成员经过讨论发现上述实验方案都存在着问题.
(1)上述方案一中存在的问题是不能说明白色固体中是否含有Ca(OH)2.
(2)上述方案二的结论是错误的,原因是由于加入的盐酸是少量的,可能只是与氢氧化钙发生了反应,还没有与碳酸钙反应,无法证明没有碳酸钙的存在.
(3)实验方案三中的结论也有些不妥,是因为不能说明白色固体中含有CaCO3,因为不溶物可能是微溶于水的氢氧化钙.
(4)实验证实,该固体是CaCO3和Ca(OH)2的混合物,请你再设计一种实验方案予以证明,只要写出实验步骤和现象即可.
| 实验操作步骤 | 实验现象 |
| (1)取样,滴加足量稀盐酸 (2)另取适量的样品,加足量的水溶解,静置取上层清液,滴加酚酞试液 | (1)产生大量的气泡 (2)溶液呈红色 |
为了进一步确定该混合物中CaCO3的质量分数,实验小组的同学取了15克样品,加入足量的稀盐酸,实验测得生成CO2气体的质量如图所示,请据图计算该混合物中CaCO3的质量分数.
【反思与评价】
实验中造成计算结果与实际值相比偏小,则可能的原因是有部分生成的二氧化碳气体因溶解于水而没有全部逸出.
17. 春节期间,小颖陪妈妈去医院打点滴,发现护士往输液管上放了一个纸包,经询问得知它是输液恒温贴,可以温暖输入人体中的液体.小颖对包里的东西能产生热量感到很神奇,于是,他向护士要了一只输液恒温贴,带回来进行了如下探究.撕开真空包装封口,剪开内包装袋,倒出其中的粉末,发现呈黑色.
春节期间,小颖陪妈妈去医院打点滴,发现护士往输液管上放了一个纸包,经询问得知它是输液恒温贴,可以温暖输入人体中的液体.小颖对包里的东西能产生热量感到很神奇,于是,他向护士要了一只输液恒温贴,带回来进行了如下探究.撕开真空包装封口,剪开内包装袋,倒出其中的粉末,发现呈黑色.
【提出问题】黑色粉末可能含有哪些物质呢?
【猜想与假设】该黑色粉末可能含有炭粉、铁粉、二氧化锰、氧化铜、四氧化三铁中的一种或几种.
【初步验证】将磁铁靠近黑色粉末,部分被吸引.
【查阅资料】四氧化三铁能被磁铁吸引.四氧化三铁与盐酸反应生成氯化亚铁、氯化铁和水.
【初步结论】黑色粉末可能含有Fe3O4(或Fe).
【进行实验】
由上述实验可知,该黑色粉末肯定含有Fe和C,肯定不含CuO;写出实验①中产生气体的化学方程式Fe+H2SO4═FeSO4+H2↑.
【交流讨论】①输液恒温贴真空包装的原因:铁粉在空气中会与水和氧气发生缓慢氧化转化成铁锈,并放出热量.
②输液恒温贴中炭粉的作用是加快铁粉生锈.
 春节期间,小颖陪妈妈去医院打点滴,发现护士往输液管上放了一个纸包,经询问得知它是输液恒温贴,可以温暖输入人体中的液体.小颖对包里的东西能产生热量感到很神奇,于是,他向护士要了一只输液恒温贴,带回来进行了如下探究.撕开真空包装封口,剪开内包装袋,倒出其中的粉末,发现呈黑色.
春节期间,小颖陪妈妈去医院打点滴,发现护士往输液管上放了一个纸包,经询问得知它是输液恒温贴,可以温暖输入人体中的液体.小颖对包里的东西能产生热量感到很神奇,于是,他向护士要了一只输液恒温贴,带回来进行了如下探究.撕开真空包装封口,剪开内包装袋,倒出其中的粉末,发现呈黑色.【提出问题】黑色粉末可能含有哪些物质呢?
【猜想与假设】该黑色粉末可能含有炭粉、铁粉、二氧化锰、氧化铜、四氧化三铁中的一种或几种.
【初步验证】将磁铁靠近黑色粉末,部分被吸引.
【查阅资料】四氧化三铁能被磁铁吸引.四氧化三铁与盐酸反应生成氯化亚铁、氯化铁和水.
【初步结论】黑色粉末可能含有Fe3O4(或Fe).
【进行实验】
| 实验 编号 | 实验操作 | 实验现象 |
| ① | 取少量黑色粉末于试管中,加足量稀硫酸 | 固体部分溶解,有气泡产生,溶液变为浅绿色 |
| ② | 将实验①试管中的物质过滤,向滤液中加入足量铁粉 | 有气泡产生,无红色物质析出 |
| ③ | 取实验②的滤渣灼烧,将内壁涂有澄清石灰水的小烧杯罩在上方 | 澄清石灰水变浑浊 |
【交流讨论】①输液恒温贴真空包装的原因:铁粉在空气中会与水和氧气发生缓慢氧化转化成铁锈,并放出热量.
②输液恒温贴中炭粉的作用是加快铁粉生锈.
16.做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究.
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和硫酸两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液(NaOH和H2O)反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
【总结反思】丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立.经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸.兴趣小组的同学经过充分讨论,一致认为猜想(3)成立.
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
0 148336 148344 148350 148354 148360 148362 148366 148372 148374 148380 148386 148390 148392 148396 148402 148404 148410 148414 148416 148420 148422 148426 148428 148430 148431 148432 148434 148435 148436 148438 148440 148444 148446 148450 148452 148456 148462 148464 148470 148474 148476 148480 148486 148492 148494 148500 148504 148506 148512 148516 148522 148530 211419
【提出问题】溶液中的溶质是什么物质?
【作出猜想】
(1)甲同学认为溶液中的溶质只有Na2SO4一种物质.
(2)乙同学认为溶液中的溶质是Na2SO4和硫酸两种物质.
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液(NaOH和H2O)反应生成偏铝酸钠(NaAlO2)等物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液变红色 | 猜想(3)成立 |
【知识拓展】(1)生活中能否用铝制品来盛放强碱性溶液?不能(填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
 .
.
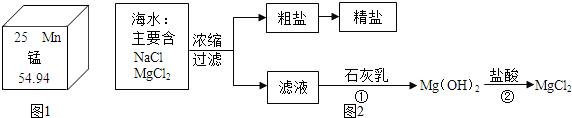
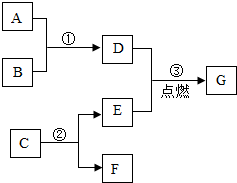 A-G是初中化学中常见的物质,其相互反应及转化关系如图所示,部分反应条件省略.已知A是易与人体血红蛋白结合的有毒气体,B是赤铁矿的主要成分,C是相对分子质量最小的氧化物,F是最轻的气体.
A-G是初中化学中常见的物质,其相互反应及转化关系如图所示,部分反应条件省略.已知A是易与人体血红蛋白结合的有毒气体,B是赤铁矿的主要成分,C是相对分子质量最小的氧化物,F是最轻的气体. 2016年4月16日厄瓜多尔发生7.8级强震,20日,中国政府派遣多支救援队到达厄首都基多,展开救助,同行携带大量救援物资,如消毐液、大米和帐篷等.
2016年4月16日厄瓜多尔发生7.8级强震,20日,中国政府派遣多支救援队到达厄首都基多,展开救助,同行携带大量救援物资,如消毐液、大米和帐篷等.