3.实验室长期保存下列试剂的方法中,不正确的是( )
| A. | 白磷保存在水中 | B. | 生石灰保存在烧杯中 | ||
| C. | 浓盐酸密封保存在试剂瓶中 | D. | 硝酸银溶液保存在棕色试剂瓶中 |
2.对下列事实的解释,不合理的是( )
| A. | 通过气味辨别氮气和氨气 分子是运动的,不同分子的性质不同 | |
| B. | 氧气经压缩储存在钢瓶中 压强增大,分子之间的间隔变小 | |
| C. | 干冰升华为二氧化碳气体 状态变化,分子大小随之变化 | |
| D. | 蔗糖在热水中溶解更快 温度越高,分子运动速率越大 |
1.根据下面实验内容书写的化学方程式,正确的是( )
| A. | 在空气中点燃镁条 Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO | |
| B. | 铝片放入稀硫酸中 Al+H2SO4═AlSO4+H2↑ | |
| C. | 氢氧化钠溶液中滴加氯化钡 2NaOH+BaCl2═Ba(OH)2↓+2NaCl | |
| D. | 碳酸钠溶液中滴加硝酸银 Na2CO3+2AgNO3═Ag2CO3↓+2NaNO3 |
19.日常生活中的下列做法,没有利用化学变化的是( )
| A. | 家庭自酿葡萄酒 | B. | 冰块给水产品保鲜 | ||
| C. | 卤水点制豆腐 | D. | 84消毒液漂白织物 |
18.合金的种类很多,用途非常广泛,黄铜是铜和锌的合金,它可以用来制造机器和电器的零件等,化学兴趣小组的同学欲测定实验室中某铜样品中铜的质量分数(不考虑黄铜中的其他杂质),请你参与他们的探究过程.
称量10g粉末状黄铜样品放入烧杯中,量取45mL稀盐酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
试求:
(1)m的数值0.04.
(2)此黄铜样品中铜的质量分数是多少?(写出计算过程)
称量10g粉末状黄铜样品放入烧杯中,量取45mL稀盐酸分三次加到其中,每次充分反应后,测定生成氢气的质量,实验数据如表:
| 第一次 | 第二次 | 第三次 | |
| 加入稀盐酸的体积(ml) | 15 | 15 | 15 |
| 生成氢气的质量(g) | 0.04 | m | 0.02 |
(1)m的数值0.04.
(2)此黄铜样品中铜的质量分数是多少?(写出计算过程)
16.请对如表中的化学方程式进行评价(填写评价序号),并注明化学反应类型.
评价序号:①完全正确 ②反应条件不正确 ③没有配平 ④违背客观事实.
0 148151 148159 148165 148169 148175 148177 148181 148187 148189 148195 148201 148205 148207 148211 148217 148219 148225 148229 148231 148235 148237 148241 148243 148245 148246 148247 148249 148250 148251 148253 148255 148259 148261 148265 148267 148271 148277 148279 148285 148289 148291 148295 148301 148307 148309 148315 148319 148321 148327 148331 148337 148345 211419
| 化学方程式 | 评价 | 化学反应类型 |
| MgCl2$\frac{\underline{\;\;△\;\;}}{\;}$Mg+Cl2↑ | ② | 分解反应 |
| Al+O2$\frac{\underline{\;点燃\;}}{\;}$Al2O3 | ③ | 化合反应 |
| HCl+NaOH═NaCl+H2O | ① | 复分解反应 |
| 2Fe+6HCl═2FeCl3+3H2↑ | ④ | 置换反应 |
 化学反应过程中常常伴随产生一些现象,同学们发现将CO2通入NaOH溶液时没有明显的现象发生,为此,他们进行了如下探究:
化学反应过程中常常伴随产生一些现象,同学们发现将CO2通入NaOH溶液时没有明显的现象发生,为此,他们进行了如下探究: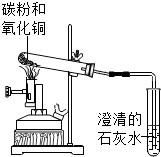 我们的祖先很早就掌握了炼铜的工艺,通过学习,同学们知道木炭可以作还原剂把氧化铜中的铜还原出来,小明查阅了大量的资料后,建议用超细炭粉与氧化铜粉末混合进行实验,他的理由是增大反应物的接触面积,使反应更充分.
我们的祖先很早就掌握了炼铜的工艺,通过学习,同学们知道木炭可以作还原剂把氧化铜中的铜还原出来,小明查阅了大量的资料后,建议用超细炭粉与氧化铜粉末混合进行实验,他的理由是增大反应物的接触面积,使反应更充分.