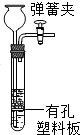
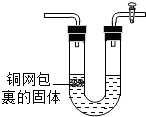
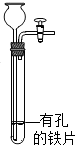
5.在工业炼铁中,石灰石发生的化学原理是:CaCO3+SiO2$\frac{\underline{\;高温\;}}{\;}$X+CO2↑,其中X的化学式是( )
| A. | CaSiO4 | B. | Ca2SiO3 | C. | CaSi2O3 | D. | CaSiO3 |
4.下列涉及学科观点的有关说法不正确的是( )
| A. | 微粒观:金刚石与石墨的碳原子排列顺序不同,故物理性质不同 | |
| B. | 结构观:一氧化碳和二氧化碳分子结构不同,其化学性质不同 | |
| C. | 转化观:在一定条件下,CO2与CO可以相互转化 | |
| D. | 守恒观:一定质量的甲烷不完全燃烧生成CO、CO2和H2O,经测定水的质量为18g,则甲烷质量为16g |
3.下列关于实验操作中先后顺序的叙述错误的是( )
| A. | 点燃可燃性气体前,先检验气体的纯度,后点燃 | |
| B. | 用滴管吸取液体时,先捏扁胶头赶尽空气,再伸入瓶中吸液 | |
| C. | 制取氧气实验停止时,应先把导管移出水面,然后再熄灭酒精灯 | |
| D. | 启普发生器制氢气时,先向漏斗中注入稀硫酸,再往容器中加入锌粒 |
1.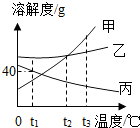 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )| A. | t2℃时,甲、乙两种物质的溶解度相等 | |
| B. | t1℃时,丙的饱和溶液中溶质的质量分数为28.6% | |
| C. | 取等质量t2℃时甲、乙、丙的饱和溶液,分别蒸发等量水后恢复至t2℃,析出晶体的质量:甲=乙>丙 | |
| D. | 分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,所得三种溶液中溶质质量分数大小关系是:乙>丙>甲 |
20.关于生活中常见的盐,下列说法不正确的是( )
| A. | 硫酸铜可用于对生吃的果蔬进行杀菌消毒 | |
| B. | 碳酸钙可用于防治骨质疏松症和治疗胃酸过多 | |
| C. | 食盐可用于调味和腌渍蔬菜、鱼、肉等 | |
| D. | 小苏打是焙制糕点所用的发酵粉的主要成分之一 |
19.下列有关铁的知识叙述不正确的是( )
| A. | 将生锈铁钉投入稀盐酸中,溶液逐渐变黄,并有气泡产生 | |
| B. | 硫酸铜、石灰水配制的农药波尔多液不能用铁制容器盛放 | |
| C. | 工业炼铁的原理是利用CO将铁从铁的氧化物中置换出来 | |
| D. | “暖宝宝”的化学原理是利用铁粉缓慢氧化放出热量 |
18.下列除去括号内杂质所选用的试剂或操作错误的是( )
| A. | CO2(CO)--通入O2点燃 | |
| B. | H2(CO2)--先通入NaOH溶液后通入浓硫酸 | |
| C. | CuSO4(H2SO4)--加CuO粉末再过滤 | |
| D. | H2O(H2O2)--加MnO2粉末再过滤 |
17.2016年“世界水日”的宣传主题是“水与就业”,下列有关水的说法正确的是( )
| A. | 淡水资源是取之不尽、用之不竭的 | |
| B. | 水电解所生成氢气和氧气的质量比为2:1 | |
| C. | 海水、湖水是混合物,自来水是纯净物 | |
| D. | 蒸馏可使海水转化为软水 |
16. 众所周知,在金属活动性顺序中,位于前面的金属能把位于后面的金属从其化合物的溶液中置换出来.化学小组同学将金属钠放入硫酸铜溶液时(如图),却没有得到红色的铜.
众所周知,在金属活动性顺序中,位于前面的金属能把位于后面的金属从其化合物的溶液中置换出来.化学小组同学将金属钠放入硫酸铜溶液时(如图),却没有得到红色的铜.
【提出问题】没有得到红色铜的原因是什么呢?
【猜想与假设】所用硫酸铜溶液的浓度过小.
【查阅资料】
①钠很活泼,常温下与水反应,生成氢氧化钠和氢气,且放出大量的热.
③氢氧化铜是蓝色絮状沉淀,难溶于水,受热至80℃以上分解为黑色氧化铜和水.
③氢氧化铜与盐酸可以发生复分解反应;氧化铜也与盐酸反应,且产物相同.
【进行实验】
【解释与结论】
(1)生成蓝色絮状沉淀时发生反应的化学方程式为2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
(2)步骤2中灰蓝色沉淀消失后生成的物质是CuCl2、H2O.
(3)实验一结果表明,猜想与假设不成立(填“成立”或“不成立”),依据是用浓的CuSO4溶液,也未得到红色固体(或铜).
【继续实验】
(4)在教师的指导下,同学们又设计了实验二:将饱和CuSO4溶液滴加在一小块钠上至钠完全反应,观察到表面生成灰黑色固体,周围有大量蓝色糊状物.同学们加入了试剂X将灰黑色和蓝色固体除去,看到有金属光泽的红色物质.则试剂X为20%盐酸.
【反思与评价】
(5)与实验一对比,实验二中得到红色铜的原因是实验二中的水少,有利于钠置换出铜.
0 148051 148059 148065 148069 148075 148077 148081 148087 148089 148095 148101 148105 148107 148111 148117 148119 148125 148129 148131 148135 148137 148141 148143 148145 148146 148147 148149 148150 148151 148153 148155 148159 148161 148165 148167 148171 148177 148179 148185 148189 148191 148195 148201 148207 148209 148215 148219 148221 148227 148231 148237 148245 211419
 众所周知,在金属活动性顺序中,位于前面的金属能把位于后面的金属从其化合物的溶液中置换出来.化学小组同学将金属钠放入硫酸铜溶液时(如图),却没有得到红色的铜.
众所周知,在金属活动性顺序中,位于前面的金属能把位于后面的金属从其化合物的溶液中置换出来.化学小组同学将金属钠放入硫酸铜溶液时(如图),却没有得到红色的铜.【提出问题】没有得到红色铜的原因是什么呢?
【猜想与假设】所用硫酸铜溶液的浓度过小.
【查阅资料】
①钠很活泼,常温下与水反应,生成氢氧化钠和氢气,且放出大量的热.
③氢氧化铜是蓝色絮状沉淀,难溶于水,受热至80℃以上分解为黑色氧化铜和水.
③氢氧化铜与盐酸可以发生复分解反应;氧化铜也与盐酸反应,且产物相同.
【进行实验】
| 实验一 | 实验操作 | 实验现象 |
| 步骤1 | 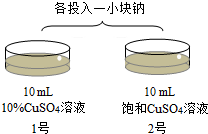 | 1号:钠在溶液中游动较少,发出嘶嘶声和持续的火光,最后消失,生成灰蓝色絮状沉淀. 2号:钠在溶液中几乎不游动,聚集在一起,发出嘶嘶声和持续的火光,最后发出啪的较大响声,然后消失,生成大量灰蓝色片状沉淀. |
| 步骤2 | 分别向1号、2号所得灰蓝色沉淀上加入等体积20%的盐酸 | 1号:沉淀完全消失,得到浅绿色溶液. 2号:沉淀完全消失,得到深绿色溶液. |
(1)生成蓝色絮状沉淀时发生反应的化学方程式为2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
(2)步骤2中灰蓝色沉淀消失后生成的物质是CuCl2、H2O.
(3)实验一结果表明,猜想与假设不成立(填“成立”或“不成立”),依据是用浓的CuSO4溶液,也未得到红色固体(或铜).
【继续实验】
(4)在教师的指导下,同学们又设计了实验二:将饱和CuSO4溶液滴加在一小块钠上至钠完全反应,观察到表面生成灰黑色固体,周围有大量蓝色糊状物.同学们加入了试剂X将灰黑色和蓝色固体除去,看到有金属光泽的红色物质.则试剂X为20%盐酸.
【反思与评价】
(5)与实验一对比,实验二中得到红色铜的原因是实验二中的水少,有利于钠置换出铜.