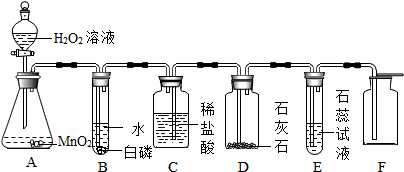
18.酸、碱、盐溶解性表示学习化学的重要工具,如表列出了部分酸、碱、盐的溶解性表(室温),请利用表中提供的信息完成以下问题:
(1)NaOH和FeCl3两种溶液混合后能(填“能”或“不能”)发生反应;
(2)写化学式:一种溶于水能够放出大量热的酸H2SO4.
(3)写出一个有水生成的化学方程式;HCl+NaOH═NaCl+H2O
(1)NaOH和FeCl3两种溶液混合后能(填“能”或“不能”)发生反应;
(2)写化学式:一种溶于水能够放出大量热的酸H2SO4.
(3)写出一个有水生成的化学方程式;HCl+NaOH═NaCl+H2O
| 离子 | OH- | Cl- | SO42- |
| H+ | 溶、挥 | 溶 | |
| Na+ | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 不 |
| Cu2+ | 不 | 溶 | 溶 |
13.在密闭容器中有以下四种物质,它们在一定条件下充分反应,测得有关数据如表所示,下列说法正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 14 | 36 | 20 | 11 |
| 反应后质量/g | 25 | 20 | 16 | 待测 |
| A. | 该反应一定是置换反应 | B. | 乙一定是氧化物 | ||
| C. | 待测值是20 | D. | 反应生成的甲、丁质量之比是5:4 |
12.研究性学习小组测定实验室里一瓶久置的NaOH固体是否变质.
【提出问题】NaOH固体是否变质?
【猜想假设】猜想1:没变质,全部是NaOH;
猜想2:全变质,全部是Na2CO3
猜想3:部分变质,既含有NaOH,又含有Na2CO3;
【进行实验】请你与他们一起完成,并回答所给问题.
上述步骤(1)中,滴加过量氯化钙溶液的目的是③使样品中的Na2C03完全反应.
【实验结论】通过实验,说明上述猜想中④猜想3是正确的.
【拓展】要除去氢氧化钠中含有的碳酸钠,所用的方法(用化学方程式表示)⑤Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【反思】通过探究,实验室中的氢氧化钠应⑥密封保存.
0 148038 148046 148052 148056 148062 148064 148068 148074 148076 148082 148088 148092 148094 148098 148104 148106 148112 148116 148118 148122 148124 148128 148130 148132 148133 148134 148136 148137 148138 148140 148142 148146 148148 148152 148154 148158 148164 148166 148172 148176 148178 148182 148188 148194 148196 148202 148206 148208 148214 148218 148224 148232 211419
【提出问题】NaOH固体是否变质?
【猜想假设】猜想1:没变质,全部是NaOH;
猜想2:全变质,全部是Na2CO3
猜想3:部分变质,既含有NaOH,又含有Na2CO3;
【进行实验】请你与他们一起完成,并回答所给问题.
| 实验步骤 | 实验现象 | 实验结论 |
| (1)称取上述固体样品8g溶于100mL水配成溶液,向溶液中滴加过量的氯化钙溶液充分反应后,静置. | 产生白色沉淀① | 说明久置固体中,一定含有Na2CO3 |
| (2)用玻璃棒蘸取少量①中的上层清液滴在pH试纸上,与标准比色卡对比,测出pH | pH=10 | 说明固体中,还一定含有 ②NaOH(填化学式). |
【实验结论】通过实验,说明上述猜想中④猜想3是正确的.
【拓展】要除去氢氧化钠中含有的碳酸钠,所用的方法(用化学方程式表示)⑤Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
【反思】通过探究,实验室中的氢氧化钠应⑥密封保存.
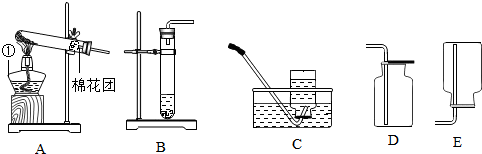
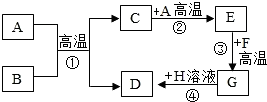 A-H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐,它们之间的转化关系如图所示,请回答:
A-H都是初中化学中常见的物质,已知B为黑色固体,D为红色固体单质,F为红色固体,H溶液中的溶质是一种盐,它们之间的转化关系如图所示,请回答: