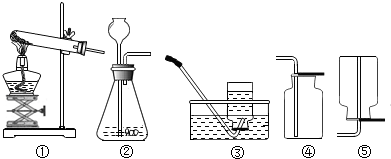
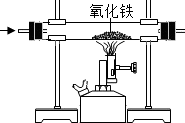
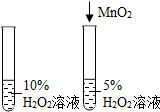
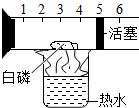
2.将一定量的乙醇(C2H6O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如表.下列判断正确的是( )
| 物质 | 乙醇 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 4.6 | 8.0 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 5.4 | 4.4 | a |
| A. | 表中a的值为2.6 | |
| B. | X一定是该反应的催化剂 | |
| C. | X可能含有氢元素 | |
| D. | 若起始时氧气的质量是9.6g,则无X生成 |
1.如图表示两种物质发生的化学反应,其中相同的球代表同种原子,小球间的短线代表原子间的结合,下列说法中不正确的是( )
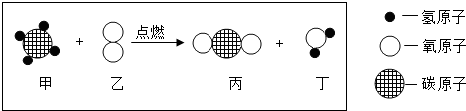

| A. | 甲物质属于有机化合物 | |
| B. | CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O | |
| C. | 图示反应前后原子的种类、个数不变 | |
| D. | 家用燃料若由煤气(主要成分为CO、H2)改为天然气,则燃气灶在进气口不变的情况下,进风口应变小 |
20.下列化学方程式与对应反应类型均正确的是( )
| 化学方程式 | 反应类型 | |
| A | Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O+CO2↑ | 分解反应 |
| B | 4Al+3O2═2Al2O3 | 化合反应 |
| C | 2Fe+6HCl═2FeCl3+3H2↑ | 置换反应 |
| D | SO3+2NaOH═Na2SO4+H2O | 复分解反应 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
16.下列鉴别物质的方法中,切实可行的是( )
| A. | 用酚酞试液鉴别氯化钠溶液和盐酸 | |
| B. | 用石蕊试液鉴别稀盐酸和稀硫酸 | |
| C. | 用水鉴别氢氧化钠固体和碳酸钙 | |
| D. | 用Na2CO3溶液鉴别Ca(OH)2溶液和CaCl2溶液 |
15.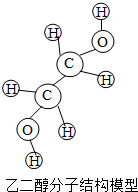 乙二醇是一种无色无臭、有甜味的液体,能与水以任意比例混合,可用作溶剂等.
乙二醇是一种无色无臭、有甜味的液体,能与水以任意比例混合,可用作溶剂等.
下列有关乙二醇的叙述错误的是( )
0 147955 147963 147969 147973 147979 147981 147985 147991 147993 147999 148005 148009 148011 148015 148021 148023 148029 148033 148035 148039 148041 148045 148047 148049 148050 148051 148053 148054 148055 148057 148059 148063 148065 148069 148071 148075 148081 148083 148089 148093 148095 148099 148105 148111 148113 148119 148123 148125 148131 148135 148141 148149 211419
 乙二醇是一种无色无臭、有甜味的液体,能与水以任意比例混合,可用作溶剂等.
乙二醇是一种无色无臭、有甜味的液体,能与水以任意比例混合,可用作溶剂等.下列有关乙二醇的叙述错误的是( )
| A. | 乙二醇的化学式为C2H602 | |
| B. | 乙二醇是由碳、氢、氧三种原子构成的 | |
| C. | 乙二醇与水不能形成饱和溶液 | |
| D. | 乙二醇可以用作汽车的防冻剂 |
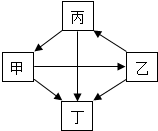 金属元素形成的化合物,依据物质的组成常见为氧化物、碱、盐,甲、乙、丙、丁均是由钙元素形成的四种常见化合物,丙、丁属于盐,另两种物质分别是氧化物和碱,它们之间的转化关系如图(部分反应物和产物已略去,“→”表示物质间存在转化关系).请回答
金属元素形成的化合物,依据物质的组成常见为氧化物、碱、盐,甲、乙、丙、丁均是由钙元素形成的四种常见化合物,丙、丁属于盐,另两种物质分别是氧化物和碱,它们之间的转化关系如图(部分反应物和产物已略去,“→”表示物质间存在转化关系).请回答