14.下列实验方案设计中,正确的是( )
| A. | 除去NaCl中少量的Na2CO3杂质,先加入足量稀硝酸,再蒸发结晶 | |
| B. | 检验可燃性气体中是否含有氢元素,在其燃烧火焰上方罩上干冷的烧杯,观察有无水雾 | |
| C. | 实验测定某矿石中碳酸钙的质量分数,先加入硫酸,再比较反应前后的质量变化 | |
| D. | 实验室制备干燥、纯净的氢气,用锌与浓盐酸反应,产生的气体经浓硫酸干燥后收集 |
13.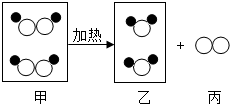 如图是某反应的微观示意图,若“
如图是某反应的微观示意图,若“ ”表示氧原子,“●”表示氢原子,下列有关说法不正确的是( )
”表示氧原子,“●”表示氢原子,下列有关说法不正确的是( )
 如图是某反应的微观示意图,若“
如图是某反应的微观示意图,若“ ”表示氧原子,“●”表示氢原子,下列有关说法不正确的是( )
”表示氧原子,“●”表示氢原子,下列有关说法不正确的是( )| A. | 图中甲、乙、丙三种物质都是氧化物 | |
| B. | 该反应属于分解反应 | |
| C. | 图中甲、乙、丙三种物质均是由分子构成的 | |
| D. | 该反应前后分子种类、原子种类均没有改变 |
12.下列实验现象的描述正确的是( )
| A. | 用玻璃尖嘴导管点燃CO,火焰呈蓝色,生成二氧化碳 | |
| B. | 光亮的铁丝插入到硫酸铜溶液中,铁丝表面有红色固体出现 | |
| C. | 二氧化碳通入氯化钙溶液中,溶液会变浑浊 | |
| D. | 干燥的红色石蕊试纸与氨气接触会变成蓝色 |
11.下列变化过程中,属于化学变化的是( )
| A. | 玉石摔碎 | B. | 风吹草动 | C. | 食物腐败 | D. | 滴水成冰 |
10.安多夫是一种嫩肉粉,成分是碳酸氢钠和氯化钠.小明发现将拌了安多夫粉的猪肉放到锅中加入食醋等调料烧煮时会产生大量的气体,他对此颇感兴趣,决定对其进行探究.

【查阅资料】
(1)碳酸氢钠是白色细小晶体,加热到50℃以上开始逐渐分解生成碳酸钠、二氧化碳和水,440℃时完全分解.
(2)白色无水硫酸铜遇到水会变成蓝色.
【实验探究一】对烧煮时产生大量气体的探究
(1)小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
他设法收集了除去醋酸气体的气体样品,用如图1装置验证水蒸气和CO2存在.装置导气管口正确的连接顺序是为:
气体样品→d→c→b→a.
(2)小明对二氧化碳的来源作了两种猜测:
猜测①:二氧化碳可能是由碳酸氢钠与食醋中的醋酸反应产生的.
猜测②:二氧化碳可能是由碳酸氢钠受热分解产生的.
针对以上猜测,小明设计了以下实验:
【实验结论】:猜想①、②都正确
【实验探究二】测定安多夫样品中碳酸氢钠的含量
上述实验2中,小明发现充分反应后,试管中仍留有一些白色固体粉末,通过查阅资料
发现是碳酸钠和氯化钠.小明想用测定白色固体中碳酸钠的质量来推算安多夫样品中碳酸氢钠的含量,于是称取实验2中得到的白色固体粉末6.9g,设计了如图2实验方案:
(1)“操作1”中玻璃棒的作用是引流.
(2)实验中加入过量氯化钙溶液的目的是使碳酸钠完全反应.
(3)确定沉淀A已洗涤干净的方法是取最后一次洗涤液,滴加硝酸银(或碳酸钠)溶液,无沉淀产生.
(4)该安多夫样品中NaHCO3的质量分数是84%.

【查阅资料】
(1)碳酸氢钠是白色细小晶体,加热到50℃以上开始逐渐分解生成碳酸钠、二氧化碳和水,440℃时完全分解.
(2)白色无水硫酸铜遇到水会变成蓝色.
【实验探究一】对烧煮时产生大量气体的探究
(1)小明对气体的成分进行了猜测:气体中除了醋酸气体之外,还可能含有水蒸气和CO2.
他设法收集了除去醋酸气体的气体样品,用如图1装置验证水蒸气和CO2存在.装置导气管口正确的连接顺序是为:
气体样品→d→c→b→a.
(2)小明对二氧化碳的来源作了两种猜测:
猜测①:二氧化碳可能是由碳酸氢钠与食醋中的醋酸反应产生的.
猜测②:二氧化碳可能是由碳酸氢钠受热分解产生的.
针对以上猜测,小明设计了以下实验:
| 实验步骤 | 实验现象 | |
| 实验1 | 取样与试管中,加入食醋 并将产生气体通入澄清石灰水中 | 有气泡产生 石灰水变浑浊 |
| 实验2 | 取安多夫样品少许加入试管中,加热使之充分反应,并把产生的气体通入澄清石灰水. | 试管口出现小水珠,澄清石灰水变浑浊,试管中残留白色固体粉末. |
【实验探究二】测定安多夫样品中碳酸氢钠的含量
上述实验2中,小明发现充分反应后,试管中仍留有一些白色固体粉末,通过查阅资料
发现是碳酸钠和氯化钠.小明想用测定白色固体中碳酸钠的质量来推算安多夫样品中碳酸氢钠的含量,于是称取实验2中得到的白色固体粉末6.9g,设计了如图2实验方案:
(1)“操作1”中玻璃棒的作用是引流.
(2)实验中加入过量氯化钙溶液的目的是使碳酸钠完全反应.
(3)确定沉淀A已洗涤干净的方法是取最后一次洗涤液,滴加硝酸银(或碳酸钠)溶液,无沉淀产生.
(4)该安多夫样品中NaHCO3的质量分数是84%.
8.某学习小组对硫酸进行如下研究:
(1)若对稀硫酸进行如下操作,溶液的pH升高的有ABC(填字母).
A.加少量水 B.加少量铁粉
C.加少量氢氧化钾 D.加少量浓硫酸
(2)向两个烧杯中分别注入两种硫酸,甲(溶质质量分数为98%,密度为1.84g/cm3)和乙(硫酸甲与水的按体积比1:1混和)各10mL,称量并记录不同时间(h)两种硫酸溶液吸水的质量,数据见表:
①若量取硫酸甲时俯视读数,在其他操作正确的情况下,所配硫酸乙的溶质质量分数将偏小(填“偏大”、“偏小”或“不变”).
②由表中实验数据可知:有关硫酸吸水性的说法错误的是B(填字母).
A.硫酸甲和乙都有吸水性 B.只有硫酸甲有吸水性 C.硫酸甲的吸水性较硫酸乙强
(3)小军同学利用稀释后的稀硫酸和硝酸钡、氢氧化钠、碳酸钾等物质的溶液对“复分解反应发生的条件”进行再探究.
①将上述四种溶液两两混合,判断其两两之间能否发生反应,请写出其中发生中和反应的化学方程H2SO4+2NaOH═Na2SO4+2H2O.
②利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液.经测定,该溶液显酸性.则在该溶液中一定含有的离子是H+、Na+、K+和NO3-,可能含有的离子是SO42-.
(1)若对稀硫酸进行如下操作,溶液的pH升高的有ABC(填字母).
A.加少量水 B.加少量铁粉
C.加少量氢氧化钾 D.加少量浓硫酸
| 时间/h | 1 | 1.5 | 4 | 8 | 12 | 24 | 48 | 60 | |
| 吸水 质量/g | 硫酸甲 | 1.6 | 2.2 | 5.2 | 10.3 | 14.0 | 20.9 | 29.2 | 32.1 |
| 硫酸乙 | 1.2 | 1.5 | 3.5 | 5.9 | 8.1 | 12.9 | 19.5 | 21.0 | |
①若量取硫酸甲时俯视读数,在其他操作正确的情况下,所配硫酸乙的溶质质量分数将偏小(填“偏大”、“偏小”或“不变”).
②由表中实验数据可知:有关硫酸吸水性的说法错误的是B(填字母).
A.硫酸甲和乙都有吸水性 B.只有硫酸甲有吸水性 C.硫酸甲的吸水性较硫酸乙强
(3)小军同学利用稀释后的稀硫酸和硝酸钡、氢氧化钠、碳酸钾等物质的溶液对“复分解反应发生的条件”进行再探究.
①将上述四种溶液两两混合,判断其两两之间能否发生反应,请写出其中发生中和反应的化学方程H2SO4+2NaOH═Na2SO4+2H2O.
②利用上述四种物质的溶液完成实验后,将所得物质混合并过滤,得到一种无色溶液.经测定,该溶液显酸性.则在该溶液中一定含有的离子是H+、Na+、K+和NO3-,可能含有的离子是SO42-.
5.把一定质量的甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如表,下列说法中正确的是( )
0 147925 147933 147939 147943 147949 147951 147955 147961 147963 147969 147975 147979 147981 147985 147991 147993 147999 148003 148005 148009 148011 148015 148017 148019 148020 148021 148023 148024 148025 148027 148029 148033 148035 148039 148041 148045 148051 148053 148059 148063 148065 148069 148075 148081 148083 148089 148093 148095 148101 148105 148111 148119 211419
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前的质量(g) | 6.4 | 4.0 | 3.2 | 2.8 |
| 反应后的质量(g) | 5.2 | 7.2 | 1.2 | X |
| A. | 乙可能是化合物 | |
| B. | 丁一定为该反应的催化剂 | |
| C. | 若消耗6g甲,则生成16g乙 | |
| D. | 甲和丙的质量之和一定等于乙的质量 |
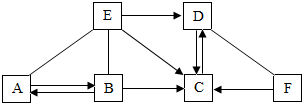 框图中的物质为初中化学常见的物质,其中A、B、C、D、E是不同类别的物质,胃液中含有少量的E,可帮助消化,B的固体在空气中易潮解,F是常见的一种红棕色固体.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.
框图中的物质为初中化学常见的物质,其中A、B、C、D、E是不同类别的物质,胃液中含有少量的E,可帮助消化,B的固体在空气中易潮解,F是常见的一种红棕色固体.图中“-”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去.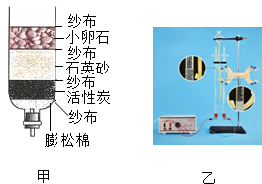 2016年3月22日是“世界水日”.水与人类的生活和生产密切相关.
2016年3月22日是“世界水日”.水与人类的生活和生产密切相关.