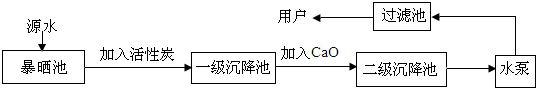
12.良好合理的健康饮食习惯可使身体健康地成长、发育,下列说法正确的是( )
| A. | 用水果代替正餐 | B. | 多吃奶类、大豆及其制品 | ||
| C. | 只吃肉,不吃菜 | D. | 纯净水才健康 |
11.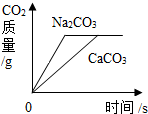 将等质量的碳酸钙粉末和碳酸钠粉末,分别浸入一定量10%盐酸和10%硫酸溶液中,产生二氧化碳的质量随时间变化曲线如图所示,下列说法正确的是( )
将等质量的碳酸钙粉末和碳酸钠粉末,分别浸入一定量10%盐酸和10%硫酸溶液中,产生二氧化碳的质量随时间变化曲线如图所示,下列说法正确的是( )
 将等质量的碳酸钙粉末和碳酸钠粉末,分别浸入一定量10%盐酸和10%硫酸溶液中,产生二氧化碳的质量随时间变化曲线如图所示,下列说法正确的是( )
将等质量的碳酸钙粉末和碳酸钠粉末,分别浸入一定量10%盐酸和10%硫酸溶液中,产生二氧化碳的质量随时间变化曲线如图所示,下列说法正确的是( )| A. | 碳酸钙一定没有剩余 | |
| B. | 消耗HCl和H2SO4的质量比为73:98 | |
| C. | 消耗碳酸钙与碳酸钠的质量比为1:1 | |
| D. | 反应产生水的质量相等 |
10.在一密闭容器内有A、B、C、D四种物质,在一定条件下发生化学反应,一段时间后,测得反应前后各物质的质量如下表,则下列说法中正确的是( )
| 物质 | A | B | C | D |
| 反应前物质质量(g) | 10 | 90 | 8 | 2 |
| 反应后物质质量(g) | 38 | 56 | 14 | X |
| A. | 反应中A和C的质量比为19:7 | B. | B一定是化合物 | ||
| C. | D一定是该反应的催化剂 | D. | 根据质量守恒定律,X的值为0 |
9.以下四组离子,有一组能大量共存且能形成无色透明溶液,它应该是( )
| A. | Fe3+ SO42- H+ Cl- | B. | Mg2+ Cl- OH- Na+ | ||
| C. | H+ Ba2+ NO3- SO42- | D. | K+H+Na+NO3- |
8.武学成同学学习了锌与硫酸反应制取氢气实验后,进行铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了如下的探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.SO2能与氢氧化钠溶液发生反应.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】武学成同学用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.

请帮助武学成同学完成如表:
【实验结论】铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸浓度达到足够大时,生成的气体产物中有二氧化硫;当硫酸溶液浓度较稀时,生成的气体产物是氢气.
【交流与反思】(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】武学成同学又将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液面以下的原因是形成液封,防止生成的气体逸出;该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸入试管.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.SO2能与氢氧化钠溶液发生反应.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】武学成同学用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.

请帮助武学成同学完成如表:
| A中硫 酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品 红溶液 | D中品 红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | 有二氧化硫和氢气 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
【交流与反思】(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】武学成同学又将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液面以下的原因是形成液封,防止生成的气体逸出;该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸入试管.
6.张南同学为测定某稀硫酸溶液中溶质的质量分数,取900g稀硫酸,平均分成6份,分别向其中加入镁粉使之充分反应,每次加入的镁粉的质量及测定生成硫酸镁的质量,记录数据如表:
(1)请写出实验中发生反应的化学方程式Mg+H2SO4═MgSO4+H2↑.
(2)表中两个空格内的数据分别是10和18;
(3)第一次反应结束后,消耗硫酸质量(x)的比例式为$\frac{24}{98}=\frac{1g}{x}$或$\frac{98}{120}=\frac{x}{5g}$;
(4)这种稀硫酸中溶质的质量分数为9.8%.
(5)若第四次反应完成后,把所得溶液蒸发掉3.3g水(此过程没有晶体析出),则最终所得溶液溶质的质量分数为3%;
(6)若用98%的浓硫酸配制上述实验中所需的稀硫酸,则需要加蒸馏水的质量是810g.
0 147803 147811 147817 147821 147827 147829 147833 147839 147841 147847 147853 147857 147859 147863 147869 147871 147877 147881 147883 147887 147889 147893 147895 147897 147898 147899 147901 147902 147903 147905 147907 147911 147913 147917 147919 147923 147929 147931 147937 147941 147943 147947 147953 147959 147961 147967 147971 147973 147979 147983 147989 147997 211419
| 实验次数 | 一 | 二 | 三 | 四 | 五 | 六 |
| 加入镁粉的质量/克 | 1 | 2 | 3 | 4 | 5 | 6 |
| 生成硫酸镁的质量/克 | 5 | 15 | 18 | 18 |
(2)表中两个空格内的数据分别是10和18;
(3)第一次反应结束后,消耗硫酸质量(x)的比例式为$\frac{24}{98}=\frac{1g}{x}$或$\frac{98}{120}=\frac{x}{5g}$;
(4)这种稀硫酸中溶质的质量分数为9.8%.
(5)若第四次反应完成后,把所得溶液蒸发掉3.3g水(此过程没有晶体析出),则最终所得溶液溶质的质量分数为3%;
(6)若用98%的浓硫酸配制上述实验中所需的稀硫酸,则需要加蒸馏水的质量是810g.