7.在一次科学实验中,同学们将饱和CuSO4溶液逐滴加到5mL饱和NaOH溶液中,观察到以下异常实验现象:
在实验①中同学们根据所学初中科学知识判断蓝色沉淀是Cu(OH)2,请写出生成蓝色沉淀的化学方程式
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】I.Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO
II.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色
【猜想与讨论】同学们交流讨论后,提出以下两种猜想.
猜想一:少许Cu(OH)2可溶于足量水中
猜想二:Cu(OH)2可在足量NaOH浓溶液中溶解,溶液呈亮蓝色
【实验探究】为验证猜想,同学们用Cu(OH)2粉末设计如下实验:
【结论与反思】根据实验可知饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应,依据的实验现象是资料Ⅰ显示Cu在室温下稳定,70℃-80℃时可脱水分解生成CuO,而表格1可知随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多,振荡后沉淀不消失,很快沉淀逐渐变黑色.
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1-6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7-9滴 | 产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色 |
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】I.Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO
II.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色
【猜想与讨论】同学们交流讨论后,提出以下两种猜想.
猜想一:少许Cu(OH)2可溶于足量水中
猜想二:Cu(OH)2可在足量NaOH浓溶液中溶解,溶液呈亮蓝色
【实验探究】为验证猜想,同学们用Cu(OH)2粉末设计如下实验:
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中, 充分振荡 | 沉淀不消失 | 猜想一错误 |
| ④ | 将少许Cu(OH)2粉末加到NaOH浓溶液中, 充分振荡 | 沉淀消失,溶液变成亮蓝色 | 猜想二正确 |
6.已知T℃时四种化合物在水中和液氨中的溶解度如下表:
(1)T℃时,把100g硝酸钡放入100g水中,充分溶解后,所得溶液的质量为192g.
(2)上述四种物质能在液氨中发生复分解反应的化学方程式为Ba(NO3)2+2AgCl=2AgNO3+BaCl2↓.
| AgNO3 | Ba(NO3)2 | AgCl | BaCl2 | |
| H2O | 170g | 92.0g | 1.50×10-4g | 33.3g |
| NH3 | 86.0g | 97.2g | 0.80g | 0.00g |
(2)上述四种物质能在液氨中发生复分解反应的化学方程式为Ba(NO3)2+2AgCl=2AgNO3+BaCl2↓.
4.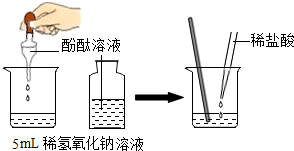 根据如图,判断以下说法错误的是( )
根据如图,判断以下说法错误的是( )
 根据如图,判断以下说法错误的是( )
根据如图,判断以下说法错误的是( )| A. | 取液后的滴管不能倒置 | B. | 用玻璃棒搅拌使反应充分 | ||
| C. | 用酚酞溶液判断该反应是否发生 | D. | 生成盐和水的反应都是酸碱反应 |
19.为验证下列化学变化的发生,需要滴加指示剂才能观察到实验现象的是( )
| A. | 向石灰石中滴加盐酸 | B. | 向氧化铁中滴加硫酸 | ||
| C. | 向水中通入二氧化碳 | D. | 向氢氧化钙溶液中通入二氧化碳 |
18.科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置.下面是该反应的微观示意图,下列说法错误的是( )

0 147796 147804 147810 147814 147820 147822 147826 147832 147834 147840 147846 147850 147852 147856 147862 147864 147870 147874 147876 147880 147882 147886 147888 147890 147891 147892 147894 147895 147896 147898 147900 147904 147906 147910 147912 147916 147922 147924 147930 147934 147936 147940 147946 147952 147954 147960 147964 147966 147972 147976 147982 147990 211419

| A. | 该反应不属于置换反应 | |
| B. | W物质中碳元素的质量分数为75% | |
| C. | 参加反应的X、Y两物质的粒子个数比为3:4 | |
| D. | 化学反应前后原子的种类、个数、质量均保持不变 |
 如图,在实验台上放置两瓶气体,集气瓶A、B中分别盛有CO2、O2、H2中的一种.
如图,在实验台上放置两瓶气体,集气瓶A、B中分别盛有CO2、O2、H2中的一种.
 水是生命之源,也是日常生活、工农业生产必不可少的.
水是生命之源,也是日常生活、工农业生产必不可少的.