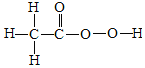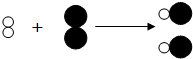6.下列过程发生了化学变化的是( )
①葡萄榨汁②葡萄酿酒③用土烧制瓷器④用土堆成土丘⑤稻草造纸⑥用纸制作风筝⑦头发剪断⑧头发长长.
①葡萄榨汁②葡萄酿酒③用土烧制瓷器④用土堆成土丘⑤稻草造纸⑥用纸制作风筝⑦头发剪断⑧头发长长.
| A. | ①③⑤⑧ | B. | ②③⑤⑥ | C. | ①③⑤⑥ | D. | ②③⑤⑧ |
3.某兴趣小组同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:氢氧化钠溶液滴入酚酞试液中,溶液变成了红色,一会儿红色就消失了.
【猜想】可能与氢氧化钠溶液质量分数大小有关.
【实验设计一】
【反思与评价】
通过大家分析讨论,认为可能还有以下猜想:
猜想一、可能是酚酞变质的缘故;
猜想二、可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
猜想三、可能是酚酞与空气中氧气反应,使红色消失的缘故. …
【实验设计二】为证实猜想三,做如下实验,请完成下表.
【理论分析】猜想一不对,理由是若酚酞试液变质,就不可能出现遇氢氧化钠溶液变红的现象;
猜想二也不正确,理由是碳酸钠溶液显碱性,也可使酚酞试液变红;
猜想三也不正确,理由是实验过程中试液一直与氧气接触.
【猜想】可能与氢氧化钠溶液质量分数大小有关.
【实验设计一】
| 实验方法 | 观察到的现象和结论 |
| 分别配制不同质量分数的氢氧化钠溶液,然后各滴加2滴酚酞试液. | 质量分数小的溶液中红色不消失,质量分数大的溶液中红色会消失,则证明与NaOH溶液质量分数大小有关. |
通过大家分析讨论,认为可能还有以下猜想:
猜想一、可能是酚酞变质的缘故;
猜想二、可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
猜想三、可能是酚酞与空气中氧气反应,使红色消失的缘故. …
【实验设计二】为证实猜想三,做如下实验,请完成下表.
| 实验步骤 | 设计这一步骤的目的 |
| 1.用煮沸过的蒸馏水配制氢氧化钠溶液. | 排除水中溶解的O2 |
| 2.在氢氧化钠溶液中滴入酚酞,并在上 方滴一些植物油. | 隔绝O2 |
猜想二也不正确,理由是碳酸钠溶液显碱性,也可使酚酞试液变红;
猜想三也不正确,理由是实验过程中试液一直与氧气接触.
1.小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加入指示剂,导致无法判断该中和反应进行的程度.于是他对所得溶液的酸碱性进行探究.
[探究目的]探究所得溶液的酸碱性.
[提出猜想]
所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
[实验验证]
[分析与思考]
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入CuCl2溶液,直到不产生沉淀为止.然后过滤,把滤液倒人蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为CuCl2+2NaOH═Cu(OH)2↓+2NaCl.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸性、小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到有气泡产生,则所取溶液呈酸性;若无明显现象,则呈中性.
方案二:取样,加入金属锌,若有气泡产生,则所取溶液酸性,该反应的化学方程式为Zn+2HCl═ZnCl2+H2↑;若无明显现象,则呈中性.
[探究目的]探究所得溶液的酸碱性.
[提出猜想]
所得溶液可能呈碱性,也可能呈中性,还可能呈酸性.
[实验验证]
| 实验操作 | 实验现象 | 结 论 |
| 用试管取该溶液lmL~2mL,滴入1-2滴无色酚酞试液,振荡 | 无色酚酞试液变红 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈中性或酸性 |
(1)若溶液呈碱性,则溶液中使其呈碱性的离子是OH-(填写微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入CuCl2溶液,直到不产生沉淀为止.然后过滤,把滤液倒人蒸发皿中加热,得到氯化钠晶体,该过程涉及的化学方程式为CuCl2+2NaOH═Cu(OH)2↓+2NaCl.
(2)若无色酚酞试液不变色,为了进一步确定溶液的酸性、小亮提出了以下方案:
方案一:取样,加入碳酸钠溶液,若观察到有气泡产生,则所取溶液呈酸性;若无明显现象,则呈中性.
方案二:取样,加入金属锌,若有气泡产生,则所取溶液酸性,该反应的化学方程式为Zn+2HCl═ZnCl2+H2↑;若无明显现象,则呈中性.
20.”塑化剂”的主要成分是邻苯二甲酸二辛酯,其化学式为C24H38O4,下列说法错误的是( )
| A. | 它是一种有机物 | |
| B. | 邻苯二甲酸二辛酯是由碳原子、氢原子、氧原子构成 | |
| C. | 它是由碳、氢、氧三种元素组成 | |
| D. | 一个邻苯二甲酸二辛酯分子中含66个原子 |
19.下列灭火方法不合理的是( )
| A. | 酒精洒在桌面上燃烧,立即用湿抹布扑灭 | |
| B. | 油锅着火,泼水灭火 | |
| C. | 森林发生火灾,砍掉部分树木,形成隔离带 | |
| D. | 纸箱着火,用水浇灭 |
17.在研究酸和碱的化学性质时,某小组想证明稀硫酸与氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应,试与他们一起完成实验方案的设计,实施和评价,并得出有关结论.
(1)探究稀硫酸与氢氧化钠溶液的反应:
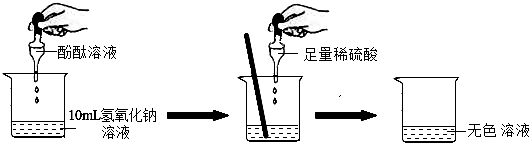
根据上述实验中颜色变化,可确定稀硫酸与氢氧化钠溶液发生了化学变化,反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O.
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:
根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量,同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并分析:
上述设计的实验方案中,正确的是方案二(填“方案一”或“方案二”)
另外一个实验方案错误的原因是NaOH和H2SO4反应后生成的硫酸钠也能和BaCl2反应产生白色沉淀BaSO4;
请你设计一个确定稀硫酸是否过量的实验方案,你选用的药品是锌粒(或碳酸钠等),实验现象及结论是若有气体放出,证明稀硫酸过量,反之稀硫酸不过量.
0 147727 147735 147741 147745 147751 147753 147757 147763 147765 147771 147777 147781 147783 147787 147793 147795 147801 147805 147807 147811 147813 147817 147819 147821 147822 147823 147825 147826 147827 147829 147831 147835 147837 147841 147843 147847 147853 147855 147861 147865 147867 147871 147877 147883 147885 147891 147895 147897 147903 147907 147913 147921 211419
(1)探究稀硫酸与氢氧化钠溶液的反应:

根据上述实验中颜色变化,可确定稀硫酸与氢氧化钠溶液发生了化学变化,反应的化学方程式为:2NaOH+H2SO4=Na2SO4+2H2O.
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:
根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量,同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并分析:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
| 方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀硫酸过量 |
另外一个实验方案错误的原因是NaOH和H2SO4反应后生成的硫酸钠也能和BaCl2反应产生白色沉淀BaSO4;
请你设计一个确定稀硫酸是否过量的实验方案,你选用的药品是锌粒(或碳酸钠等),实验现象及结论是若有气体放出,证明稀硫酸过量,反之稀硫酸不过量.

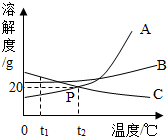 如图是A、B、C三种固体物质的溶解度曲线.
如图是A、B、C三种固体物质的溶解度曲线.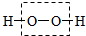 ②H-O-H ③O=C=O ④
②H-O-H ③O=C=O ④