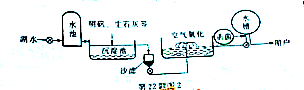
8.下列各组物质的溶液不用其他试剂就可鉴别的是( )
| A. | NaCl Na2CO3 Ca(NO3)2 HCl | |
| B. | HCl CuSO4 KNO3 Na2SO4 | |
| C. | Na2SO4 BaCl2 K2CO3 KNO3 | |
| D. | NaNO3 Na2SO4 HCl H2SO4 |
6.下列实验操作先后顺序正确的是( )
| A. | 蒸发食盐水时,先在铁圈上放置蒸发皿,后放酒精灯 | |
| B. | 如果不慎将碱液沾到皮肤上,先涂上硼酸液,后用大量水冲洗 | |
| C. | 测定溶液pH,先将试纸湿润,后用干净的玻璃棒蘸取待测液点在试纸上 | |
| D. | 氯酸钾制氧气结束时,先把导管从盛有水的烧杯中取出,再停止加热 |
3.下列实验方案中,设计合理的是( )
| A. | 检验二氧化碳中是否含有氯化氢气体,用紫色的石蕊溶液检验 | |
| B. | 除去铜粉中的氧化铜,将混合物放入稀硫酸中,过滤,洗涤,烘干 | |
| C. | 制少量氢氧化镁,将适量的氢氧化钡溶液与硫酸镁溶液混合,过滤 | |
| D. | 分离氯化钠和氯化钙,加入适量碳酸钠溶液,充分反应后,过滤,蒸发 |
2.“H68黄铜”(即铜含量为68%的铜锌合金),可焊性、耐蚀性能等均佳,是应用最广的一种黄铜.小东为测定市场上某黄铜制品中铜的实际含量,将10g黄铜样品加入烧杯中,分六次加入某稀硫酸,每次充分反应后,测得剩余固体的质量,数据记录如下:
(1)小东要配制50g溶质的质量分数为19.6%的稀硫酸用于测得黄铜样品.计算他所需98%的浓硫酸的质量和加入水的质量.(写出计算过程)
(2)分析上表数据,小东测得的黄铜样品的实际含铜质量分数为67.5%.
(3)实验结束后,小东测得剩余溶液显酸性.计算剩余溶液中硫酸的质量分数.
| 实验记录序号 | (1) | (2) | (3) | (4) | (5) | (6) |
| 加入稀硫酸质量/g | 5 | 5 | 5 | 5 | 5 | 5 |
| 剩余固体质量/g | 9.35 | 8.70 | 8.05 | 7.40 | 6.75 | 6.75 |
(2)分析上表数据,小东测得的黄铜样品的实际含铜质量分数为67.5%.
(3)实验结束后,小东测得剩余溶液显酸性.计算剩余溶液中硫酸的质量分数.
1.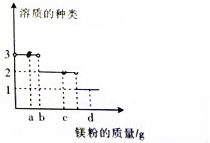 在一定量的AgNO3和Fe(NO3)2的混合溶液中加入镁粉,其溶质种类与加入镁粉的质量关系如图,下列说法正确的是( )
在一定量的AgNO3和Fe(NO3)2的混合溶液中加入镁粉,其溶质种类与加入镁粉的质量关系如图,下列说法正确的是( )
 在一定量的AgNO3和Fe(NO3)2的混合溶液中加入镁粉,其溶质种类与加入镁粉的质量关系如图,下列说法正确的是( )
在一定量的AgNO3和Fe(NO3)2的混合溶液中加入镁粉,其溶质种类与加入镁粉的质量关系如图,下列说法正确的是( )| A. | 加入a g镁粉时,溶液中溶质为硝酸镁、硝酸银、硝酸亚铁 | |
| B. | 加入b g镁粉时溶液中一定含有硝酸银 | |
| C. | 加入c g镁粉时,过滤出的滤渣为铁和银 | |
| D. | 加入d g镁粉时,溶液中溶质为硝酸镁和硝酸铁 |
20.如图中实验操作正确的是( )
| A. | 闻气体气味 | B. | 取用块状固体 | C. | 滴加液体 | D. | 加热液体 |
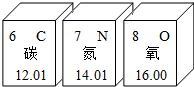
19.如图摘自元素周期表,据此判断下列叙述错误的是( )
0 147620 147628 147634 147638 147644 147646 147650 147656 147658 147664 147670 147674 147676 147680 147686 147688 147694 147698 147700 147704 147706 147710 147712 147714 147715 147716 147718 147719 147720 147722 147724 147728 147730 147734 147736 147740 147746 147748 147754 147758 147760 147764 147770 147776 147778 147784 147788 147790 147796 147800 147806 147814 211419

| A. | 氮原子的核外电子数为7 | |
| B. | 氧的相对原子质量为16.00 | |
| C. | C、N、0的原子序数依次增增 | |
| D. | 碳、氮、氧在元素周期表中属于同一族 |
 如图是某物质的分子结构示意图,小球代表一种原子,大球代表另一种原子.完成下列各题:
如图是某物质的分子结构示意图,小球代表一种原子,大球代表另一种原子.完成下列各题: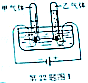 水是我们接触最多的物质.
水是我们接触最多的物质.