5.物质的变化需要在一定条件下进行,通过控制反应条件可以控制化学反应的快慢.下列做法是为了减慢化学反应的是( )
| A. | 用较浓的食醋除水垢 | |
| B. | 实验室制取氧气时用二氧化锰做催化剂 | |
| C. | 将食物放入冰箱中保存 | |
| D. | 烧煤时煤块粉碎成煤粉 |
4.化学与生活、社会密切相关.下列说法不正确的是( )
| A. | 施用熟石灰改良酸性土壤时,不宜同时施用碳酸氢铵 | |
| B. | 不吃水果蔬菜,多吃含蛋白质的肉类,更能增强体质 | |
| C. | 为防止电池中的重金属等污染土壤和水体,积极开发废电池综合利用技术 | |
| D. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
3.小红在餐厅看到服务员用盖子熄灭燃着的固体酒精,该灭火方法的主要原理是( )
| A. | 使可燃物的温度降低到着火点以下 | B. | 隔绝氧气 | ||
| C. | 降低可燃物的着火点 | D. | 移走可燃物 |
2.溶液是一种重要的混合物,下列关于溶液的叙述正确的是( )
| A. | 溶液中各部分的性质可能不相同 | |
| B. | 一瓶食盐水密封放置2天后,食盐会从水中分离出来 | |
| C. | 厨房洗涤剂能溶解油污形成溶液 | |
| D. | 向室温下硝酸钾的饱和溶液中加入水,所得溶液还可以继续溶解硝酸钾 |
1. 构建分子模型是研究分子的常用方法.复方冬青油软膏具有强力迅速镇痛的作用,其有效成分的分子模型如图所示,下列说法中正确的是( )
构建分子模型是研究分子的常用方法.复方冬青油软膏具有强力迅速镇痛的作用,其有效成分的分子模型如图所示,下列说法中正确的是( )
 构建分子模型是研究分子的常用方法.复方冬青油软膏具有强力迅速镇痛的作用,其有效成分的分子模型如图所示,下列说法中正确的是( )
构建分子模型是研究分子的常用方法.复方冬青油软膏具有强力迅速镇痛的作用,其有效成分的分子模型如图所示,下列说法中正确的是( )| A. | 该有机物的化学式为C8H7O3 | |
| B. | 该有机物中碳、氢、氧的质量比为8:8:3 | |
| C. | 与分子模型相比,化学式不能表示分子中原子的排列方式,因此,分子模型比化学式更有推广价值 | |
| D. | 该有机物完全燃烧生成二氧化碳和水 |
20.随着科技的不断进步,在显微镜下观察分子和原子的运动已经成为可能,经过科学家们不断地探索和努力,分子、原子的理论愈来愈完善,下列说法不正确的是( )
| A. | 从科学预测分子原子的存在,到真实看到分子原子,科学研究是一个大胆假设、实践验证的过程 | |
| B. | 原子是化学变化中的表现是由最外层电子决定的 | |
| C. | 原子是有外壳的球体,在分子中静止不动 | |
| D. | 分子、原子都是由更小的粒子构成的 |
19.化学用语是国际通用的化学语言,下列有关说法正确的是( )
| A. | 一氧化碳的化学式是Co | B. | 钠离子的符号为Na+ | ||
| C. | 2O表示两个氧分子 | D. | H2O中含有氢分子 |
18.为探究氢氧化钙溶液和稀盐酸反应后所得溶液中溶质的成分,同学们通过测定反应后溶液的PH,得到了如图1所示的PH曲线,请回答下列问题.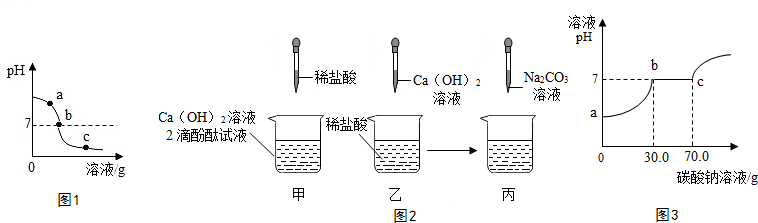
(1)由图1可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,取a、b、c三处反应后的溶液于三个烧杯中,但是忘了做标记,同学们通过设计方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液.
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3═CaCO3↓+2NaCl.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了如表方案:
(4)如图2,同学们做甲、乙、两个中和反应实验的探究.
①甲实验恰好中和,则该溶液中的溶质是CaCl2(化学式).
②取乙反应后的溶液60.0g,滴加质量分数26.5%的Na2CO3溶液,如图2丙,溶液pH的变化如图3,请计算该溶液中CaCl2的溶质质量分数18.5%(写出计算过程,精确到0.1%).
0 147575 147583 147589 147593 147599 147601 147605 147611 147613 147619 147625 147629 147631 147635 147641 147643 147649 147653 147655 147659 147661 147665 147667 147669 147670 147671 147673 147674 147675 147677 147679 147683 147685 147689 147691 147695 147701 147703 147709 147713 147715 147719 147725 147731 147733 147739 147743 147745 147751 147755 147761 147769 211419

(1)由图1可知该实验操作是将稀盐酸滴加到另一种溶液中;
(2)该反应的化学方程式为Ca(OH)2+2HCl═CaCl2+2H2O;
(3)实验过程中,取a、b、c三处反应后的溶液于三个烧杯中,但是忘了做标记,同学们通过设计方案(不再用测定pH的方法),探究三种样品分别属于哪处溶液.
【查阅资料】CaCl2溶液显中性,CaCl2+Na2CO3═CaCO3↓+2NaCl.
【探究过程】
①分别取少量样品于三支试管中,加入酚酞试液,观察到其中一支试管内出现溶液由无色变成红色的现象.结论:该样品是a处溶液.
②为进一步确定b或c处溶液,又设计了如表方案:
| 实验步骤 | 实验现象 | 实验结论 |
| 另取余下样品少量于两支试管中,分别滴加足量的Na2CO3溶液. | 只产生白色沉淀 | 该样品为b处溶液. |
| 先产生气泡,后产生白色沉淀 | 该样品为c处溶液,并推知溶液中的阳离子有Ca2+、H+. |
①甲实验恰好中和,则该溶液中的溶质是CaCl2(化学式).
②取乙反应后的溶液60.0g,滴加质量分数26.5%的Na2CO3溶液,如图2丙,溶液pH的变化如图3,请计算该溶液中CaCl2的溶质质量分数18.5%(写出计算过程,精确到0.1%).