18.为了促进农作物的生长,增强抗旱能力,明明建议施用适量的磷肥,明明父母应选择的化肥是( )
| A. | KCl | B. | CO(NH2)2 | C. | Ca3(PO4)2 | D. | KNO3 |
17.下列实验操作合理的是( )
| A. | 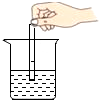 测溶液pH | B. | 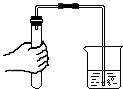 检查装置气密性 | C. | 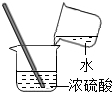 稀释浓硫酸 | D. | 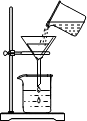 过滤 |
16.下列生活用品中,主要由合成材料制成的是( )
| A. | 真丝手套 | B. | 尼龙背包 | C. | 纯棉毛巾 | D. | 铝镁合金 |
12.如图所示实验操作符合规范的是( )
| A. | 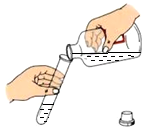 倾倒液体 | B. | 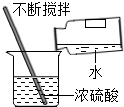 浓硫酸的稀释 | ||
| C. | 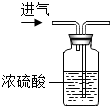 干燥氧气 | D. | 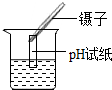 测定某溶液的pH值 |
11.化学小组同学在课外读物中看到:“通常CO2可作灭火剂,但有些物质(如Na)着火,不能用CO2熄灭.”他们决定探究CO2与Na反应的产物.
【提出猜想】CO2与Na反应可能生成4种物质:C、CO、Na2O、Na2CO3.
【查阅资料】
①Na是非常活泼的金属,常温下与O2、H2O等物质反应.
②碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
③Na2O是白色固体,与H2O反应生成NaOH.
④向氯化钯(PdCl2)溶液中通入CO,产生黑色沉淀.
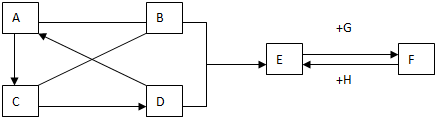
【实验过程】同学们在老师的指导下设计了如下图所示装置(部分夹持仪器已略去)
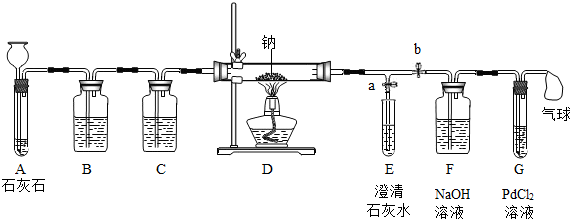
(1)实验记录
(2)实验反思
①实验记录②中,E中出现浑浊,再点燃酒精灯的目的是排出装置中的空气,防止空气的干扰.
②若无装置C,对实验有影响的物质是水.
③检验第4种物质是否存在的实验方案:取D中白色固体于试管中,加水完全溶解,加入过量CaCl2溶液至不再产生沉淀,滴加酚酞试液,溶液呈红色.说明白色固体中含Na2O.
【提出猜想】CO2与Na反应可能生成4种物质:C、CO、Na2O、Na2CO3.
【查阅资料】
①Na是非常活泼的金属,常温下与O2、H2O等物质反应.
②碱性的Na2CO3溶液与中性的CaCl2溶液发生复分解反应.
③Na2O是白色固体,与H2O反应生成NaOH.
④向氯化钯(PdCl2)溶液中通入CO,产生黑色沉淀.
【实验过程】同学们在老师的指导下设计了如下图所示装置(部分夹持仪器已略去)

(1)实验记录
| 序号 | 实验操作 | 主要实验现象 | 实验结论和解释 |
| ① | 打开a,关闭b,由长颈漏斗注入稀盐酸 | A中产生大量气泡 E中出现浑浊 | E中反应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O |
| ② | 当E中出现浑浊时,打开b,关闭a,点燃酒精灯 | D中Na剧烈燃烧,产生白烟内壁附着黑色、白色固体 G中产生黑色沉淀 | 反应产物一定有C和CO |
| ③ | 取D中白色固体于试管中,加水溶解,再加入石灰水 | 产生白色沉淀 | 反应产物还有Na2CO3 |
①实验记录②中,E中出现浑浊,再点燃酒精灯的目的是排出装置中的空气,防止空气的干扰.
②若无装置C,对实验有影响的物质是水.
③检验第4种物质是否存在的实验方案:取D中白色固体于试管中,加水完全溶解,加入过量CaCl2溶液至不再产生沉淀,滴加酚酞试液,溶液呈红色.说明白色固体中含Na2O.
10.某科研所成功利用染化厂的废料铁泥(主要成分是Fe2O3、FeO和铁)制备可用于隐形飞机涂层的纳米四氧化三铁.
(1)在物质分类中,四氧化三铁属于氧化物(填写物质类别).
(2)制备过程中要用到双氧水(过氧化氢溶液),其中双氧水溶液的用量、调节的pH、反应时间是三个关键条件,研究时需要进行七组对比实验.若实验序号1是该制备过程的理论最佳制备条件,请在下表中完善实验序号为7的实验条件(与1-6组实验条件不同).
(3)调节溶液的pH可用碳酸钠或碳酸氢钠.
查阅资料可知:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,此反应的基本类型是分解反应反应,此反应证明NaHCO3的热稳定性小于 Na2CO3(填“大于”或“小于”).
请你根据以上性质设计实验方案鉴别Na2CO3和NaHCO3固体.分别取两种适量固体于两试管中,分别加热,并将可能生成的气体通入澄清石灰水中,如有白色沉淀生成,则该试管中是NaHCO3.
试写出实验方案中另一个化学反应方程式Ca(OH)2+CO2=CaCO3↓+H2O.
(1)在物质分类中,四氧化三铁属于氧化物(填写物质类别).
(2)制备过程中要用到双氧水(过氧化氢溶液),其中双氧水溶液的用量、调节的pH、反应时间是三个关键条件,研究时需要进行七组对比实验.若实验序号1是该制备过程的理论最佳制备条件,请在下表中完善实验序号为7的实验条件(与1-6组实验条件不同).
| 实验序号 | 双氧水溶液(mL) | pH | 反应时间(h) |
| 1 | 6 | 10 | 3 |
| 2 | 5 | 10 | 3 |
| 3 | 6 | 11 | 3 |
| 4 | 6 | 10 | 2 |
| 5 | 7 | 10 | 3 |
| 6 | 6 | 9 | 3 |
| 7 | 6 | 10 | 4(大于3即可) |
查阅资料可知:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,此反应的基本类型是分解反应反应,此反应证明NaHCO3的热稳定性小于 Na2CO3(填“大于”或“小于”).
请你根据以上性质设计实验方案鉴别Na2CO3和NaHCO3固体.分别取两种适量固体于两试管中,分别加热,并将可能生成的气体通入澄清石灰水中,如有白色沉淀生成,则该试管中是NaHCO3.
试写出实验方案中另一个化学反应方程式Ca(OH)2+CO2=CaCO3↓+H2O.
9.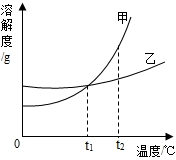 甲、乙两种固体的溶解度曲线如图所示.下列有关叙述中错误的是( )
甲、乙两种固体的溶解度曲线如图所示.下列有关叙述中错误的是( )
0 147520 147528 147534 147538 147544 147546 147550 147556 147558 147564 147570 147574 147576 147580 147586 147588 147594 147598 147600 147604 147606 147610 147612 147614 147615 147616 147618 147619 147620 147622 147624 147628 147630 147634 147636 147640 147646 147648 147654 147658 147660 147664 147670 147676 147678 147684 147688 147690 147696 147700 147706 147714 211419
 甲、乙两种固体的溶解度曲线如图所示.下列有关叙述中错误的是( )
甲、乙两种固体的溶解度曲线如图所示.下列有关叙述中错误的是( )| A. | t2℃时甲的溶解度比乙大 | |
| B. | 将相等质量的甲、乙两物质的饱和溶液温度从t2℃降到t1℃,析出的甲固体质量比乙固体质量大 | |
| C. | 升高温度可将甲的饱和溶液变为不饱和溶液 | |
| D. | t2℃时,甲和乙的饱和溶液各100g,其中溶质的质量相等 |