1.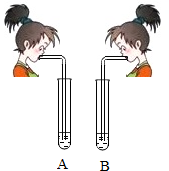 氢氧化钠和氢氧化钙是两种常见的碱.李红同学将两种碱的溶液分别装入试管A、B中,并进行了如图所示的实验.实验中,李红同学向两支试管吹气,A中有白色沉淀生成,发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.B中无现象,此时B中反应的化学方程式为2NaOH+CO2=Na2CO3+H2O,为了探究吹气后B中溶质的成分,李红进行了如下探究.
氢氧化钠和氢氧化钙是两种常见的碱.李红同学将两种碱的溶液分别装入试管A、B中,并进行了如图所示的实验.实验中,李红同学向两支试管吹气,A中有白色沉淀生成,发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.B中无现象,此时B中反应的化学方程式为2NaOH+CO2=Na2CO3+H2O,为了探究吹气后B中溶质的成分,李红进行了如下探究.
【提出猜想】
猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠
…
【实验和结论】
【反思与评价】
老师评价李红得出的结论不正确,是因为猜想2(填数字)成立也会产生相同的现象.如果要验证“猜想3成立”,必需更换试剂,将Ca(OH)2溶液换成CaCl2溶液.
 氢氧化钠和氢氧化钙是两种常见的碱.李红同学将两种碱的溶液分别装入试管A、B中,并进行了如图所示的实验.实验中,李红同学向两支试管吹气,A中有白色沉淀生成,发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.B中无现象,此时B中反应的化学方程式为2NaOH+CO2=Na2CO3+H2O,为了探究吹气后B中溶质的成分,李红进行了如下探究.
氢氧化钠和氢氧化钙是两种常见的碱.李红同学将两种碱的溶液分别装入试管A、B中,并进行了如图所示的实验.实验中,李红同学向两支试管吹气,A中有白色沉淀生成,发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O.B中无现象,此时B中反应的化学方程式为2NaOH+CO2=Na2CO3+H2O,为了探究吹气后B中溶质的成分,李红进行了如下探究.【提出猜想】
猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠
…
【实验和结论】
| 实验 | 实验现象 | 结论 |
| 取B中少量溶液于试管中,向其中加入氢氧化钙溶液至不再产生沉淀为止,过滤后取上层清液,向其中加几滴酚酞试液 | 产生白色沉淀溶液呈现红色 | 猜想3成立 |
老师评价李红得出的结论不正确,是因为猜想2(填数字)成立也会产生相同的现象.如果要验证“猜想3成立”,必需更换试剂,将Ca(OH)2溶液换成CaCl2溶液.
19.酱油是中国的传统调味品,如表是某酱油的部分营养成分列表,根据所学知识回答.
酱油的部分营养成分列表(每100克中含)
(1)表中不含六大基本营养素中的维生素.
(2)表中“钠”、“钙”等是指元素(填“单质”、“分子”、“原子”或“元素”).
(3)老年人每天都要摄入足量的钙,有利于防止骨质疏松.
(4)糖类主要是给人体提供能量.除了糖类,上表中油脂和蛋白质也能给人体提供能量.
(5)人体缺硒可能引起表皮角质化和癌症,但摄入量过高又会使人中毒.这里告诉人们的道理是要均衡膳食.
酱油的部分营养成分列表(每100克中含)
| 成分名称 | 含量 | 成分名称 | 含量 | 成分名称 | 含量 |
| 水分(克) | 54.7 | 蛋白质(克) | 13 | 脂肪(克) | 0.7 |
| 糖类(克) | 10.2 | 钠(毫克) | 7700 | 钙(毫克) | 46 |
| 铁(毫克) | 8.6 | 硒(微克) | 2.96 |
(2)表中“钠”、“钙”等是指元素(填“单质”、“分子”、“原子”或“元素”).
(3)老年人每天都要摄入足量的钙,有利于防止骨质疏松.
(4)糖类主要是给人体提供能量.除了糖类,上表中油脂和蛋白质也能给人体提供能量.
(5)人体缺硒可能引起表皮角质化和癌症,但摄入量过高又会使人中毒.这里告诉人们的道理是要均衡膳食.
18.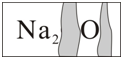 实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里.由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【理论分析】为了确定该溶液,他们首先进行了分析:
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠溶液.乙同学依据碳酸氢钠和硝酸钠的化学式中钠的原子个数为1,而标签中为2,提出,该溶液也不可能是碳酸氢钠、硝酸钠的溶液.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
【实验结论】
(2)该瓶无色溶液的溶质是碳酸钠.生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(3)丙同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
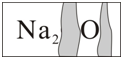 实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里.由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
【理论分析】为了确定该溶液,他们首先进行了分析:
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠溶液.乙同学依据碳酸氢钠和硝酸钠的化学式中钠的原子个数为1,而标签中为2,提出,该溶液也不可能是碳酸氢钠、硝酸钠的溶液.
【设计实验】为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
| 实验操作 | 实验现象 |
| ①取少量该无色溶液于试管中,慢慢滴加BaC12溶液 ②静置后,倾去上层清液,向沉淀中滴加稀盐酸 | 产生白色沉淀 产生大量气泡,沉淀消失. |
(2)该瓶无色溶液的溶质是碳酸钠.生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
【实验反思】
(3)丙同学认为原设计的实验还可简化,同样达到鉴别的目的.丙同学设计的实验如下(将实验操作及实验现象填入相应的空格中):
| 实 验 操 作 | 实 验 现 象 |
| 取上述无色溶液少许于试管中,滴加少量的稀盐酸 | 溶液中有气泡产生 |
12.某学校化学兴趣小组的同学们在实验室发现一瓶石灰水试剂瓶瓶壁和瓶塞周围有一些白色粉末.为了弄清楚白色粉末的成分及形成原因,他们进行了如下探究:
【提出问题】白色粉末成分的猜想和成因分析.
【做出猜想】①可能是CaCO3,原因是石灰水与空气中的CO2反应.
②可能是Ca(OH)2 ,原因是溶剂蒸发,石灰水中的溶质结晶析出.
③还可能是以上二者的混合物.
【实验探究】甲同学取白色粉末于试管中,加少量的水、震荡,发现试管底部有白色固体,于是他得出白色粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是Ca(OH)2微溶于水.
为了得出较严密的结论,他们进行了下表所示实验,请完成实验报告:
由上述实验可知,白色粉末成分的猜想③是正确的.
【拓展反思】
通过上述实验的探究,同学们向实验员提出了保存、使用易变质溶液的下列建议,合理的是ab.
a.密封保存 b.使用前临时配制 c.禁止使用该试剂.
0 147507 147515 147521 147525 147531 147533 147537 147543 147545 147551 147557 147561 147563 147567 147573 147575 147581 147585 147587 147591 147593 147597 147599 147601 147602 147603 147605 147606 147607 147609 147611 147615 147617 147621 147623 147627 147633 147635 147641 147645 147647 147651 147657 147663 147665 147671 147675 147677 147683 147687 147693 147701 211419
【提出问题】白色粉末成分的猜想和成因分析.
【做出猜想】①可能是CaCO3,原因是石灰水与空气中的CO2反应.
②可能是Ca(OH)2 ,原因是溶剂蒸发,石灰水中的溶质结晶析出.
③还可能是以上二者的混合物.
【实验探究】甲同学取白色粉末于试管中,加少量的水、震荡,发现试管底部有白色固体,于是他得出白色粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是Ca(OH)2微溶于水.
为了得出较严密的结论,他们进行了下表所示实验,请完成实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| ①取上述试管中的上层清液,滴加1~2滴酚酞试夜 | 溶液呈红色 | 白色粉末中有氢氧化钙 |
| ②往上述试管残留的白色固体中加入加入稀盐酸 | 有气泡产生 | 白色粉末中含有CaCO3 |
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 |  | 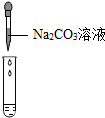 | 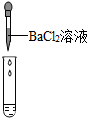 |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【拓展反思】
通过上述实验的探究,同学们向实验员提出了保存、使用易变质溶液的下列建议,合理的是ab.
a.密封保存 b.使用前临时配制 c.禁止使用该试剂.
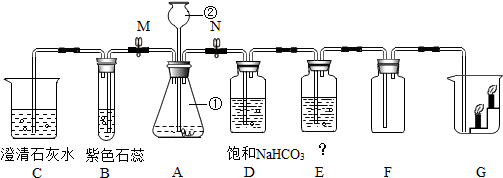
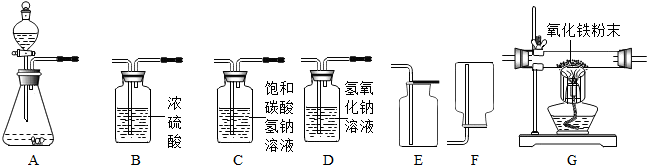
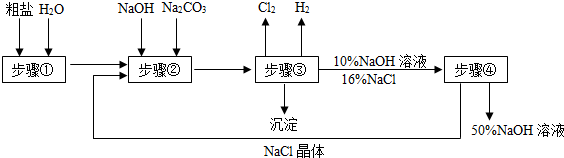
 我国著名化学家侯德邦先生发明的“侯氏制碱法”,不仅使我国制碱工业得到极大进步,而且促进了世界制碱技术.
我国著名化学家侯德邦先生发明的“侯氏制碱法”,不仅使我国制碱工业得到极大进步,而且促进了世界制碱技术.