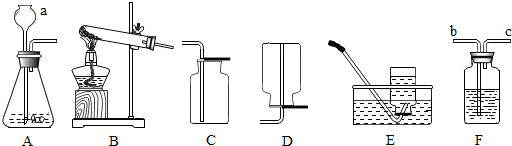
6.关于①、②两组对比实验的说法正确的是( )
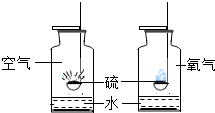
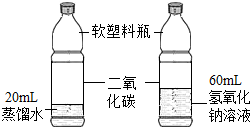
| ①对比硫在空气和氧气中燃烧的剧烈程度 | ②探究二氧化碳能否与氢氧化钠反应 |
 |  |
| A. | 两个实验方案设计均合理 | |
| B. | 实验①中可观察到硫在空气中燃烧发出明亮的蓝紫色火焰 | |
| C. | 实验②中右瓶变瘪的程度更大 | |
| D. | 实验②反应后向右瓶中加入足量稀盐酸,无明显现象 |
5.某化学兴趣小组的同学们学习了纯碱的知识后,对著名的侯氏制碱法产生了浓厚的兴趣,决定对侯氏制碱法进行深入的探究,请你一起参与他们的探究.
【查阅资料】
Ⅰ.侯氏制碱法的原理:
第一步:向饱和食盐水中先通入过量氨气(溶液显碱性),再通入过量的二氧化碳,即可析出NaHCO3固体,反应方程式是:NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl.
第二步:将第一步反应后所得的混合物进行过滤后,将滤渣加热,可生成纯碱、一种能使澄清石灰水变浑浊的气体和一种常见的氧化物.
Ⅱ.已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解得气体体积)
Ⅲ.已知NH4Cl加热条件下易分解,反应的化学方程式是NH4Cl$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+HCl↑
【资料回顾】
(1)第一步中析出NaHCO3固体的原因是相同条件下,碳酸氢钠的溶解度比氯化钠和碳酸钠小,实验中先向饱和食盐水中通入过量氨气,再通入过量的二氧化碳,其原因是①(填序号).
①使CO2更易被吸收 ②NH3比CO2更易制取 ③CO2的密度比NH3大
(2)写出第二步中将滤渣加热发生反应的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)该工业同时可得副产物NH4Cl,它在农业上可作氮肥,写出NH4Cl与熟石灰固体加热的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
【定性探究】
第一步反应所得混合物在第二步过滤后所得滤液中溶质的成分是什么?
【作出猜想】
猜想Ⅰ:NH4Cl
猜想Ⅱ:NH4Cl和NaHCO3
猜想Ⅲ:NH4Cl和NaCl
猜想Ⅳ:NH4Cl、NaCl和NaHCO3.
【设计实验】
【交流讨论】小明同学认为步骤②结论不正确,他的理由是氯化铵能和硝酸银反应生成白色沉淀氯化银.
小张为证明滤液中是否含NaCl,设计了以下方案:另取少量滤液蒸干后充分灼烧,取灼烧后的残余固体溶于水,往其中滴加足量稀HNO3后,再滴加AgNO3溶液,产生白色沉淀.
【得出结论】猜想Ⅳ成立.
【定量探究】
实际生产中得到的纯碱样品中含有少量NaCl,国际上规定纯碱的纯度(即纯碱的质量分数)≥98.0%为合格品,同学们想判断某纯碱样品是否合格,分成四个小组,各取25克该样品全部溶解于水中,向其中加入相同溶质质量分数的CaCl2溶液.四组加入的CaCl2溶液的质量与产生的沉淀的质量关系如表.
(1)通过计算判断该纯碱样品是否是合格品?
(2)若要计算CaCl2溶液的溶质质量分数,可以选择第一、二组数据计算.
【查阅资料】
Ⅰ.侯氏制碱法的原理:
第一步:向饱和食盐水中先通入过量氨气(溶液显碱性),再通入过量的二氧化碳,即可析出NaHCO3固体,反应方程式是:NaCl+CO2+NH3+H2O═NaHCO3↓+NH4Cl.
第二步:将第一步反应后所得的混合物进行过滤后,将滤渣加热,可生成纯碱、一种能使澄清石灰水变浑浊的气体和一种常见的氧化物.
Ⅱ.已知20℃时有关物质的溶解度如下(气体指1体积水中能溶解得气体体积)
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
【资料回顾】
(1)第一步中析出NaHCO3固体的原因是相同条件下,碳酸氢钠的溶解度比氯化钠和碳酸钠小,实验中先向饱和食盐水中通入过量氨气,再通入过量的二氧化碳,其原因是①(填序号).
①使CO2更易被吸收 ②NH3比CO2更易制取 ③CO2的密度比NH3大
(2)写出第二步中将滤渣加热发生反应的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
(3)该工业同时可得副产物NH4Cl,它在农业上可作氮肥,写出NH4Cl与熟石灰固体加热的化学方程式2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑.
【定性探究】
第一步反应所得混合物在第二步过滤后所得滤液中溶质的成分是什么?
【作出猜想】
猜想Ⅰ:NH4Cl
猜想Ⅱ:NH4Cl和NaHCO3
猜想Ⅲ:NH4Cl和NaCl
猜想Ⅳ:NH4Cl、NaCl和NaHCO3.
【设计实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取少量滤液于试管中,滴加稀盐酸 | 产生无色无味气体 | 证明滤液中含有的物质是NaHCO3 |
| ②另取少量滤液于试管中,滴加足量稀HNO3后,再滴加AgNO3溶液 | 产生白色沉淀 | 证明滤液中含有NaCl |
小张为证明滤液中是否含NaCl,设计了以下方案:另取少量滤液蒸干后充分灼烧,取灼烧后的残余固体溶于水,往其中滴加足量稀HNO3后,再滴加AgNO3溶液,产生白色沉淀.
【得出结论】猜想Ⅳ成立.
【定量探究】
实际生产中得到的纯碱样品中含有少量NaCl,国际上规定纯碱的纯度(即纯碱的质量分数)≥98.0%为合格品,同学们想判断某纯碱样品是否合格,分成四个小组,各取25克该样品全部溶解于水中,向其中加入相同溶质质量分数的CaCl2溶液.四组加入的CaCl2溶液的质量与产生的沉淀的质量关系如表.
| 第一组 | 第二组 | 第三组 | 第四组 | |
| CaCl2溶液的质量(克) | 100 | 200 | 300 | 400 |
| 产生沉淀的质量(克) | 8 | 16 | 20 | 20 |
(2)若要计算CaCl2溶液的溶质质量分数,可以选择第一、二组数据计算.
2.下列说法正确的是( )
| A. | 能使无色酚酞试液变红的一定是碱的溶液 | |
| B. | 干电池工作时将化学能转化为电能 | |
| C. | 合金的硬度一般比各成分金属小 | |
| D. | 铝制品比铁制品具有更好的抗腐蚀性能,是因为铝比铁更活泼 |
1.下列对某一主题知识的归纳,均正确的一组是( )
| A.生活常识 | B.物质鉴别 |
| ①用洗洁精去油污--乳化作用 ②人体缺钙元素一一导致甲状腺肿大 | ①食盐与纯碱一一品尝味道 ②硬水与软水一一观察颜色区别 |
| C.安全常识 | D.“一定”与“不一定” |
| ①点燃氢气之前一定要先验纯 ②进入陌生溶洞前--先做灯火试验 | ①有盐和水生成的反应一定是中和反应 ②含氧元素的物质一定是氧化物 |
| A. | A | B. | B | C. | C | D. | D |
20.下列实验现象的描述正确的是( )
| A. | 将二氧化碳通入氧化钙溶液中产生白色沉淀 | |
| B. | 打开浓盐酸的试剂瓶塞,瓶口出现白烟 | |
| C. | 灼烧棉线,产生烧焦羽毛的气味 | |
| D. | 镁条在空气中燃烧,发出耀眼的强光,生成白色固体 |
19.下列有关生产、环保、能源、资源问题叙述错误的是( )
| A. | 25m3的石油液化气加压可装入容积为0.024m3的钢瓶,这是因为分子变小了 | |
| B. | 防止金属腐蚀是保护金属资源的有效途径 | |
| C. | pH<5.6的降水称为酸雨,它的形成与大气中SO2等污染物增多有关 | |
| D. | 提倡城市道路使用太阳能景观路灯 |
18.下列图示的实验操作,正确的是( )
| A. | 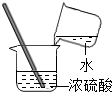 稀释浓硫酸 | B. | 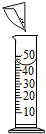 配制氯化钠溶液 | C. | 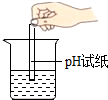 测定溶液pH | D. |  蒸发食盐水 |
17.下列变化中属于化学变化的是( )
0 147258 147266 147272 147276 147282 147284 147288 147294 147296 147302 147308 147312 147314 147318 147324 147326 147332 147336 147338 147342 147344 147348 147350 147352 147353 147354 147356 147357 147358 147360 147362 147366 147368 147372 147374 147378 147384 147386 147392 147396 147398 147402 147408 147414 147416 147422 147426 147428 147434 147438 147444 147452 211419
| A. | 分离液态空气制氧气 | B. | 石蜡受热熔化 | ||
| C. | 浓硫酸使小木条变黑 | D. | 棉线织成布 |