20.检验一瓶久置的NaOH溶液是否变质,下列所用试剂不正确的是( )
| A. | 稀H2SO4 | B. | 酚酞试液 | C. | BaCl2溶液 | D. | Ca(NO3)2溶液 |
19.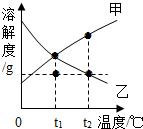 甲、乙两物质的溶解度曲线如图,将等质量的t2℃甲、乙饱和溶液分别降温到t1℃.下列说法一定正确的是( )
甲、乙两物质的溶解度曲线如图,将等质量的t2℃甲、乙饱和溶液分别降温到t1℃.下列说法一定正确的是( )
 甲、乙两物质的溶解度曲线如图,将等质量的t2℃甲、乙饱和溶液分别降温到t1℃.下列说法一定正确的是( )
甲、乙两物质的溶解度曲线如图,将等质量的t2℃甲、乙饱和溶液分别降温到t1℃.下列说法一定正确的是( )| A. | 两溶液仍饱和 | B. | 此时溶解度相等 | ||
| C. | 溶质质量分数:甲=乙 | D. | 溶液质量:甲=乙 |
18.锆(Zr)的一种氧化物是耐高温的新型陶瓷材料.经测定锆的相对原子质量为91,其氯化物的相对分子质量为233.若锆在氯化物和这种氧化物中的化合价相同,则该氧化物的化学式为( )
| A. | Zr2O | B. | ZrO | C. | Zr2O3 | D. | ZrO2 |
17.下列物质中,能使鸡蛋清溶液发生盐析的是( )
| A. | 甲醛 | B. | 浓硝酸 | C. | 饱和硫酸铵溶液 | D. | 醋酸铅 |
16.在不用酸碱指示剂的情况下,某兴趣小组的同学做完氢氧化钠与稀硫酸的中和反应实验后,对所得溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究.
【提出问题】溶液中的溶质有哪些物质?
【作出猜想】甲、乙、丙、丁四位同学分别作出了如下猜想:
甲同学:溶液中的溶质只有Na2SO4一种物质.
乙同学:溶液中的溶质有Na2SO4和硫酸两种物质.
丙同学:溶液中的溶质有Na2SO4和NaOH两种物质.
丁同学:溶液中的溶质有Na2SO4、NaOH和H2SO4三种物质.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和另外一种物质.
【实验验证】
【交流讨论】(1)戊同学根据所学化学知识和乙、丙两同学的实验现象,首先肯定甲、丁两同学的猜想都不成立,戊同学认为丁同学的猜想不成立的理由是NaOH和H2SO4因能发生反应,不能同时存在.经过进一步分析,戊同学认为乙同学的猜想也不成立,他的理由又是滴入酚酞试液后,溶液变红色,说明溶液呈碱性,溶液中不可能含有硫酸.该兴趣小组的同学经过充分讨论,一致认为丙同学的猜想成立.
(2)乙同学实验中铝片一定要反复打磨,除去表面的致密的保护膜,否则干扰实验现象和结论.
【总结反思】(1)在分析反应后所得物质的成分时,除考虑生成物外,还要考虑反应物是否有剩余.
(2)做氢氧化钠与稀硫酸反应实验时,可先向氢氧化钠溶液中逐滴滴加稀硫酸,边滴加
边振荡,然后用PH试纸(多次)测定反应后溶液的pH,当pH为7时停止滴加稀硫酸,就可控制反应后溶液中的溶质只有Na2SO4.用PH试纸测定溶液pH的方法是用玻璃棒蘸取溶液滴在PH试纸上,把试纸呈现的颜色与标准比色卡对照.
【拓展提高】(1)生活中能否用铝制品来盛放强碱性溶液?不能(选填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液中的溶质和溶剂共同发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
【提出问题】溶液中的溶质有哪些物质?
【作出猜想】甲、乙、丙、丁四位同学分别作出了如下猜想:
甲同学:溶液中的溶质只有Na2SO4一种物质.
乙同学:溶液中的溶质有Na2SO4和硫酸两种物质.
丙同学:溶液中的溶质有Na2SO4和NaOH两种物质.
丁同学:溶液中的溶质有Na2SO4、NaOH和H2SO4三种物质.
【查阅资料】①Na2SO4溶液显中性.
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和另外一种物质.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 | |
| 乙同学 实验 | 取中和反应后的溶液少许于试管中,将表面反复打磨后的铝片放入试管内的溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 乙同学 猜想成立 |
| 丙同学 实验 | 取中和反应后的溶液少许于试管中,向试管内滴加几滴无色酚酞试液 | 无色溶液变成红色 | 丙同学 猜想成立 |
(2)乙同学实验中铝片一定要反复打磨,除去表面的致密的保护膜,否则干扰实验现象和结论.
【总结反思】(1)在分析反应后所得物质的成分时,除考虑生成物外,还要考虑反应物是否有剩余.
(2)做氢氧化钠与稀硫酸反应实验时,可先向氢氧化钠溶液中逐滴滴加稀硫酸,边滴加
边振荡,然后用PH试纸(多次)测定反应后溶液的pH,当pH为7时停止滴加稀硫酸,就可控制反应后溶液中的溶质只有Na2SO4.用PH试纸测定溶液pH的方法是用玻璃棒蘸取溶液滴在PH试纸上,把试纸呈现的颜色与标准比色卡对照.
【拓展提高】(1)生活中能否用铝制品来盛放强碱性溶液?不能(选填“能”或“不能”)
(2)乙同学的实验中铝片与氢氧化钠溶液发生了反应,请写出铝与该溶液中的溶质和溶剂共同发生反应的化学方程式2Al+2NaOH+2H2O═2NaAlO2+3H2↑.
11.下列图象不能正确反映其对应操作中各量变化关系的是( )
0 147158 147166 147172 147176 147182 147184 147188 147194 147196 147202 147208 147212 147214 147218 147224 147226 147232 147236 147238 147242 147244 147248 147250 147252 147253 147254 147256 147257 147258 147260 147262 147266 147268 147272 147274 147278 147284 147286 147292 147296 147298 147302 147308 147314 147316 147322 147326 147328 147334 147338 147344 147352 211419
| A. | 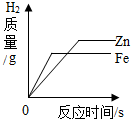 向等质量的形状相同的锌片、铁片分别加入足量的等质量分数的稀硫酸 | |
| B. | 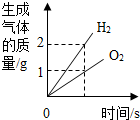 电解水 | |
| C. | 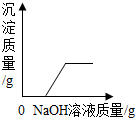 向氯化铁和盐酸的混合溶液中加入过量的氢氧化钠溶液 | |
| D. | 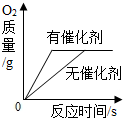 用两份相同质量相同质量分数的过氧化氢溶液制取氧气 |
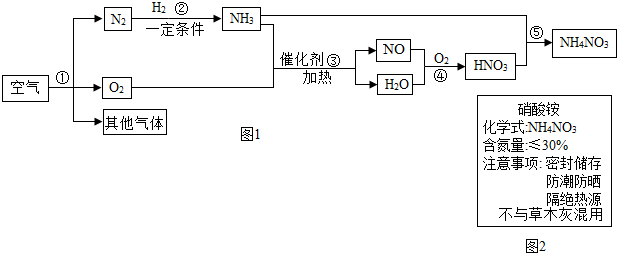
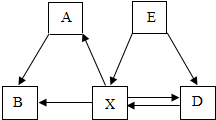 初中化学中几种常见物质之间的相互转化关系如图所示(每个字母各代表一种物质,每个箭头表示一个转换关系,部分反应物、生成物及反应条件略去)已知常温下B为气体,是植物进行光合作用的一种重要原料;D和E常温下均为无
初中化学中几种常见物质之间的相互转化关系如图所示(每个字母各代表一种物质,每个箭头表示一个转换关系,部分反应物、生成物及反应条件略去)已知常温下B为气体,是植物进行光合作用的一种重要原料;D和E常温下均为无