2.实验设计是化学实验的重要环节,用对比实验方法探究二氧化碳的性质,请根据下列实验要求回答相关问题,
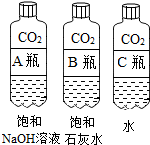
【实验一】振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O;对比A瓶与C(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
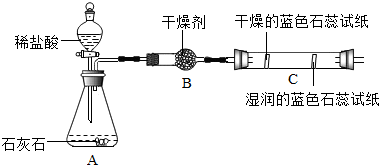
【实验二】观察到C装置中发生的现象是干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色,结论是CO2+H2O=H2CO3(用化学方程式表示).
| 实验一 | 实验二 |
 |  |
【实验二】观察到C装置中发生的现象是干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色,结论是CO2+H2O=H2CO3(用化学方程式表示).
18.从化学的视角认识下列食物中国富含蛋白质的是( )
| A. |  米饭 | B. |  西红柿 | C. |  牛肉 | D. |  花生油 |
17.下列物质中属于纯净物的是( )
| A. | 液氧 | B. | 生铁 | C. | 杨梅酒 | D. | 铅笔芯 |
16.“水是生命之源”,下列关于水的说法正确的是( )
| A. | 水是有机物,能赋予生命 | |
| B. | 水是一种极好的溶剂,能维持人体的体液平衡 | |
| C. | 水分解可以得到氢气,因此水是廉价且清洁的能源物质 | |
| D. | 水中氧元素含量很高,能提供人体所需的氧气 |
15.(1)碳酸钠是玻璃、造纸、肥皂、洗涤剂、纺织、制革等工业的重要原料,它属于盐(填“酸”、“碱”或“盐”).
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑,
制取和收集氨气可用如图中的AD装置.

(3)实验室常用石灰石和稀盐酸制取二氧化碳气体,发生装置可选择图中的B(填仪器字母),反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(4)实验室用B装置制取氧气,反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(5)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
请你据此分析计算:
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)
0 147088 147096 147102 147106 147112 147114 147118 147124 147126 147132 147138 147142 147144 147148 147154 147156 147162 147166 147168 147172 147174 147178 147180 147182 147183 147184 147186 147187 147188 147190 147192 147196 147198 147202 147204 147208 147214 147216 147222 147226 147228 147232 147238 147244 147246 147252 147256 147258 147264 147268 147274 147282 211419
(2)无水碳酸钠的工业制法主要有氨碱法和联合制碱法两种.氨碱法即以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气(极易溶于水)为原料来制取纯碱.工业上是用N2和H2在高温、高压和催化剂条件下合成氨的.实验室一般用氯化铵和消石灰共热来制备少量的氨气,该反应的化学方程式为2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2H2O+2NH3↑,
制取和收集氨气可用如图中的AD装置.

(3)实验室常用石灰石和稀盐酸制取二氧化碳气体,发生装置可选择图中的B(填仪器字母),反应的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑.
(4)实验室用B装置制取氧气,反应的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(5)某海洋化工集团用氨碱法生产的纯碱产品中含有少量氯化钠杂质,其产品包装袋上注明:碳酸钠≥96%.为测定该产品中含碳酸钠的质量分数,进行了以下实验,取11.0g纯碱样品放入烧杯中,称得烧杯及所盛纯碱样品的总质量为158.0g,再把100g稀盐酸平均分成四份依次加入样品中,每次均充分反应.实验数据记录如下:
| 所加盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及所盛物质的总质量/g | 181.2 | 204.4 | 228.6 | 253.6 |
①第一次加入稀盐酸充分反应后,生成二氧化碳的质量是1.8g.
②该产品中碳酸钠的质量分数是否合格?(要求写出计算过程,结果精确到0.1%)