11.下列鉴别物质的方法中,切实可行的是( )
| A. | 用酚酞试液鉴别氯化钠溶液和盐酸 | |
| B. | 用酚酞试液鉴别氢氧化钠溶液和碳酸钠溶液 | |
| C. | 用水鉴别碳酸钙和氧化钙 | |
| D. | 用碳酸钠溶液鉴别Ca(OH)2和BaCl2溶液 |
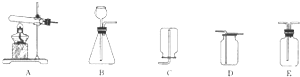
10.碳酸镁晶须(MgCO3•nH2O,n=1~5的整数)广泛应用于冶金、耐火材料及化工产品等领域.为测定碳酸镁晶须中n的值,学习小组设计了如图1装置并进行了3次实验:(不考虑稀盐酸挥发)

【查阅资料】:
a、碳酸镁晶须受热分解,生成3种氧化物;碱石灰是氢氧化钠和生石灰的混合物.
b、相对分子质量:[Mr(MgCO3):84、Mr(H2O):18、Mr(MgO):40、Mr(CO2):44]
【实验步骤】
①检验装置的气密性;②准确称取3.45g MgCO3•nH2O放在B装置中,连接仪器;
③打开弹簧夹a,鼓入一段时间空气,称量C装置的质量;
④关闭弹簧夹a,打开分液漏斗活塞,缓缓滴入稀盐酸至不再产生气体,关闭分液漏斗活塞;
⑤打开弹簧夹a,缓缓鼓入空气;
⑥准确称量C装置的质量(如表);
⑦重复上述步骤;
⑧根据数据进行计算.
【实验分析及数据处理】
(1)A装置中盛放的溶液是NaOH(浓)溶液,其目的是除去空气中的CO2防止干扰实验
(2)D装置的作用是防止空气中的CO2进入C装置,造成误差;
(3)计算碳酸镁晶须中的n值:(要有计算过程)
【实验反思】
(4)实验结果与理论值有偏差,可以在B、C增加一个除去氯化氢气体的装置可以减少误差;
(5)下列选项中,会造成CO2测定结果偏大的是①⑤;偏小的是②③④;
①反应结束后,没有通空气; ②称量C装置前,没有通空气;
③没有A装置; ④没有D装置;
⑤稀盐酸滴加速率太快; ⑥C装置中NaOH溶液浓度过大;
(6)为精确测定n的值,在老师指导下,小组同学称取13.8g MgCO3•nH2O进行热数据分析,并绘制
出如图2所示的热重曲线示意图.则:
①t2℃时,剩余固体为MgCO3•H2O(填化学式);
②最终剩余的4.0g物质是MgO(填化学式);
③MgCO3•nH2O完全分解的化学方程式为:MgCO3•3H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgO+3H2O+CO2.

【查阅资料】:
a、碳酸镁晶须受热分解,生成3种氧化物;碱石灰是氢氧化钠和生石灰的混合物.
b、相对分子质量:[Mr(MgCO3):84、Mr(H2O):18、Mr(MgO):40、Mr(CO2):44]
【实验步骤】
①检验装置的气密性;②准确称取3.45g MgCO3•nH2O放在B装置中,连接仪器;
③打开弹簧夹a,鼓入一段时间空气,称量C装置的质量;
④关闭弹簧夹a,打开分液漏斗活塞,缓缓滴入稀盐酸至不再产生气体,关闭分液漏斗活塞;
⑤打开弹簧夹a,缓缓鼓入空气;
| 编 号 | 1 | 2 | 3 |
| 实验前 | 228.00 | 228.00 | 228.00 |
| 实验后 | 229.10 | 229.11 | 229.09 |
⑦重复上述步骤;
⑧根据数据进行计算.
【实验分析及数据处理】
(1)A装置中盛放的溶液是NaOH(浓)溶液,其目的是除去空气中的CO2防止干扰实验
(2)D装置的作用是防止空气中的CO2进入C装置,造成误差;
(3)计算碳酸镁晶须中的n值:(要有计算过程)
【实验反思】
(4)实验结果与理论值有偏差,可以在B、C增加一个除去氯化氢气体的装置可以减少误差;
(5)下列选项中,会造成CO2测定结果偏大的是①⑤;偏小的是②③④;
①反应结束后,没有通空气; ②称量C装置前,没有通空气;
③没有A装置; ④没有D装置;
⑤稀盐酸滴加速率太快; ⑥C装置中NaOH溶液浓度过大;
(6)为精确测定n的值,在老师指导下,小组同学称取13.8g MgCO3•nH2O进行热数据分析,并绘制
出如图2所示的热重曲线示意图.则:
①t2℃时,剩余固体为MgCO3•H2O(填化学式);
②最终剩余的4.0g物质是MgO(填化学式);
③MgCO3•nH2O完全分解的化学方程式为:MgCO3•3H2O$\frac{\underline{\;\;△\;\;}}{\;}$MgO+3H2O+CO2.
8.下列关于物质的检验方法正确的是( )
| A. | 用硫酸铜溶液鉴别氢氧化钠和碳酸钠溶液 | |
| B. | 用紫色石蕊试液测定雨水的酸碱度 | |
| C. | 往固体中加入稀盐酸,出现气泡说明该固体一定是碳酸盐 | |
| D. | 只用酚酞试液就能将氯化钠溶液、氢氧化钠溶液、盐酸区别开来 |
5.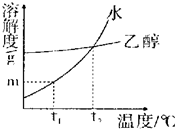 固体物质X在水、乙醇两种溶剂中的溶解度随温度变化的曲线如图所示.下列说法不正确的是( )
固体物质X在水、乙醇两种溶剂中的溶解度随温度变化的曲线如图所示.下列说法不正确的是( )
 固体物质X在水、乙醇两种溶剂中的溶解度随温度变化的曲线如图所示.下列说法不正确的是( )
固体物质X在水、乙醇两种溶剂中的溶解度随温度变化的曲线如图所示.下列说法不正确的是( )| A. | 在水和乙醇中物质X的溶解度都随温度上升高而增大 | |
| B. | t1℃时,物质X在水中的溶解度为mg | |
| C. | t2℃时物质X的水溶液降温至t1℃有晶体析出 | |
| D. | t2℃时,物质X在水中与在乙醇中的溶解度相同 |
3.(1)有S、H、O、Fe四种元素,请选用这四种元素中的一种或几种写出相应的化学式:
(2)用上表的四种具体物质,写一个符合下列要求的化学方程式:复分解反应2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O(合理即可).
0 147079 147087 147093 147097 147103 147105 147109 147115 147117 147123 147129 147133 147135 147139 147145 147147 147153 147157 147159 147163 147165 147169 147171 147173 147174 147175 147177 147178 147179 147181 147183 147187 147189 147193 147195 147199 147205 147207 147213 147217 147219 147223 147229 147235 147237 147243 147247 147249 147255 147259 147265 147273 211419
| 类 别 | 单 质 | 酸 | 碱 | 盐 |
| 化学式 | Fe | H2SO4 | Fe(OH)3 | FeSO4 |
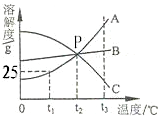 如图是 A、B、C三种固体物质(均不含结晶水)的溶解度曲线,根据图示回答:
如图是 A、B、C三种固体物质(均不含结晶水)的溶解度曲线,根据图示回答: