4.下列说法正确的是( )
| A. | 铝是地壳中含量最多的金属元素 | |
| B. | 不锈钢就是永不生锈的钢 | |
| C. | 生铁可以完全溶解在足量的稀盐酸中 | |
| D. | 油罐车的尾部常有一条铁链拖到地面上,这是利用了铁的导热性 |
3.某化学实验活动小组的同学为了探究实验室中久置氢氧化钠固体的成分,进行了有关实验,请你参与他们进行的探究活动:
【猜想与假设】
猜想Ⅰ:全部是NaOH;
猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:NaOH、Na2CO3.
【实验探究】
(1)实验如下:
(2)为了进一步的验证猜想结果,小明同学提出了如下实验方案:鸡血步骤二的实验,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立.
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈碱性(填“酸”或“碱”)能使酚酞变红,因此,他认为该方案的操作步骤中应该改进的是继续滴加氯化钡溶液至过量,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立.
(3)实验小组的同学展开讨论,又提出了一个定量试验方案,通过测定产生沉淀的质量来证明猜想Ⅱ或Ⅲ成立.试验如下:准确称量m克固体样品中于试管中,加热蒸馏水完全溶解,然后滴加足量氯化钡溶液,充分反应后过滤、洗涤、干燥称的沉淀的质量为n克,若猜想Ⅲ成立,则m与n的关系式为(用含m和n的等式或不等式表示)$\frac{106}{197}$n<m.
【反思与交流】久置固体氢氧化钠变质的原因是(用化学方程式表示)2NaOH+CO2═Na2CO3+H2O.
【猜想与假设】
猜想Ⅰ:全部是NaOH;
猜想Ⅱ:全部是Na2CO3;
猜想Ⅲ:NaOH、Na2CO3.
【实验探究】
(1)实验如下:
| 实验操作步骤 | 实验现象 | 结论及解释 |
| 步骤一:取少量固体样品于试中,加蒸馏水完全溶解,然后加入足量的稀盐酸 | 实验过程中始终没有气泡产生 | 则证明猜想Ⅰ成立 |
| 步骤二:取少量固体样品于试管中,加蒸馏水完全溶解,然后滴加氢氧化钡溶液. | 实验过程中产生白色沉淀 | 则证明猜想Ⅱ或Ⅲ成立,此过程中发生反应的化学方程式BaCl2+Na2CO3═BaCO3↓+2NaCl. |
小华同学立即对小明同学的方案提出了质疑,通过查阅资料知道,氯化钡溶液呈中性,不能使无色酚酞试液变红,但碳酸钠溶液呈碱性(填“酸”或“碱”)能使酚酞变红,因此,他认为该方案的操作步骤中应该改进的是继续滴加氯化钡溶液至过量,过滤,然后向滤液中滴加无色酚酞试液,若酚酞变红,则猜想Ⅲ成立;若酚酞不变红,则猜想Ⅱ成立.
(3)实验小组的同学展开讨论,又提出了一个定量试验方案,通过测定产生沉淀的质量来证明猜想Ⅱ或Ⅲ成立.试验如下:准确称量m克固体样品中于试管中,加热蒸馏水完全溶解,然后滴加足量氯化钡溶液,充分反应后过滤、洗涤、干燥称的沉淀的质量为n克,若猜想Ⅲ成立,则m与n的关系式为(用含m和n的等式或不等式表示)$\frac{106}{197}$n<m.
【反思与交流】久置固体氢氧化钠变质的原因是(用化学方程式表示)2NaOH+CO2═Na2CO3+H2O.
2.下列关于化学方程式:C2H6O+3O2$\frac{\underline{\;点燃\;}}{\;}$3H2O+2CO2的认识,错误的是( )
| A. | 定性上,乙醇具有可燃性 | |
| B. | 微观上,参加反应的乙醇分子和氧分子的个数比为1:3 | |
| C. | 宏观上,点燃条件下乙醇与氧气完全反应生成水和二氧化碳 | |
| D. | 定量上,每46g乙醇和32g氧气完全反应生成54g水和88g二氧化碳 |
1.某物质的分子模型如图所示,下列说法错误的是( )
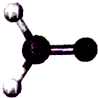

| A. | 该物质属于有机物 | B. | 该物质的化学为CH2O | ||
| C. | 该物质的1个分子中含4个原子 | D. | 氢元素的质量分数=1/30×100% |
20.某化学兴趣小组设计的下列实验方案中,错误的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 区别羊毛和棉花 | 燃烧法 |
| B | 除去HCl气体中少量的CO2 | 通过生石灰 |
| C | NaOH固体中混有少量CaCO3 | 加入足量的水、溶解、过滤、蒸干 |
| D | 验证NaCl溶液中混有盐酸 | 取少量溶液,滴加紫色石蕊溶液 |
| A. | A | B. | B | C. | C | D. | D |
19.下列物质的用途与性质对应关系错误的是( )
| A. | 熟石灰能与酸反应-改良酸性土壤 | |
| B. | 二氧化碳可溶于水-二氧化碳可用于人工降雨 | |
| C. | 氢氧化钠固体易潮解-可用作干燥剂 | |
| D. | 活性炭具有吸附剂-用于除去异味 |
18.化学与生活联系非常紧密,下列做法错误的是( )
| A. | 合理使用化肥、农药能增加农产物产量 | |
| B. | 用甲醛溶液浸泡海产品,以期保质保鲜 | |
| C. | 多吃水果蔬菜可补充人体需要的维生素 | |
| D. | 食用加碘盐可预防大脖子病 |
16.以下是某研究小组探究影响反应速率部分因素的相关实验数据.
(1)写出上述反应产生氧气的文字表达式过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,该反应的类型为分解反应.
(2)从实验①和②对比可得出,化学反应的速率与反应物的浓度有关.从微观上看,化学反应的实质是微观粒子相互接触、相互碰撞的结果,化学反应速率与微观粒子的概率有关.试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是:反应物浓度越大,单位体积的反应物中含有的粒子数越多,粒子间碰撞的概率越大,化学反应速率越快.
(3)用一定量20%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,但产生氧气的总重量不变(选填“减小”或“增大”或“不变”).
(4)【继续探究】除了上面探究过的影响过氧化氢化学反应速率的因素外,还有哪些因素会影响过氧化氢反应的速率?请你提出假设并设计实验进行探究.
0 147038 147046 147052 147056 147062 147064 147068 147074 147076 147082 147088 147092 147094 147098 147104 147106 147112 147116 147118 147122 147124 147128 147130 147132 147133 147134 147136 147137 147138 147140 147142 147146 147148 147152 147154 147158 147164 147166 147172 147176 147178 147182 147188 147194 147196 147202 147206 147208 147214 147218 147224 147232 211419
| 实验序号 | 过氧化氢溶液浓度% | 过氧化氢溶液体积/mL | 温度℃ | 二氧化锰的用量/g | 收集氧气的体积/mL | 反应所需 的时间/s |
| ① | 5 | 1 | 20 | 0.1 | 4 | 16 |
| ② | 15 | 1 | 20 | 0.1 | 4 | 6 |
| ③ | 20 | 5 | 35 | 0 | 2 | 48 |
| ④ | 20 | 5 | 55 | 0 | 2 | 12 |
(2)从实验①和②对比可得出,化学反应的速率与反应物的浓度有关.从微观上看,化学反应的实质是微观粒子相互接触、相互碰撞的结果,化学反应速率与微观粒子的概率有关.试从微观角度解释“反应物浓度越大,化学反应速率越快”的原因是:反应物浓度越大,单位体积的反应物中含有的粒子数越多,粒子间碰撞的概率越大,化学反应速率越快.
(3)用一定量20%的过氧化氢溶液制氧气,为了减小反应速率,可加适量的水稀释,但产生氧气的总重量不变(选填“减小”或“增大”或“不变”).
(4)【继续探究】除了上面探究过的影响过氧化氢化学反应速率的因素外,还有哪些因素会影响过氧化氢反应的速率?请你提出假设并设计实验进行探究.

