14.下列净化水的措施中,能将硬水转化为软水的是( )
| A. | 蒸馏 | B. | 过滤 | C. | 吸附 | D. | 沉淀 |
13.下列图示的实验操作中,正确的是( )
| A. |  塞进橡皮塞 | B. |  称取一定质量的食盐 | ||
| C. |  向试管中滴加液体 | D. |  检查装置气密性 |
11.下列物质的用途和性质对应错误的是( )
| A. | 浓硫酸做干燥剂:浓硫酸具有吸水性 | |
| B. | 氧气可用于炼钢:氧气具有可燃性 | |
| C. | 二氧化碳可用于灭火:二氧化碳不支持燃烧 | |
| D. | 氢氧化铝可用于治疗胃酸过多症:氢氧化铝具有碱性可与胃酸发生中和反应 |
10.下列变化中,属于化学变化的是( )
| A. | 海水蒸发晒盐 | B. | 冰雪融化成水 | C. | 生铁百炼成钢 | D. | 烧碱吸水潮解 |
9.白云石粉是一种生产高级玻璃器皿、医药用瓶、光学玻璃的原料,某化学兴趣小组对白云石粉极其好奇,决定对其进行探究.
【查阅资料】白云石属于碳酸盐矿物,白云石粉主要成分的化学式可表示为:xMgCO3•yCaCO3.( 杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
一.定性探究:白云石粉的成分和性质

【实验分析】
(1)过滤操作中用到的玻璃仪器有玻璃棒、烧杯、漏斗.
(2)由步骤①②的现象可得出白云石粉中一定含有的离子是CO32-(填离子符号).
(3)步骤③生成氢氧化镁的化学方程式是MgCl2+2NaOH═Mg(OH)2↓+2NaCl.步骤④的反应现象是产生白色沉淀.
【结论】综合上述实验现象可初步证明白云石由碳酸钙、碳酸镁组成.
[实验质疑】小组同学经过讨论认为:因氢氧化钙微溶于水,导致沉淀B中除了氢氧化镁之外应该还混有氢氧化钙,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究.
二.定量探究:白云石的组成
[查阅资料】碳酸钙开始分解的温度为898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸钙与碳酸镁的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解.
【实验设计】为测定白云石中的含钙量及x:y的值,该兴趣小组设计了如下装置并进行实验:

【实验步骤】①组装仪器,检查装置的气密性;②准确称取15.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量B、C、D装置的质量;③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量;⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量.
实验数据记录如表:
【实验分析和数据处理】
(4)装置D的作用是吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小;
(5)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是使残留在装置内的二氧化碳气体全部被C装置吸收.
(6)计算白云石中钙元素的质量分数.(写出计算过程,结果保留小数点后一位):
(7)设计实验证明白云石粉已完全分解的实验方法是取少量反应后固体于试管中,加入足量的稀盐酸,无气泡产生,说明完全分解(写出实验方法、现象、结论)
(8)白云石(xMgCO3•yCaCO3)中的 x:y=1:2(最简整数比),若加热前没有鼓入一段时间的氮气,将会导致x:y的值偏大(填偏大、偏小或不变).
【查阅资料】白云石属于碳酸盐矿物,白云石粉主要成分的化学式可表示为:xMgCO3•yCaCO3.( 杂质是二氧化硅,其不溶于水,也不与盐酸反应,受热不分解)
一.定性探究:白云石粉的成分和性质

【实验分析】
(1)过滤操作中用到的玻璃仪器有玻璃棒、烧杯、漏斗.
(2)由步骤①②的现象可得出白云石粉中一定含有的离子是CO32-(填离子符号).
(3)步骤③生成氢氧化镁的化学方程式是MgCl2+2NaOH═Mg(OH)2↓+2NaCl.步骤④的反应现象是产生白色沉淀.
【结论】综合上述实验现象可初步证明白云石由碳酸钙、碳酸镁组成.
[实验质疑】小组同学经过讨论认为:因氢氧化钙微溶于水,导致沉淀B中除了氢氧化镁之外应该还混有氢氧化钙,对定量测定白云石粉的组成干扰较大,在老师的指导下该兴趣小组采用热分解法进行定量探究.
二.定量探究:白云石的组成
[查阅资料】碳酸钙开始分解的温度为898℃,1000℃时完全分解生成生石灰和二氧化碳气体;碳酸钙与碳酸镁的化学性质相似;碳酸镁开始分解的温度为540℃,700℃时完全分解.
【实验设计】为测定白云石中的含钙量及x:y的值,该兴趣小组设计了如下装置并进行实验:

【实验步骤】①组装仪器,检查装置的气密性;②准确称取15.0g 白云石粉末放在A装置中,打开弹簧夹,鼓入一段时间氮气,称量B、C、D装置的质量;③关闭弹簧夹,打开控温电加热器,缓缓调升温度至700℃,持续加热至固体质量不变;④打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量;⑤关闭弹簧夹,调升温度至1000℃,持续加热至固体质量不变,打开弹簧夹,缓缓鼓入一段时间氮气,准确称量B、C、D装置的质量.
实验数据记录如表:
| B中溶液质量/g | C中溶液质量/g | D中溶液质量/g | |
| 反应前 | 50.0 | 100.0 | 50.0 |
| 700℃ | 50.0 | 102.1 | 50.1 |
| 1000℃ | 50.0 | 106.3 | 50.3 |
(4)装置D的作用是吸收氮气带出的水蒸气,防止测得二氧化碳的质量偏小;
(5)持续加热至固体质量不变后缓缓鼓入一段时间氮气的目的是使残留在装置内的二氧化碳气体全部被C装置吸收.
(6)计算白云石中钙元素的质量分数.(写出计算过程,结果保留小数点后一位):
(7)设计实验证明白云石粉已完全分解的实验方法是取少量反应后固体于试管中,加入足量的稀盐酸,无气泡产生,说明完全分解(写出实验方法、现象、结论)
(8)白云石(xMgCO3•yCaCO3)中的 x:y=1:2(最简整数比),若加热前没有鼓入一段时间的氮气,将会导致x:y的值偏大(填偏大、偏小或不变).
7.某实验小组的同学用氢氧化钠溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂.此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质的成分进行探究.
(1)写出该中和反应的化学方程式NaOH+HCl═NaCl+H2O.
(2)探究烧杯内溶液中溶质的成分:
【提出问题】该烧杯内的溶液中溶质成分是什么?
【进行猜想】(A)溶质可能只是NaCl与NaOH
(B)溶质可能只是NaCl
(C)溶质可能是NaCl与HCl
【实验探究】上述猜想中都有NaCl,理由是氯化钠是生成物.
①小明从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴紫色石蕊试液,发现溶液变红.
②小华选用两种不同于小明方法也得到相同的结论,请你帮他完成实验,填写一下表格:
【实验结论】通过以上探究,猜想C正确.
【反思与拓展】小明提出小华的实验方案二中有错误,错误的原因是氯化钠和硝酸银反应,也能产生氯化银白色沉淀,不能证明一定含有氯化氢.
(1)写出该中和反应的化学方程式NaOH+HCl═NaCl+H2O.
(2)探究烧杯内溶液中溶质的成分:
【提出问题】该烧杯内的溶液中溶质成分是什么?
【进行猜想】(A)溶质可能只是NaCl与NaOH
(B)溶质可能只是NaCl
(C)溶质可能是NaCl与HCl
【实验探究】上述猜想中都有NaCl,理由是氯化钠是生成物.
①小明从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴紫色石蕊试液,发现溶液变红.
②小华选用两种不同于小明方法也得到相同的结论,请你帮他完成实验,填写一下表格:
| 实验方案 | 预计现象 |
| 方案一: 取少量反应后溶液于试管中,加入铁粉 | 有气泡产生,溶液由无色变为浅绿色 |
| 方案二:取少量反应后溶液于试管中,逐滴加入硝酸银溶液 | 有白色沉淀产生 |
【反思与拓展】小明提出小华的实验方案二中有错误,错误的原因是氯化钠和硝酸银反应,也能产生氯化银白色沉淀,不能证明一定含有氯化氢.
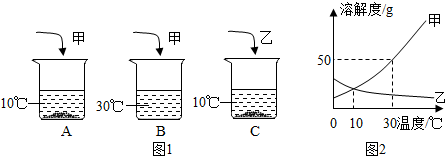
5.A、B、C三个烧杯中盛有相同质量的水,分别加入甲、乙两物质各10g(如图是甲、乙两种物质的溶解度曲线图),充分溶解后的情况如图所示,下列说法中正确的是( )
0 147016 147024 147030 147034 147040 147042 147046 147052 147054 147060 147066 147070 147072 147076 147082 147084 147090 147094 147096 147100 147102 147106 147108 147110 147111 147112 147114 147115 147116 147118 147120 147124 147126 147130 147132 147136 147142 147144 147150 147154 147156 147160 147166 147172 147174 147180 147184 147186 147192 147196 147202 147210 211419

| A. | A、C烧杯中溶质质量分数一定相等 | |
| B. | B烧杯中的溶液一定是不饱和溶液 | |
| C. | C烧杯中溶液的溶质质量分数一定为10% | |
| D. | 升温后A、C两种溶液均可变为不饱和溶液 |





