1.金属材料在人类活动中已得到越来越广泛的应用,下列材料属于金属共性的是( )
| A. | 有良好的导电性、导热性 | B. | 密度较大,熔点较低 | ||
| C. | 是银白色的固体 | D. | 都是混合物 |
19.在实验室中,不能用磨口玻璃塞的玻璃试剂瓶盛装氢氧化钠溶液,因为氢氧化钠会与玻璃成分中的某种物质X发生化学反应,使玻璃塞和玻璃试剂瓶口粘连在一起,其反应的化学方程式为:X+2NaOH═Na2SiO3+H2O,则X的化学式为( )
0 146846 146854 146860 146864 146870 146872 146876 146882 146884 146890 146896 146900 146902 146906 146912 146914 146920 146924 146926 146930 146932 146936 146938 146940 146941 146942 146944 146945 146946 146948 146950 146954 146956 146960 146962 146966 146972 146974 146980 146984 146986 146990 146996 147002 147004 147010 147014 147016 147022 147026 147032 147040 211419
| A. | H2SiO4 | B. | SiO2 | C. | Si | D. | SiH4 |
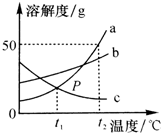 如图是a、b、c三种物质的溶解度曲线,回答下列问题:
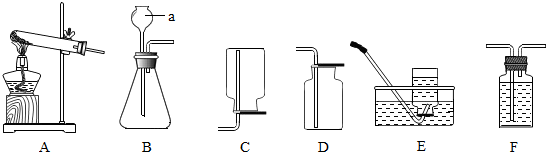
如图是a、b、c三种物质的溶解度曲线,回答下列问题: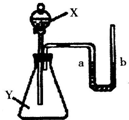 如下装置中,在密闭的锥形瓶中放入一种Y物质,当向分液漏斗中X物质滴入锥形瓶中时,U型管左侧液面下降,右侧液面上升,根据要求回答下列问题:
如下装置中,在密闭的锥形瓶中放入一种Y物质,当向分液漏斗中X物质滴入锥形瓶中时,U型管左侧液面下降,右侧液面上升,根据要求回答下列问题: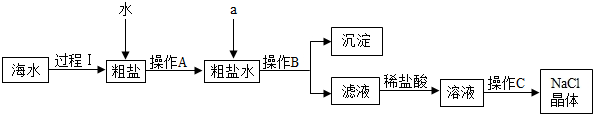
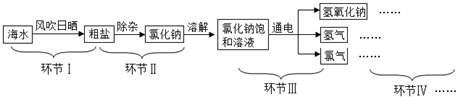
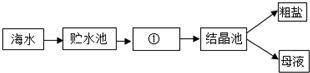
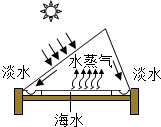 钓鱼岛及其附属岛屿自古以来就是我国固有领土,其附近海域蕴含丰富的化石燃料和矿产资源.
钓鱼岛及其附属岛屿自古以来就是我国固有领土,其附近海域蕴含丰富的化石燃料和矿产资源.