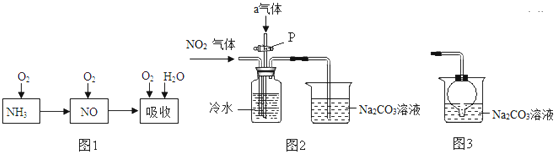
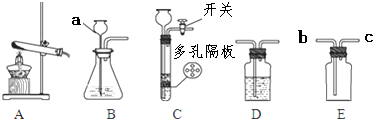
10.下列属于物理变化是 ( )
| A. | 绿色植物光合作用吸收二氧化碳 | B. | 用糯米等原料做酒 | ||
| C. | 分离液态空气制氧气 | D. | 灼烧方法来区分羊毛和化纤 |
9.硫酸铜是一种应用极其广泛的化工原料,易溶于水而不易溶于酒精;以下是某工厂用含铁废铜为原料生产胆矾(CuSO4•5H2O)和副产物石膏(CaSO4•2H2O)的生产流程示意图:
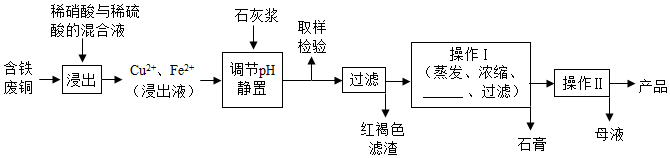
胆矾和石膏在不同温度下的溶解度(g/100g水)如表.
请回答下列问题:
(1)红褐色滤渣的主要成分是Fe(OH)3;
(2)含铁的废铜和稀硫酸反应的化学方程式Fe+H2SO4=FeSO4+H2↑;
(3)操作I最后温度应该控制在100℃左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、冷却结晶、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是减少因晶体溶解造成的损失.

胆矾和石膏在不同温度下的溶解度(g/100g水)如表.
| 温度(℃) | 20 | 40 | 60 | 80 | 100 |
| 石膏 | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾 | 32 | 44.6 | 61.8 | 83.8 | 114 |
(1)红褐色滤渣的主要成分是Fe(OH)3;
(2)含铁的废铜和稀硫酸反应的化学方程式Fe+H2SO4=FeSO4+H2↑;
(3)操作I最后温度应该控制在100℃左右;
(4)从溶液中分离出硫酸铜晶体的操作Ⅱ应为蒸发浓缩、冷却结晶、过滤、洗涤、干燥;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是减少因晶体溶解造成的损失.
5.化学学习让我们有很多收获.下列归纳和总结完全正确的一组是
( )
| A.对化学资源的认识 | B.对人物贡献的认识 |
| ①可用塑料来代替部分铜制造汽车零部件 ②稀土是不可再生的重要战略资源,应合 理利用和保护 | ①拉瓦锡:定量法测定空气的组成 ②张青莲:电解水法测定水的组成 |
| C.对物质俗称的认识 | D.对安全的认识 |
| ①烧碱、纯碱都是氢氧化钠 ②熟石灰、消石灰都是氢氧化钙 | ①点燃可燃性气体前一定要验纯 ②含有亚硝酸钠的工业用盐可以食用 |
| A. | A | B. | B | C. | C | D. | D |
4.下列除杂(括号内为杂质)选用的试剂或方法正确的是( )
| A. | CuO(C):隔绝空气高温加热 | |
| B. | CaCl2溶液(HCl):加入过量碳酸钙,充分反应后过滤 | |
| C. | CO2(CO):点燃 | |
| D. | BaSO4(BaCO3):加足量稀盐酸、过滤、蒸发、结晶 |
3.下列说法中正确的是( )
| A. | 向某固体中加入稀盐酸,产生气体,则该固体一定是碳酸盐 | |
| B. | 置换反应中一定会发生元素化合价的改变 | |
| C. | 把CuSO4、HNO3、BaCl2同时加到水中,能得到无色透明的溶液 | |
| D. | 某溶液中加入BaCl2溶液,产生白色沉淀,则该溶液中肯定含有SO42- |
2.如图所示为某反应在同一容器中反应前后微粒示意图.下列说法不正确的是( )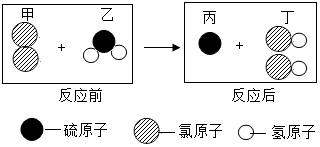

| A. | 反应物乙属于氧化物 | |
| B. | 该反应的化学方程式为Cl2+H2S=S↓+2HCl | |
| C. | 原子是化学变化中的最小粒子 | |
| D. | 物质丁的溶液pH小于7 |
1.味精是常见调味料之一,主要成分是谷氨酸钠[化学式为C5H8NO4Na],熔点232℃,20℃时溶解度71.7g.下列有关叙述错误的是( )
0 146805 146813 146819 146823 146829 146831 146835 146841 146843 146849 146855 146859 146861 146865 146871 146873 146879 146883 146885 146889 146891 146895 146897 146899 146900 146901 146903 146904 146905 146907 146909 146913 146915 146919 146921 146925 146931 146933 146939 146943 146945 146949 146955 146961 146963 146969 146973 146975 146981 146985 146991 146999 211419
| A. | 谷氨酸钠相对分子质量为169 | |
| B. | 谷氨酸钠是由5个碳原子、8个氢原子、4个氧原子、1个氮原子和1个钠原子构成 | |
| C. | 20℃时,100g水最多可配制成171.7g谷氨酸钠的饱和溶液 | |
| D. | 谷氨酸钠中钠元素的质量分数约为13.6% |