5.矿泉水中元素及国标含量如表所示,请用化学用语回答下列问题.
①矿泉水中含有的镁元素Mg;
②久置的水中溶有一定量的氧气,请表示出n个氧分子nO2;
③表中的一种阴离子Cl-等;
④硫酸钙中钙元素的化合价$\stackrel{+2}{Ca}$SO4.
| 矿物质水中主要成分(mg/1L) | |
| 偏硅酸(H2SiO3)≥25 | 钙≥0.2 |
| 硫酸根≥0.05 | 钠≥0.2 |
| 氯离子≤5 | 镁≥0.2 |
②久置的水中溶有一定量的氧气,请表示出n个氧分子nO2;
③表中的一种阴离子Cl-等;
④硫酸钙中钙元素的化合价$\stackrel{+2}{Ca}$SO4.
4.将质量为15g的大理石加入烧杯中,再加人120g溶质质量分数为7.3%的稀盐酸,充分反应后(该大理石所含杂质既不溶于水也不参加反应),所得溶液的质量为125.6g(不考虑溶液中残留的二氧化碳),则大理石的纯度约为( )
| A. | 66.7% | B. | 80% | C. | 90% | D. | 90.9% |
1.(1)根据表1中相关信息,回答下列问题:
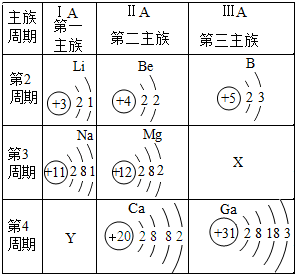
①X处对应原子的最外层电子数为3,Y处对应原子的核外电子层数为4;
②镓原子(Ca)的核外电子数为31,其在化学反应中易失(填“得”或“失”)电子形成镓离子,该离子符号为Ga3+.
(2)物质甲和乙完全反应生成物质丙和丁,各物质的微观示意图如表2所示,下列说法正确的有A
A.甲物质属于有机物
B.该反应属于置换反应
C.反应前后元素的种类增加
D.该反应的化学方程式为:C2H2+3O2═2CO2+2H2O.

①X处对应原子的最外层电子数为3,Y处对应原子的核外电子层数为4;
②镓原子(Ca)的核外电子数为31,其在化学反应中易失(填“得”或“失”)电子形成镓离子,该离子符号为Ga3+.
(2)物质甲和乙完全反应生成物质丙和丁,各物质的微观示意图如表2所示,下列说法正确的有A
| 物质 | 甲 | 乙 | 丙 | 丁 | 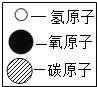 |
| 分子示意图 |  |  |  |
B.该反应属于置换反应
C.反应前后元素的种类增加
D.该反应的化学方程式为:C2H2+3O2═2CO2+2H2O.
19.将一定质量的饱和氯化钠溶液通电一段时间后,质量叙述正确的是( )
(反应原理为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑)
(反应原理为:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$2NaOH+H2↑+Cl2↑)
| A. | 溶液的pH逐渐减小 | B. | 溶液中钠元素的质量增大 | ||
| C. | 溶液中氧元素的质量分数不变 | D. | 氯化钠溶液的溶质质量分数减小 |
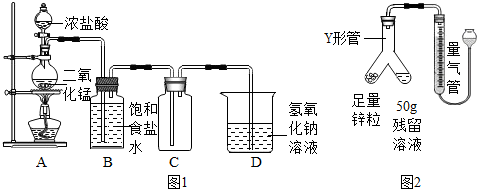
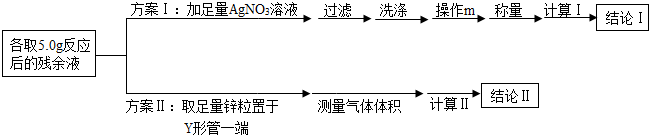
18.下列对如图所示四个实验的认识错误的是( )
 |  |  |  |
| 甲 | 乙 | 丙 | 丁 |
| A. | 甲和丁实验的主要目的是探究物质的化学性质 | |
| B. | 乙实验的目的是探究化学反应前后物质的质量关系 | |
| C. | 对于有气体参与的定量实验,实验前需检查乙和丙装置的气密性 | |
| D. | 为探究酸碱是否发生反应,丁实验必需准确量取氢氧化钠溶液的体积 |
17.下列各组物质能在水溶液中大量共存的是( )
| A. | MgSO4和BaCl2 | B. | HNO3和NaCl | C. | Ca(OH)2和Fe2(SO4)3 | D. | KOH和H2SO4 |
16.以下实验无法比较铜和铁的金属活动性强弱的是( )
0 146737 146745 146751 146755 146761 146763 146767 146773 146775 146781 146787 146791 146793 146797 146803 146805 146811 146815 146817 146821 146823 146827 146829 146831 146832 146833 146835 146836 146837 146839 146841 146845 146847 146851 146853 146857 146863 146865 146871 146875 146877 146881 146887 146893 146895 146901 146905 146907 146913 146917 146923 146931 211419
| A. | 观察两种金属片的颜色 | B. | 铜片放入氯化亚铁溶液中 | ||
| C. | 铁片放入硫酸铜溶液中 | D. | 铜片、铁片分别放入稀硫酸中 |