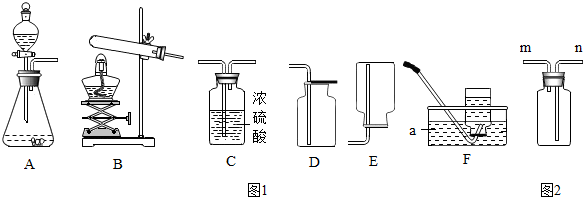
15.小明等四位同学以“蜡烛的高度会影响蜡烛燃烧时间的长短,并通过实验比较它们的效果”为课题开展研究,请就他们活动中的一些问题,你认为不正确的是( )
| A. | 在同组实验时,都使用颜色相同的蜡烛 | |
| B. | 在同组实验时,都使用粗细相同的蜡烛 | |
| C. | 在同组实验时,都使用大小相同的烧杯 | |
| D. | 在同组实验时,灯芯的材料可以不同 |
14.下列化学实验的操作不正确的是( )
| A. | 给烧杯加热时,要垫上石棉网 | |
| B. | 给试管里的液体加热,液体体积不超过试管容积的三分之一 | |
| C. | 给试管里的液体加热时,不让试管口对着自己和旁人 | |
| D. | 实验中剩余的药品都要放回原试剂瓶 |
11.某无色溶液可使紫色石蕊试纸变红,该溶液中还能大量共存的离子组为( )
| A. | NH4+、Na+、Cl-、CO32- | B. | B、Na+、K+、Cu2+、Cl- | ||
| C. | K+、Cl-、Mg2+、SO42- | D. | Ag+、NO3-、Mg2+、Cl- |
10.吸烟有害健康,其中一种有害物质尼古丁化学式为(C10H14N2),下列关于尼古丁的说法正确的是( )
| A. | 尼古丁中含有氮气分子 | |
| B. | 尼古丁属于有机物 | |
| C. | 尼古丁中氮元素质量分数最小 | |
| D. | 尼古丁由10个碳原子、14个氢原子、2个氮原子构成 |
9.高岭石的化学式可表示为Al2(Si2O5)(OH)4,其中Si的化学价为( )
| A. | +2 | B. | +4 | C. | +6 | D. | -2 |
8.按金属单质、碱、盐的顺序排列的一组物质是( )
| A. | 铜、纯碱、氯化钾 | B. | 钢、火碱、硝酸银 | ||
| C. | 水银、熟石灰、小苏打 | D. | 锌、氢氧化铜、石灰石 |
7.化学与生活、社会密切相关,下列说法正确的是( )
| A. | 食品添加剂有害人体健康,应禁止使用 | |
| B. | 购物时减少使用或不用塑料袋,是为了减少“白色污染” | |
| C. | 为防止土壤和水体富营养化,应禁止使用化肥与农药 | |
| D. | 不吃水果蔬菜,多吃含蛋白质的肉类,更能增强体质 |
6.某同学对一瓶长期暴漏在空气中的氢氧化钠固体样品的成分及含量进行探究.
【提出问题】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3.
则NaOH变质反应的化学方程式为CO2+2NaOH=Na2CO3+H2O;
【查阅资料】
①碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
②CO2在饱和碳酸氢钠溶液汇总几乎不溶解.
【实验探究】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
【提出问题2】怎样提纯该样品得到纯净的氢氧化钠固体?
【实验探究2】为得到纯净的氢氧化钠固体,小亮明设计了如图1所示的实验流程.请回答下列问题:
(1)该实验中发生反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(2)最终所得氢氧化钠固体质量大于(填“大于”、“等于”或“小于”)变质后样品中氢氧化钠的质量.
【实验反思】
(1)通过本题,你学会了定性检验氢氧化钠的变质和除杂提纯物质.为了得到可靠的实验结果,探究过程中你需要思考的问题有①②④⑤⑥(填数字序号);
①选择试剂种类 ②确定试剂用量 ③试剂产地 ④实验装置与步骤的设计 ⑤实验安全环保 ⑥测量中减少误差.
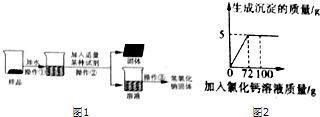
(2)向50g Na2co3溶液总逐滴加入一定溶质质量分数的CaCl2溶液,实验过程中,生成沉淀的质量与加入CaCl2溶液的质量关系如图所示,试计算:恰好完全反应时,所得溶液中溶质的质量分数.
0 146666 146674 146680 146684 146690 146692 146696 146702 146704 146710 146716 146720 146722 146726 146732 146734 146740 146744 146746 146750 146752 146756 146758 146760 146761 146762 146764 146765 146766 146768 146770 146774 146776 146780 146782 146786 146792 146794 146800 146804 146806 146810 146816 146822 146824 146830 146834 146836 146842 146846 146852 146860 211419
【提出问题】该样品中含有哪些物质?
【提出猜想】通过分析,提出如下猜想:
猜想Ⅰ:已完全变质,该样品中只含Na2CO3;
猜想Ⅱ:部分变质,该样品中含有NaOH和Na2CO3.
则NaOH变质反应的化学方程式为CO2+2NaOH=Na2CO3+H2O;
【查阅资料】
①碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应;
②CO2在饱和碳酸氢钠溶液汇总几乎不溶解.
【实验探究】为确定该样品的成分,小明设计了如下实验方案,请你一起完成下列实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品溶于水,加入 过量CaCl2溶液; | 白色沉淀产生 | 该反应的化学方程式:Na2CO3+CaCl2═2NaCl+CaCO3↓ |
| (2)将上述反应后的混合液过滤,取滤液加入酚酞试液; | 溶液变红色 | 证明猜想Ⅱ正确 |
【实验探究2】为得到纯净的氢氧化钠固体,小亮明设计了如图1所示的实验流程.请回答下列问题:
(1)该实验中发生反应的化学方程式为Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
(2)最终所得氢氧化钠固体质量大于(填“大于”、“等于”或“小于”)变质后样品中氢氧化钠的质量.
【实验反思】
(1)通过本题,你学会了定性检验氢氧化钠的变质和除杂提纯物质.为了得到可靠的实验结果,探究过程中你需要思考的问题有①②④⑤⑥(填数字序号);
①选择试剂种类 ②确定试剂用量 ③试剂产地 ④实验装置与步骤的设计 ⑤实验安全环保 ⑥测量中减少误差.
(2)向50g Na2co3溶液总逐滴加入一定溶质质量分数的CaCl2溶液,实验过程中,生成沉淀的质量与加入CaCl2溶液的质量关系如图所示,试计算:恰好完全反应时,所得溶液中溶质的质量分数.

 A、B、C、D、E是初中化学中常见的五种物质.在通常情况下,A为黑色粉末状固体,B、C均为无色无味的气体,D为不溶于水的白色固体,在实验室常用含D的物质与稀盐酸反应制取C,单质E是组成空气的主要成分之一.它们之间的关系如图所示(图中反应条件及反应④和⑤中某些反应物、生成物已略去).
A、B、C、D、E是初中化学中常见的五种物质.在通常情况下,A为黑色粉末状固体,B、C均为无色无味的气体,D为不溶于水的白色固体,在实验室常用含D的物质与稀盐酸反应制取C,单质E是组成空气的主要成分之一.它们之间的关系如图所示(图中反应条件及反应④和⑤中某些反应物、生成物已略去).