6.2013年4月25日晚8点,台州市路桥区峰江街道一金属堆场,十多吨金属镁发生爆燃.金属镁是一种银白色的金属,燃烧时能产生眩目的白光,极易发生爆炸.此外,金属镁在高温条件下遇到水会释放出氢气,还能在二氧化碳中剧烈燃烧产生一种白色粉末和一种黑色粉末.你认为他的结论不正确的是( )
| A. | 某些金属的燃烧不能用CO2灭火 | |
| B. | 该反应是放出热量 | |
| C. | 该反应的实质是Mg和CO2中混有的O2反应 | |
| D. | 某些金属的燃烧不能用水扑救 |
4.下列实验操作错误的是( )
| A. | 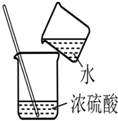 稀释浓硫酸 | B. | 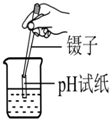 测定溶液pH值 | ||
| C. | 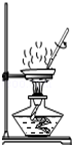 蒸发食盐水 | D. | 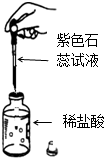 检验稀盐酸的酸碱性 |
3.下列有关实验操作中,错误的是( )
| A. | 实验室用排水法收集O2,实验结束时,应该先将导管移出水面,再熄灭酒精灯 | |
| B. | 点燃H2前,必须先检验H2的纯度 | |
| C. | 用H2还原CuO,应该选通H2,然后再加热 | |
| D. | 用H2还原CuO结束时,应该先停止通H2,然后再停止加热 |
2.分离、除杂和检验是化学实验的重要环节,下列实验设计能达到目的是
( )
| 实验内容 | 实验设计 | |
| A | 除去铜粉中少量的铁粉 | 加入足量的稀硫酸,过滤,蒸发 |
| B | 提纯含有少量NaCl的KNO3固体 | 先加入水溶解,蒸发结晶 |
| C | 区分NH4HCO3和NH4Cl | 取样,加稀盐酸,观察是否有气泡产生 |
| D | 分离CO2和CO混合物 | 先用NaOH溶液吸收掉CO2分离出CO,再向剩余溶液中加浓盐酸,即可“释放”出纯净的CO2 |
| A. | A | B. | B | C. | C | D. | D |
20.化学老师交给某研究性学习小组一个任务:测定实验室里一瓶久置的NaOH固体是否变质.该小组的同学进行了如下实验探究:
【提出问题】猜想I:没变质,全部是NaOH;猜想II:部分变质,既含有NaOH又含有Na2CO3:猜想Ⅲ:完全变质,全部是Na2CO3.
【查阅资料】①已知反应:CaCl2+Na2CO3=2NaCl+CaCO3↓
②部分盐溶液在常温下的pH如下:
设计方案并进行实验】请你与他们一起共同完成,并回答所给问题.
上述步骤①中,滴加过量CaCl2溶液的目的是除去Na2CO3
【实验结论】通过实验,说明上述猜想中Ⅱ是正确的.
【思维拓展】有同学认为先向溶液中滴加足量的Ca(OH)2溶液,再滴入酚酞,根据现象不同来判断猜想II或猜想Ⅲ成立.经讨论同学们认为此方案不行,原因是氢氧化钙和碳酸钠反应会产生氢氧化钠,对氢氧化钠的检验产生干扰.
0 146639 146647 146653 146657 146663 146665 146669 146675 146677 146683 146689 146693 146695 146699 146705 146707 146713 146717 146719 146723 146725 146729 146731 146733 146734 146735 146737 146738 146739 146741 146743 146747 146749 146753 146755 146759 146765 146767 146773 146777 146779 146783 146789 146795 146797 146803 146807 146809 146815 146819 146825 146833 211419
【提出问题】猜想I:没变质,全部是NaOH;猜想II:部分变质,既含有NaOH又含有Na2CO3:猜想Ⅲ:完全变质,全部是Na2CO3.
【查阅资料】①已知反应:CaCl2+Na2CO3=2NaCl+CaCO3↓
②部分盐溶液在常温下的pH如下:
| 盐溶液 | NaCI | Na2CO3 | CaCl2 |
| pH | 等于7 | 大于7 | 等于7 |
| 实验步骤 | 实验现象 | 实验结论 |
| ①称取上述氢氧化钠固体样品8.0g溶于50ml,水配成溶液,向溶液中滴加氯化钙溶液至过量,充分反应后,静置. | 产生白色沉淀 | 说明久置固体中,一定含有 Na2CO3(填化学式). |
| ②用玻璃棒蘸取少量①中充分反应后的上层清液滴在一小块pH试纸上,与标准比色卡对比,测出pH | pH=11 | 说明久置固体中,还一定含有NaOH (填化学式). |
【实验结论】通过实验,说明上述猜想中Ⅱ是正确的.
【思维拓展】有同学认为先向溶液中滴加足量的Ca(OH)2溶液,再滴入酚酞,根据现象不同来判断猜想II或猜想Ⅲ成立.经讨论同学们认为此方案不行,原因是氢氧化钙和碳酸钠反应会产生氢氧化钠,对氢氧化钠的检验产生干扰.

 用相同质量的铁和锌(颗粒状态相同)跟一定量的稀硫酸反应,其反应过程如图所示(图中横、纵坐标分别表示反应的时间t和产生氢气的质量m).试回答:
用相同质量的铁和锌(颗粒状态相同)跟一定量的稀硫酸反应,其反应过程如图所示(图中横、纵坐标分别表示反应的时间t和产生氢气的质量m).试回答: 归纳是学习的重要方法,李明在学习酸、碱、盐后,绘制出如图所示的物质之间的反应关系,(图中短线连接的物质表示能相互反应),请填写下列空白:
归纳是学习的重要方法,李明在学习酸、碱、盐后,绘制出如图所示的物质之间的反应关系,(图中短线连接的物质表示能相互反应),请填写下列空白: