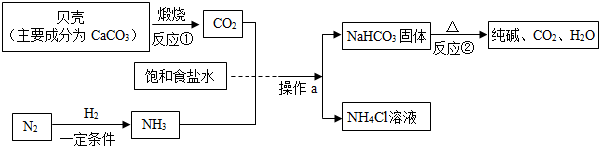
10.当前,世界已经迈向了“低碳”时代,选择“低碳”既是一种生活方式也是一种生存责任.公交系统推广使用节能减排的双燃料公交车,这种公交车以天然气为主要燃料.下图为天然气的主要成分甲烷完全燃烧的化学反应的微观示意图.
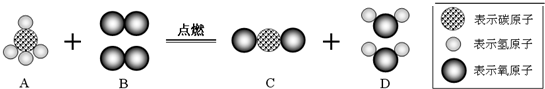
请根据示意图回答下列问题:
(1)用微粒观点分析,上述反应前后原子种类和数目一定不变.
(2)写出上述反应的化学方程式:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
则a的值为2.8,根据表格中数据,请完成相关的化学方程式4CH4+7O2$\frac{\underline{\;点燃\;}}{\;}$2CO2+2CO+8H2O.

请根据示意图回答下列问题:
(1)用微粒观点分析,上述反应前后原子种类和数目一定不变.
(2)写出上述反应的化学方程式:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(3)甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
| 物质 | 甲烷 | 氧气 | 水 | 二氧化碳 | X |
| 反应前质量/g | 3.2 | 11.2 | 0 | 0 | 0 |
| 反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
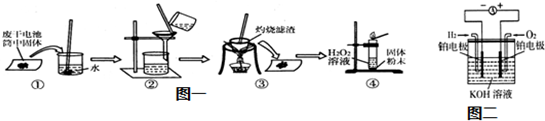
7. 利用如图所示装置测定某含菱铁矿的矿石样品中碳酸亚铁的质量分数(杂质不含铁元素且在实验过程中不发生任何变化),实验数据记录在下表中.
利用如图所示装置测定某含菱铁矿的矿石样品中碳酸亚铁的质量分数(杂质不含铁元素且在实验过程中不发生任何变化),实验数据记录在下表中.
提示:FeCO3 $\frac{\underline{\;高温\;}}{\;}$FeO+CO2↑,CO+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2
下列判断正确的是( )
 利用如图所示装置测定某含菱铁矿的矿石样品中碳酸亚铁的质量分数(杂质不含铁元素且在实验过程中不发生任何变化),实验数据记录在下表中.
利用如图所示装置测定某含菱铁矿的矿石样品中碳酸亚铁的质量分数(杂质不含铁元素且在实验过程中不发生任何变化),实验数据记录在下表中.提示:FeCO3 $\frac{\underline{\;高温\;}}{\;}$FeO+CO2↑,CO+FeO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2
| 实验前 | 实验后 | |
| 硬质玻璃管(含样品) | 160.6g | 154.6g |
| 说 明 | ①空硬质玻璃管质量为l40.6g ②含铁各物质反应完全 | |
| A. | 一氧化碳还原氧化亚铁的反应属于置换反应 | |
| B. | 充分反应后,玻璃管及其中物质的总质量较反应前减少6g,该质量为参加反应的碳酸亚铁中碳酸根的质量 | |
| C. | 矿石样品中含碳酸亚铁的质量为11.6g | |
| D. | 实验结束后盛有澄清石灰水的试管的总质量比反应前的总质量增加了4.4g |
6.下列实验操作正确的是( )
0 146588 146596 146602 146606 146612 146614 146618 146624 146626 146632 146638 146642 146644 146648 146654 146656 146662 146666 146668 146672 146674 146678 146680 146682 146683 146684 146686 146687 146688 146690 146692 146696 146698 146702 146704 146708 146714 146716 146722 146726 146728 146732 146738 146744 146746 146752 146756 146758 146764 146768 146774 146782 211419
| A. | 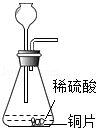 实验室制取氢气 | B. | 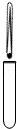 取用块状固体 | C. |  稀释浓硫酸 | D. | 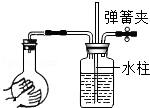 气密性检查 |