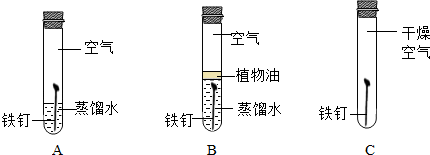
6.若将亚硝酸钠(NaNO2)误作食盐食用,会使人中毒,甚至死亡.NaNO2中N元素的化合价是( )
| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
5.维生素C(C6H8O6)主要存在于蔬菜和水果中,它能促进人体生长发育,增强人体对疾病的抵抗力.近年来,科学家还发现维生素 C 有防癌作用.下列关于维生素 C 的说法中错误的是( )
| A. | 维生素 C 是氧化物 | |
| B. | 维生素 C 是由6个碳元素、8个氢元素、6个氧元素组成 | |
| C. | 维生素 C 中,C、H、O三种元素的质量比为 9:1:12 | |
| D. | 青少年应多吃蔬菜水果,切忌偏食 |
4.我国青海湖采集的天然碱样品可表示为aNa2CO3•bNaHCO3•cH2O(a、b、c为最简整数比).某实验小组为测定其组成,称取该天然碱样品16.6g进行如下实验:
资料Ⅰ:碳酸氢钠不稳定,加热易分解为碳酸钠、二氧化碳和水,而碳酸钠比较稳定,
加热时不分解;
资料Ⅱ:图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
资料Ⅲ:装置C、F、G中都是碱石灰(CaO与NaOH的固体混合物)
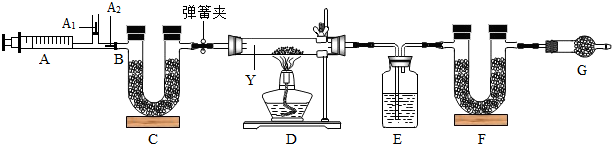
【实验步骤】①连接好装置,先检查装置的气密性;②反复推拉注射器;③称量E、F的质量;④关闭弹簧夹,加热D处试管直到反应不再进行;⑤打开弹簧夹,再次反复缓缓推拉注射器;⑥再次称量E、F的质量.
问题探究】
(1)仪器Y的名称是硬质玻璃管;
(2)实验步骤①连接好装置,先检查装置的气密性;
(3)E中的药品为浓硫酸(填名称),目的是吸收水蒸气,F的作用是吸收生成的二氧化碳,G的作用是防止空气中的二氧化碳和水蒸气被F吸收;
(4)实验步骤②与③能否颠倒不能(填“能”或“不能”). 若无装置C,则所测得的碳酸氢钠质量分数偏大(填“偏大”、“偏小”、“无影响”).若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数偏小(填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是使残留在装置中的二氧化碳和水蒸气充分被吸收.
(5)写出装置D中发生的化学反应化学方程式aNa2CO3•bNaHCO3•cH2O$\frac{\underline{\;\;△\;\;}}{\;}$$\frac{2a+b}{2}$Na2CO3+$\frac{b+2c}{2}$H2O+$\frac{b}{2}$CO2↑(计量数用abc表示)
(6)通过右表数据,求得该天然碱化学式中a:b:c=2:1:2.(写出过程,4分)
资料Ⅰ:碳酸氢钠不稳定,加热易分解为碳酸钠、二氧化碳和水,而碳酸钠比较稳定,
加热时不分解;
资料Ⅱ:图中B处为两个单向阀:推注射器时A1关闭,A2处打开;拉注射器时,A1打开进空气,A2关闭.
资料Ⅲ:装置C、F、G中都是碱石灰(CaO与NaOH的固体混合物)

【实验步骤】①连接好装置,先检查装置的气密性;②反复推拉注射器;③称量E、F的质量;④关闭弹簧夹,加热D处试管直到反应不再进行;⑤打开弹簧夹,再次反复缓缓推拉注射器;⑥再次称量E、F的质量.
问题探究】
(1)仪器Y的名称是硬质玻璃管;
(2)实验步骤①连接好装置,先检查装置的气密性;
(3)E中的药品为浓硫酸(填名称),目的是吸收水蒸气,F的作用是吸收生成的二氧化碳,G的作用是防止空气中的二氧化碳和水蒸气被F吸收;
(4)实验步骤②与③能否颠倒不能(填“能”或“不能”). 若无装置C,则所测得的碳酸氢钠质量分数偏大(填“偏大”、“偏小”、“无影响”).若不进行步骤⑤的操作,则所测得的碳酸氢钠质量分数偏小(填“偏大”、“偏小”、“无影响”),该操作中推注射器时缓缓的目的是使残留在装置中的二氧化碳和水蒸气充分被吸收.
(5)写出装置D中发生的化学反应化学方程式aNa2CO3•bNaHCO3•cH2O$\frac{\underline{\;\;△\;\;}}{\;}$$\frac{2a+b}{2}$Na2CO3+$\frac{b+2c}{2}$H2O+$\frac{b}{2}$CO2↑(计量数用abc表示)
| 反应前 | 反应后 | |
| 装置E的质量/g | 100.0 | 102.25 |
| 装置F的质量/g | 50.0 | 51.1 |
20.下列说法正确的是( )
| A. | 只有燃烧反应才会放出热量 | |
| B. | 浓氢氧化钠溶液沾到手上,马上用大量清水冲洗,然后涂上硼酸溶液 | |
| C. | 生成盐和水的反应一定是中和反应 | |
| D. | 盐中一定含有金属元素 |
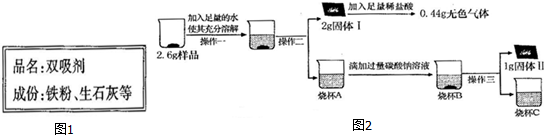
19.“双吸剂”是一种常见袋装食品的保鲜剂,能吸收空气中的氧气、二氧化碳、水蒸气 等.化学兴趣小组的同学在某食品袋中发现一包“双吸剂”,其标签如图1所示.同学们 对这包久置的“双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置“双吸剂”固体的成分是什么?
【查阅资料】
①铁与氯化铁溶液在常温下反应生成氯化亚铁
:Fe+2FeCl3═3FeCl2;
②碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究1】下表是小明设计的实验方案和记录的实验报告,请你补充完整.
【实验质疑】小组同学通过讨论认为实验并不能得出一定不含Fe2O3的结论,理由是Fe2O3+6HCl═2FeCl3+3H2O、Fe+2FeCl3=3FeCl2(用化学方程式表示).
为进一步确定这包久置的“双吸剂”固体的成分进行如下定量实验.
【实验探究2】取3g样品研碎,并用磁铁充分吸引后,得到剩余固体2.6g,按照图2流程进行实验,请回答相关问题:
(1)操作二、操作三名称是过滤.
(2)固体I的成分是CaCO3和Fe2O3.(填物质化学式,下同);
(3)烧杯A中溶液和加入的碳酸钠溶液反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.

【提出问题】久置“双吸剂”固体的成分是什么?
【查阅资料】
①铁与氯化铁溶液在常温下反应生成氯化亚铁
:Fe+2FeCl3═3FeCl2;
②碱性的Na2CO3溶液可以与中性的CaCl2溶液发生复分解反应.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究1】下表是小明设计的实验方案和记录的实验报告,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量样品放入试管中,滴加一定量的稀盐酸.用带异營的单孔橡皮塞塞紧试管口,导管另 一端伸入澄清石灰水中. | 试管中固体逐漸减少,有大量无色气体产生,得到浅绿色溶液,澄清石灰水变浑浊. | 样品中一定含有Fe和CaCO3, 不含Fe2O3. |
| (2)取少量样品放入试管中,加水 溶解,静置后取上层清液滴加无 色酚酞试液. | 试管底部有不溶物,上层清液由无色变为红色. | 样品中含有氧化钙或氢氧化钙. |
为进一步确定这包久置的“双吸剂”固体的成分进行如下定量实验.
【实验探究2】取3g样品研碎,并用磁铁充分吸引后,得到剩余固体2.6g,按照图2流程进行实验,请回答相关问题:
(1)操作二、操作三名称是过滤.
(2)固体I的成分是CaCO3和Fe2O3.(填物质化学式,下同);
(3)烧杯A中溶液和加入的碳酸钠溶液反应的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
18.物质都是由微粒构成的.下列物质由分子构成的是( )
0 146453 146461 146467 146471 146477 146479 146483 146489 146491 146497 146503 146507 146509 146513 146519 146521 146527 146531 146533 146537 146539 146543 146545 146547 146548 146549 146551 146552 146553 146555 146557 146561 146563 146567 146569 146573 146579 146581 146587 146591 146593 146597 146603 146609 146611 146617 146621 146623 146629 146633 146639 146647 211419
| A. | 二氧化碳 | B. | 氯化钠 | C. | 金刚石 | D. | 铜 |