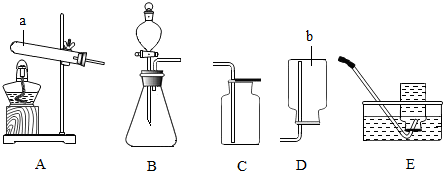
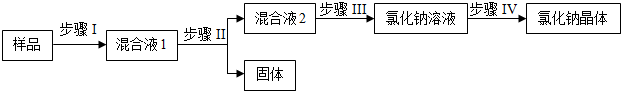
2.下列有关溶液的说法错误的是( )
| A. | 生理盐水中溶质是氯化钠 | |
| B. | 一种溶液中溶剂只有一种 | |
| C. | 浓溶液可能是不饱和溶液 | |
| D. | 饱和溶液就是不能再溶解这种溶质的溶液 |
1.下列说法符合质量守恒定律的是( )
| A. | 酒精敞口放置一段时间后,质量减少 | |
| B. | 铜片放入硝酸银溶液中,固体质量增加 | |
| C. | 2克氢气和1克氧气充分反应生成3克水 | |
| D. | 碳酸分解反应中,分子和原子个数都增加 |
19.下列各组物质,属于单质的是( )
| A. | 二氧化碳 | B. | 水 | C. | 臭氧(化学式:O3) | D. | 澄清石灰水 |
17.下列实验进行中的现象或实验原理正确的是( )
| A. | 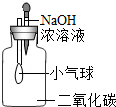 小气球变瘪 | B. |  U型管内液面左高右低 | ||
| C. | 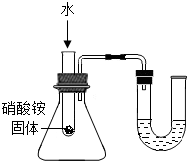 U型管内液面左高右低 | D. | 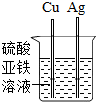 验证铁、铜和银金属活动性强弱 |
16.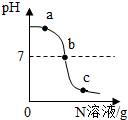 已知M、N分别是稀盐酸、氢氧化钠溶液中的一种.某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH值,如图所示.
已知M、N分别是稀盐酸、氢氧化钠溶液中的一种.某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH值,如图所示.
(1)M是氢氧化钠溶液,该反应的化学方程式NaOH+HCl=NaCl+H2O.
(2)反应过程中,老师取a、b、c三处反应后的溶液,打乱顺序后,请同学们不测定溶液的pH值,用其它方法对三种溶液进行探究.
小明和小红分别取其中一种溶液进行实验;
小明向所取溶液中加入CuSO4溶液,观察到有蓝色沉淀生成.
结论:是a处溶液.
小红向少量另一种溶液中滴加酚酞溶液,观察到溶液呈无色
结论:是b处或c处溶液.
为进一步确定该溶液成分,小红又设计并完成如下实验:
0 146417 146425 146431 146435 146441 146443 146447 146453 146455 146461 146467 146471 146473 146477 146483 146485 146491 146495 146497 146501 146503 146507 146509 146511 146512 146513 146515 146516 146517 146519 146521 146525 146527 146531 146533 146537 146543 146545 146551 146555 146557 146561 146567 146573 146575 146581 146585 146587 146593 146597 146603 146611 211419
 已知M、N分别是稀盐酸、氢氧化钠溶液中的一种.某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH值,如图所示.
已知M、N分别是稀盐酸、氢氧化钠溶液中的一种.某化学兴趣小组同学在一定量的M中不断滴加N,并测定所得溶液的pH值,如图所示.(1)M是氢氧化钠溶液,该反应的化学方程式NaOH+HCl=NaCl+H2O.
(2)反应过程中,老师取a、b、c三处反应后的溶液,打乱顺序后,请同学们不测定溶液的pH值,用其它方法对三种溶液进行探究.
小明和小红分别取其中一种溶液进行实验;
小明向所取溶液中加入CuSO4溶液,观察到有蓝色沉淀生成.
结论:是a处溶液.
小红向少量另一种溶液中滴加酚酞溶液,观察到溶液呈无色
结论:是b处或c处溶液.
为进一步确定该溶液成分,小红又设计并完成如下实验:
| 实验步骤 | 实验现象 | 结论 |
| 取少量该溶液,向其中滴加石蕊溶液(合理即可) | 溶液变红 | 为c处溶液,并推知溶液中的离子有Na+、H+、Cl-(填写离子符号) |
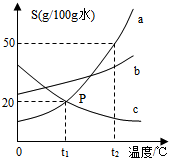 如图是a、b、c三种物质的溶解度曲线.试回答:
如图是a、b、c三种物质的溶解度曲线.试回答: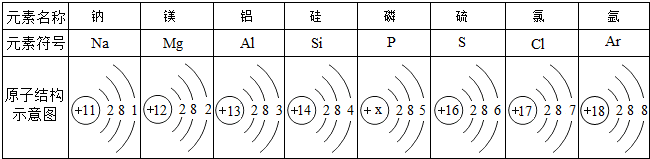 请回答下列问题:
请回答下列问题: