7.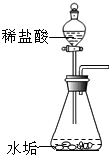 将过量稀盐酸逐滴加入到12.5g水垢粉末中,称量下图装置6分钟内减轻的质量,结果表示如下:
将过量稀盐酸逐滴加入到12.5g水垢粉末中,称量下图装置6分钟内减轻的质量,结果表示如下:
(1)仅利用上述实验数据,分析得出两个结论:
①实验中共产生4.4g CO2气体;
②随反应的进行,稀盐酸与水垢的反应速率减小(填“增大”“减小”“不变”),
你的依据是相同时间内质量减少的越来越少.
(2)求水垢中碳酸钙的质量分数80%.
(3)实验中测得碳酸钙的质量分数偏大的原因:氯化氢气体、水蒸气等随二氧化碳一起排出.
(4)如水垢化学式可表示为Mg(OH)2•2CaCO3,写出该水垢与稀盐酸总反应方程式:Mg(OH)2•2CaCO3+6HCl═2CaCl2+MgCl2+4H2O+2CO2↑.
 将过量稀盐酸逐滴加入到12.5g水垢粉末中,称量下图装置6分钟内减轻的质量,结果表示如下:
将过量稀盐酸逐滴加入到12.5g水垢粉末中,称量下图装置6分钟内减轻的质量,结果表示如下:| 时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
| 减少的质量/g | 0 | 2.2 | 3.2 | 3.8 | 4.2 | 4.4 | 4.4 |
①实验中共产生4.4g CO2气体;
②随反应的进行,稀盐酸与水垢的反应速率减小(填“增大”“减小”“不变”),
你的依据是相同时间内质量减少的越来越少.
(2)求水垢中碳酸钙的质量分数80%.
(3)实验中测得碳酸钙的质量分数偏大的原因:氯化氢气体、水蒸气等随二氧化碳一起排出.
(4)如水垢化学式可表示为Mg(OH)2•2CaCO3,写出该水垢与稀盐酸总反应方程式:Mg(OH)2•2CaCO3+6HCl═2CaCl2+MgCl2+4H2O+2CO2↑.
5.下列溶液中,使用无色酚酞试液能一次性鉴别出来的是( )
| A. | NaCl Na2SO4 | B. | NaCl HCl NaOH | ||
| C. | NaCl NaOH | D. | NaCl NaOH CaCl2 |
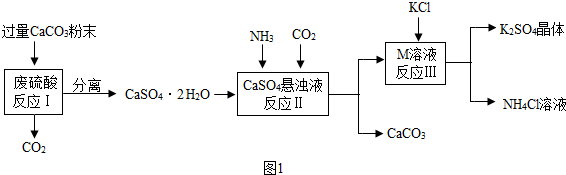
2.蛇纹石矿可以看做MgO、Fe2O3、Al2O3、SiO2组成.由蛇纹石制取碱式碳酸镁的实验流程如图1所示: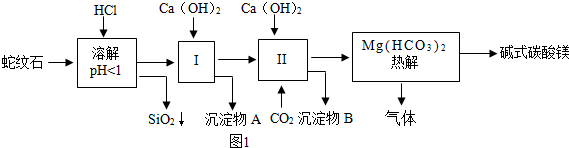
(1)蛇纹石加盐酸溶解后,溶液有Mg2+等3种金属离子产生,写出产生Mg2+的化学方程式MgO+2HCl=MgCl2+H2O.(2)进行Ⅰ操作时,控制溶液pH=6~7(有关氢氧化物沉淀的pH见表),沉淀物A中含有Fe(OH)3和Al(OH)3.该操作中Ca(OH)2不能过量,若Ca(OH)2过量,溶液pH会升高,可能导致Al(OH)3溶解,Mg(OH)2会沉淀析出.
(3)已知Mg(HCO3)2受热分解可以产生三种氧化物,请写出该反应方程式Mg(HCO3)2$\frac{\underline{\;\;△\;\;}}{\;}$MgO+2CO2↑+H2O.
(4)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是CO2.
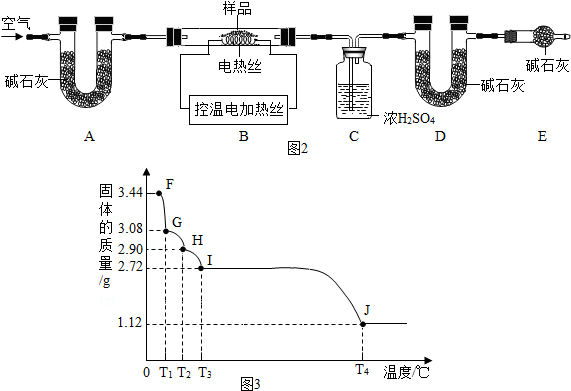
(5)确定产品碱式碳酸镁(mMgCO3•nMg(OH)2•xH2O)的组成.某同学组装仪器如图2所示:
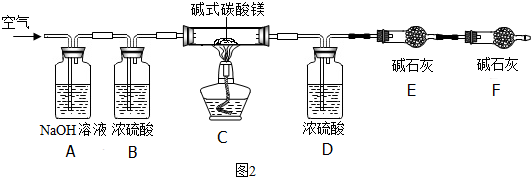
【资料查询】MgCO3、Mg(OH)2受热易分解,各生成对应的两种氧化物.
实验测得:硬质玻璃管中剩余的固体质量为2.0g,D处浓H2SO4增重0.9g,E处碱石灰增重1.76g.
①A装置中NaOH溶液的作用是除去空气中的二氧化碳;B装置中药品是除去空气中的水蒸气;在实验中要持续通入空气,其目的是使得碱式碳酸镁分解产生的二氧化碳和水蒸气被完全排出.
②通过计算可得碱式碳酸镁(mMgCO3•nMg(OH)2•xH2O)中m:n=4:1.x值为4.若将F装置去掉,对实验结果的影响是m值偏大(填“偏大”、“偏小”或“不变”).

(1)蛇纹石加盐酸溶解后,溶液有Mg2+等3种金属离子产生,写出产生Mg2+的化学方程式MgO+2HCl=MgCl2+H2O.(2)进行Ⅰ操作时,控制溶液pH=6~7(有关氢氧化物沉淀的pH见表),沉淀物A中含有Fe(OH)3和Al(OH)3.该操作中Ca(OH)2不能过量,若Ca(OH)2过量,溶液pH会升高,可能导致Al(OH)3溶解,Mg(OH)2会沉淀析出.
| 氢氧化物 | 溶液pH | |||
| 开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
| Fe(OH)3 | 2.3 | 3.4 | 沉淀不溶 | 沉淀不溶 |
| Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
| Mg(OH)2 | 8.6 | 11.1 | 沉淀不溶 | 沉淀不溶 |
(4)物质循环使用,能节约资源.上述实验中,可以循环使用的物质是CO2.
(5)确定产品碱式碳酸镁(mMgCO3•nMg(OH)2•xH2O)的组成.某同学组装仪器如图2所示:

【资料查询】MgCO3、Mg(OH)2受热易分解,各生成对应的两种氧化物.
实验测得:硬质玻璃管中剩余的固体质量为2.0g,D处浓H2SO4增重0.9g,E处碱石灰增重1.76g.
①A装置中NaOH溶液的作用是除去空气中的二氧化碳;B装置中药品是除去空气中的水蒸气;在实验中要持续通入空气,其目的是使得碱式碳酸镁分解产生的二氧化碳和水蒸气被完全排出.
②通过计算可得碱式碳酸镁(mMgCO3•nMg(OH)2•xH2O)中m:n=4:1.x值为4.若将F装置去掉,对实验结果的影响是m值偏大(填“偏大”、“偏小”或“不变”).
1.铁和铝是我们生活中常见的两种金属.某化学小组欲探究铁和铝的金属活动性强弱,设计如下实验方案:
(1)小组同学取来相同质量的铁、铝分别放入起始温度相同、体积也相同的10%稀盐酸中,一开始观察到的现象是铁表面有气泡,而铝无明显现象,小明于是得出与课本中相反的结论.小文同学马上提出质疑,你认为质疑的主要理由是铝表面有一层致密的氧化铝(或未打磨金属).一开始铝表面现象不明显,但此时发生的化学方程式为Al2O3+6HCl=2AlCl3+3H2O.为了达到实验目的,除了以上条件相同外,你认为还要控制2中金属的表面积或颗粒大小相同.
(2)他们改正后重新实验,得出与课本相同的结论是铝的活动性比铁强.请写出铁与稀盐酸反应的化学方程式Fe+2HCl=FeCl2+H2↑.
【应用拓展】请再设计一个与上述不同的实验方案,也能得到以上相同的正确结论.
小组同学通过对生活中金属制品的观察和课本所学的知识,仍能得出同样的正确结论.你的解释是铝在常温下就能与氧气反应形成一层致密的氧化铝薄膜,而铁在常温下与氧气几乎不反应.
0 146351 146359 146365 146369 146375 146377 146381 146387 146389 146395 146401 146405 146407 146411 146417 146419 146425 146429 146431 146435 146437 146441 146443 146445 146446 146447 146449 146450 146451 146453 146455 146459 146461 146465 146467 146471 146477 146479 146485 146489 146491 146495 146501 146507 146509 146515 146519 146521 146527 146531 146537 146545 211419
(1)小组同学取来相同质量的铁、铝分别放入起始温度相同、体积也相同的10%稀盐酸中,一开始观察到的现象是铁表面有气泡,而铝无明显现象,小明于是得出与课本中相反的结论.小文同学马上提出质疑,你认为质疑的主要理由是铝表面有一层致密的氧化铝(或未打磨金属).一开始铝表面现象不明显,但此时发生的化学方程式为Al2O3+6HCl=2AlCl3+3H2O.为了达到实验目的,除了以上条件相同外,你认为还要控制2中金属的表面积或颗粒大小相同.
(2)他们改正后重新实验,得出与课本相同的结论是铝的活动性比铁强.请写出铁与稀盐酸反应的化学方程式Fe+2HCl=FeCl2+H2↑.
【应用拓展】请再设计一个与上述不同的实验方案,也能得到以上相同的正确结论.
| 操作方法 | 实验现象 |
| 将打磨过的铝放入硫酸亚铁溶液中,观察现象 或打磨过的铁钉放入硫酸铝溶液中,观察现象 | 铝表面出现固体,溶液由浅绿色慢慢变成无色 或无明显变化 |
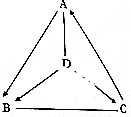 如图所示,A一D是九年级化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应(部分物质和反应条件未标出).已知B、C均为氧化物,D为胃液中的主要成分.
如图所示,A一D是九年级化学常见的物质.图中“→”表示转化关系,“-”表示相互能反应(部分物质和反应条件未标出).已知B、C均为氧化物,D为胃液中的主要成分.