3.某化学课堂围绕“酸碱中和反应”,将学生分成若干小组,在老师引导下开展探究活动.以下是教学片段,请你参与学习并帮助填写空格(包括表中空格).
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
Ⅰ.定性探究
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由猜想四;H2SO4和NaOH在溶液中不能共存.
【继续实验】
(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,分别进行如下三组探究实验.
【得出结论】通过探究,全班同学一致确定猜想二是正确的.
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中明显的一处错误是pH试纸浸入溶液中;
(2)实验方案探究中也有一个是不合理的,不合理的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
II.定量探究
取上述【演示实验】反应后烧杯中的溶液100g,设计如图实验:

计算反应后溶液中Na2SO4的质量分数是多少?(请列出计算过程)
【演示实验】将一定量的稀H2SO4加入到盛有NaOH溶液的烧杯中.
【学生板演】该反应的化学方程式H2SO4+2NaOH=Na2SO4+2H2O.
Ⅰ.定性探究
【提出问题】实验中未观察到明显现象,部分同学产生了疑问:反应后溶液中溶质是什么呢?
【猜想】针对疑问大家纷纷提出猜想.甲组同学的猜想如下:
猜想一:只有Na2SO4 猜想二:有Na2SO4和H2SO4
猜想三:有Na2SO4和NaOH 猜想四:有Na2SO4、H2SO4和NaOH
乙组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是哪一种并说出理由猜想四;H2SO4和NaOH在溶液中不能共存.
【继续实验】
(1)丙组同学取烧杯中的少量溶液于试管中,滴加几滴CuSO4溶液,无明显变化,溶液中一定没有NaOH.
(2)为了验证其余猜想,各组同学取烧杯中的溶液,并选用老师提供的pH试纸、铜片、BaC12溶液、Na2CO3溶液,分别进行如下三组探究实验.
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaCl2溶液 |
| 实验操作 | 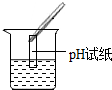 | 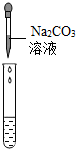 |  |
| 实验现象 | 试纸变色,比照比色卡,pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
【评价反思】老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定.同时指出上述三个实验探究中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
(1)实验操作中明显的一处错误是pH试纸浸入溶液中;
(2)实验方案探究中也有一个是不合理的,不合理的原因是Na2SO4与BaCl2反应也会生成白色沉淀,不能证明一定有H2SO4存在.
II.定量探究
取上述【演示实验】反应后烧杯中的溶液100g,设计如图实验:

计算反应后溶液中Na2SO4的质量分数是多少?(请列出计算过程)
1.善于梳理化学知识,能使你头脑更聪明.以下有错误的一组( )
| A | 化学变化中的能量变化 | B | 化肥知识 |
| 蜡烛燃烧--放热反应 碳还原二氧化碳--吸热反应 | 钾肥作用--增强抗寒、抗旱能力 使用事项--不能与碱性物质共用 | ||
| C | 元素与人体健康 | D | 化学原理解释生活常识 |
| 缺锌--易引起食欲不振,发育不良 缺钙--易骨质疏松或得佝偻病 | 用氢氧化钠去油污--与油脂反应 用 汽油除去油污--溶解作用 |
| A. | A | B. | B | C. | C | D. | D |
20.红枣常食有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”.其标签如图所示.某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】①铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
②碳酸钠溶液和氢氧化钙溶液反应会生成碳酸钙沉淀,反应的方程式为:
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究】
【实验质疑】
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙会和水反应生成氢氧化钙.
(2)甲同学的实验中如果含有Fe2O3,则会和盐酸发生反应,Fe2O3和盐酸发生反应的方程式为①Fe2O3+6HCl═2FeCl3+3H2O,丙同学思考后认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是②氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色
他们设计如下实验方案继续验证.

乙同学对滤渣B进行探究.
【反思与评价】
(1)乙同学经过实验测得上述滤渣C的质量为1.0g,计算滤液A中含氢氧化钙的质量.(写出解题过程)
(2)丙同学经过实验测得磁铁吸引后残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g.综合上述实验及乙、丙同学的数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
(3)结合固体的成分,你认为这包“504双吸剂”,除了能吸收空气中的水分外,还能吸收空气中的氧气从而达到防腐的作用.
0 146208 146216 146222 146226 146232 146234 146238 146244 146246 146252 146258 146262 146264 146268 146274 146276 146282 146286 146288 146292 146294 146298 146300 146302 146303 146304 146306 146307 146308 146310 146312 146316 146318 146322 146324 146328 146334 146336 146342 146346 146348 146352 146358 146364 146366 146372 146376 146378 146384 146388 146394 146402 211419
【提出问题】久置固体的成分是什么?
【查阅资料】①铁与氯化铁溶液在常温下发生反应生成氯化亚铁;
②碳酸钠溶液和氢氧化钙溶液反应会生成碳酸钙沉淀,反应的方程式为:
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红. | 固体中一定含有①CaO 和氢氧化钙. |
| (2)另取少量固体放于试管中,滴加足量的稀盐酸. | 固体逐渐消失,有大量②气泡产生,得到浅绿色溶液. | 固体中一定含有③Fe, 一定不含Fe2O3 |
(1)乙同学认为甲同学的实验中不能得出一定含Ca(OH)2的结论,理由是氧化钙会和水反应生成氢氧化钙.
(2)甲同学的实验中如果含有Fe2O3,则会和盐酸发生反应,Fe2O3和盐酸发生反应的方程式为①Fe2O3+6HCl═2FeCl3+3H2O,丙同学思考后认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是②氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色.
氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色
他们设计如下实验方案继续验证.

乙同学对滤渣B进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、有气泡冒出、溶液变为黄色溶液变为黄色、澄清的石灰水变浑浊 澄清的石灰水变浑浊 | 固体中一定含有 ③CaCO3和Fe2O3 |
(1)乙同学经过实验测得上述滤渣C的质量为1.0g,计算滤液A中含氢氧化钙的质量.(写出解题过程)
(2)丙同学经过实验测得磁铁吸引后残留固体中含钙物质的总质量为1.6g,滤渣B中CaCO3的质量为1.0g.综合上述实验及乙、丙同学的数据,久置固体的成分是Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
(3)结合固体的成分,你认为这包“504双吸剂”,除了能吸收空气中的水分外,还能吸收空气中的氧气从而达到防腐的作用.
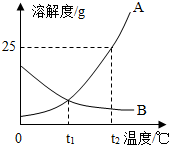 如图为A、B两种固体物质的溶解度曲线.
如图为A、B两种固体物质的溶解度曲线.